Роль 18-ФДГ ПЕТ/КТ у плануванні радіотерапії пухлин аноректальної локалізації: стан проблеми
Колеснік О.О., Ашихмін А.В., Солодянникова О.І., Кметюк Я.В., Мусаєва К.О.
Резюме. 3D-Конформна радіотерапія та модульована за інтенсивністю радіотерапія є основними методиками променевого лікування пацієнтів із пухлинами аноректальної локалізації. Комп’ютерна томографічна симуляція є рутинною основою планування радіотерапії, проте має низку обмежень, наприклад: низьку контрастність м’яких тканин порожнини таза, частковий об’ємний ефект. Магнітно-резонансна томографія та позитронно-емісійна томографія подолали ці обмеження та забезпечують додаткову цінну інформацію для планування радіотерапії аноректальної зони. На додаток позитронно-емісійна томографія дозволяє уточнювати стадію пухлини, а також сприяє досягненню консенсусу при оконтурюванні цільових об’ємів. Однак залишається низка невирішених проблем для введення цього методу у рутинне застосування в клінічній онкологічній практиці.
 Передопераційна хіміорадіотерапія є стандартним неоад’ювантним етапом лікування при локально-розповсюджених аноректальних карциномах. При поєднанні радіотерапії з хіміотерапією значно зменшуються локальні розміри пухлини (часткова відповідь — partial response), а в 30% випадків досягається повна відповідь (complete response) із повною морфологічною регресією. У таких пацієнтів можливе проведення сфінктерзберігаючого хірургічного лікування із найнижчим рівнем локального рецидивування, найкращими показниками 5-річної виживаності та збереженням якості життя порівняно з післяопераційним курсом хіміорадіотерапії [4–6].
Передопераційна хіміорадіотерапія є стандартним неоад’ювантним етапом лікування при локально-розповсюджених аноректальних карциномах. При поєднанні радіотерапії з хіміотерапією значно зменшуються локальні розміри пухлини (часткова відповідь — partial response), а в 30% випадків досягається повна відповідь (complete response) із повною морфологічною регресією. У таких пацієнтів можливе проведення сфінктерзберігаючого хірургічного лікування із найнижчим рівнем локального рецидивування, найкращими показниками 5-річної виживаності та збереженням якості життя порівняно з післяопераційним курсом хіміорадіотерапії [4–6].
Проте досі є актуальним зниження гострої та пізньої токсичності при опроміненні прилеглих структур (петель тонкого кишечнику, сечового міхура, головок стегнових кісток). Модульована за інтенсивністю радіотерапія (МІРТ) забезпечує висококонформний розподіл дози в цільових об’ємах і мінімізує дозу, отриману прилеглими дозолімітуючими структурами, що в свою чергу зменшує прояви токсичності при підведенні більших доз до пухлинного осередку [11, 12].
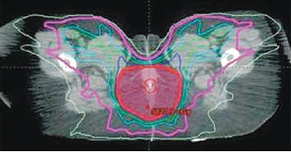
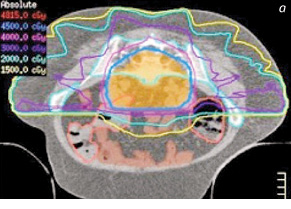
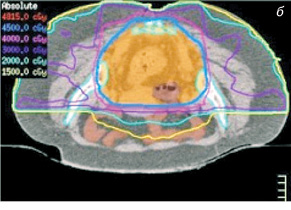
Наводимо план опромінення з використанням технології МІРТ (рис. 1–3).
Візуалізаційні модальності, застосовувані для симуляції МІРТ
З метою визначення найменшого виправданого цільового об’єму при плануванні МІРТ важливо використовувати високоякісні діагностичні зображення. Історично склалося, що симуляцію та планування радіотерапії при карциномах прямої кишки проводили за даними рентгенографії, виконаної в ортогональних проекціях. Для визначення цільових об’ємів опромінення використовували кісткові орієнтири та контрастування порожнини кишечнику.
Завдяки впровадженню сучасного програмного забезпечення для планування та комп’ютерної томографії (КТ) визначення цільових об’ємів значно вдосконалилося за рахунок тривимірної конформної радіотерапії (3D-КРТ). Подальші дослідження продемонстрували переваги планування радіотерапії за даними КТ-зображень: підвищилася точність визначення меж пухлини, знизилася токсичність тощо [16].
Разом із тим КТ-візуалізація структур малого таза має певні обмеження за рахунок низької контрастності м’яких тканин. Також слід враховувати, що при оконтурюванні цільових об’ємів карциноми прямої кишки необхідно забезпечити максимальну контрастність нормальних і пухлинно-інфільтрованих тканин [15, 17].
За останні два десятиріччя методом, що дає найбільш точну візуалізацію при локально-розповсюдженій карциномі прямої кишки, стала магнітно-резонансна томографія (МРТ). Чутливість методу щодо визначення глибини пухлинної інвазії та метастатичного ураження лімфовузлів становить 71–91%, специфічність — 78–100%. Порівняно з КТ, МРТ більш інформативна для визначення глибини пухлинної інвазії локальних структур через стінку прямої кишки, ураження пресакральної та мезоректальної клітковини, які є зонами високого ризику рецидиву, встановлення макроскопічного об’єму пухлини (МОП). Вищевказана інформація може сприяти збереженню анального сфінктера при хірургічному лікуванні та зменшенню дози опромінення на навколишні нормальні тканини при збереженні достатньої лікувальної дози на пухлинний осередок [2, 7]. У дослідженні, в якому порівнювали КТ- та МРТ-симуляцію радіотерапії, встановлено, що КТ-дані є прийнятними для точного оконтурювання МОП, при цьому дані МРТ-дослідження доповнюють та уточнюють інформацію про об’єм пухлини, її протяжність, розповсюдженість відносно анального каналу, особливо у випадках анальної чи сигмоїдної інвазії. Проте використання лише МРТ-зображень для планування радіотерапії не є оптимальним, тому що така методика, на відміну від КТ, не забезпечує достатній обсяг інформації про електронну щільність об’єкта, за рахунок чого досягається точне визначення доз із урахуванням тканинної негомогенності цільового об’єму. Тому на практиці застосовують мультимодальний підхід із використанням КТ- і МРТ-досліджень малого таза на планувальній робочій станції [7].
Особливості застосування 18-ФДГ ПЕТ/КТ при плануванні та контролі ефективності МІРТ пухлин аноректальної локалізації
Позитронно-емісійна томографія (ПЕТ)/КТ на основі одержання метаболічного зображення забезпечує найбільш надійний і точний спосіб визначення істинних розмірів пухлини.
Фтор-18-флуородезоксиглюкоза (18-ФДГ) є найрозповсюдженішим радіофармпрепаратом, який застосовується в онкологічній візуалізації, а також єдиним препаратом, що використовується при плануванні радіотерапії. 18-ФДГ є аналогом глюкози, інкорпорується у клітини пухлини через мембранні транспортні канали глюкози та потрапляє в метаболічну «пастку» при фосфорилюванні гексокіназами. Акумуляція 18-ФДГ у клітинах пухлини зумовлена тканинним кровотоком у пухлині, активністю мембранних транспортних каналів, ферментів-гексокіназ і загальним рівнем споживання глюкози. При патогістологічній оцінці видно, що пухлинне утворення складається з неопластичних клітин, строми та реактивних клітин запалення (макрофаги, лімфоцити тощо) у різних співвідношеннях. Накопичення 18-ФДГ відбувається як у неопластичних клітинах, так і в туморасоційованих клітинах запалення. Інакше кажучи, 18-ФДГ є неспецифічним трейсером для виявлення неопластичних клітин, що забезпечує при ПЕТ/КТ найкращу візуалізацію для стадіювання [1, 8].
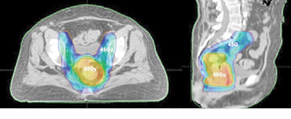
Наводимо деякі власні ілюстрації, які демонструють діагностичні можливості 18-ФГД ПЕТ/КТ у виявленні та розповсюдженні пухлин аноректальної локалізації (рис. 4, 5).
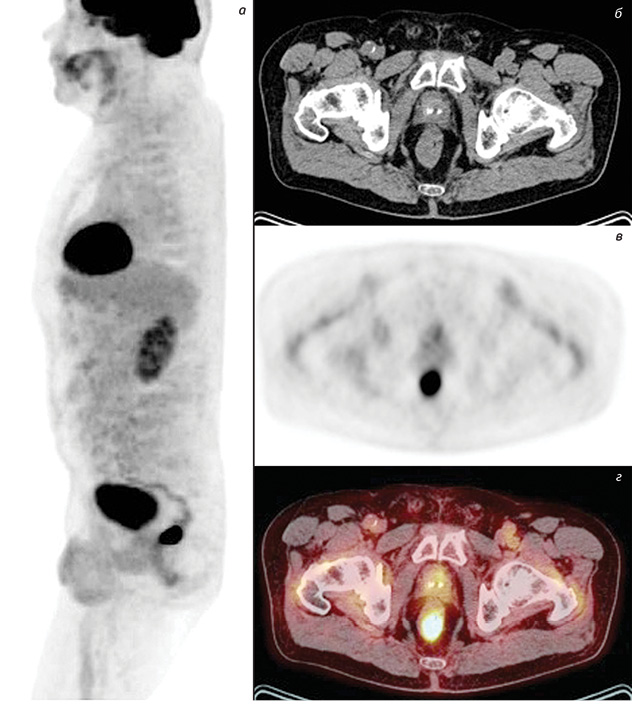
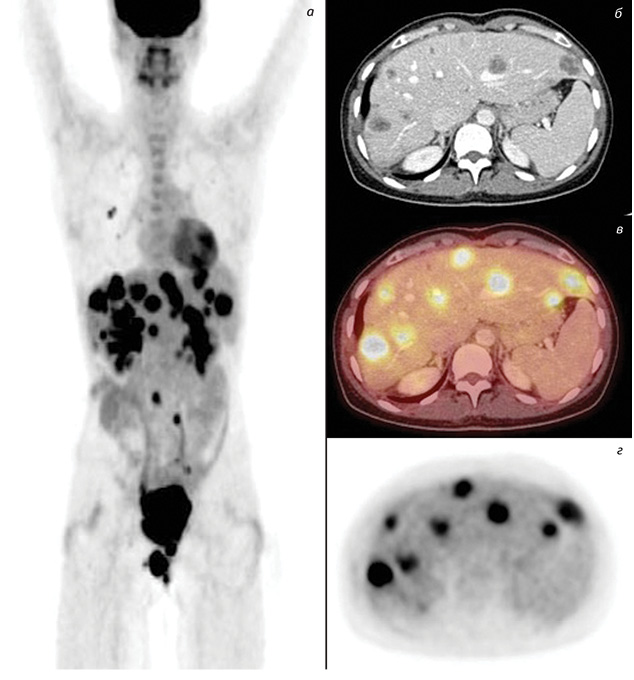
На сьогодні досвід клінічного застосування 18-ФДГ ПЕТ/КТ доводить доцільність використання такої візуалізації в онкології, а саме: для диференційної діагностики, стадіювання перед хірургічним або променевим лікуванням, рестадіювання після терапії.
18-ФДГ ПЕТ/КТ також продемонструвала високу чутливість при моніторингу терапевтичної ефективності хіміо- та радіотерапії [13].
За результатами численних досліджень щодо використання 18-ФДГ ПЕТ/КТ-зображень для подальшого динамічного контролю та планування радіотерапії виявлено найбільшу точність системного та локорегіонарного стадіювання порівняно з конвенційними КТ- і МРТ-методиками. Встановлено, що МОП, визначений за даними ПЕТ/КТ, є статистично значно більшим за встановлений за допомогою КТ із середньою різницею 25%. При цьому при порівнянні МОП, визначеного за МРТ та ПЕТ/КТ, виявлено тенденцію до переоцінки об’єму пухлини в середньому на 11% за даними МРТ [7, 10, 11].
Саме тому ПЕТ/КТ активно впроваджується у відділеннях радіотерапії для планування та оцінки контролю якості. Раціональність застосування функціональних 18-ФДГ ПЕТ/КТ-зображень при плануванні радіотерапії карцином прямої кишки та анального каналу обґрунтована високою чутливістю та специфічністю ПЕТ/КТ порівняно зі стандартними структурними методиками візуалізації. Середня чутливість і специфічність 18-ФДГ ПЕТ/КТ становить 83 і 91% відповідно та при КТ — 64 і 74% відповідно [1, 3, 14]. Проте слід враховувати, що дрібні вогнища (<1 см) можуть достовірно не визначатися на ПЕТ-зображеннях при проведенні ПЕТ/КТ. У пацієнтів із цукровим діабетом хибнонегативні результати 18-ФДГ ПЕТ/КТ можуть бути зумовлені некоригованою гіперглікемією на момент проведення дослідження. Протягом перших тижнів після хіміотерапії резидуальні елементи пухлини мають пригнічену метаболічну активність, що також призводить до хибнонегативних результатів (рис. 6).
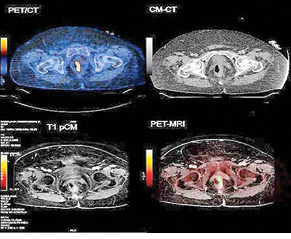
Дані 18-ФДГ ПЕТ/КТ-дослідження застосовують уже на етапі відбору пацієнтів для проведення радикальної терапії через високий потенціал ПЕТ/КТ у виявленні віддалених вогнищ метастазування. Це допомагає виключити пацієнтів, яким показане лише паліативне лікування (за деякими даними, до 30%), що загалом покращує показники виживаності пацієнтів, що пройшли радикальний курс лікування [1, 4].
У подальшому виконане ПЕТ/КТ-дослідження використовують для планування радіотерапії. 18-ФДГ ПЕТ/КТ-зображення забезпечує не лише функціональну, але й найдетальнішу анатомічну інформацію за рахунок КТ-даних. Як результат, з’являється можливість найбільш точно визначити справжній МОП і значно знизити розбіжність контура при плануванні радіотерапії декількома спеціалістами [9].
На точність оконтурювання цільових об’ємів на основі ПЕТ впливають декілька факторів:
- точне визначення меж МОП залежить від фізичних обмежень роздільної здатності ПЕТ-технології (найменша роздільна здатність становить 4,5 мм), що впливає на чіткість контура;
- чутливість ПЕТ залежить від рівня фіксації радіотрейсера в тому випадку, якщо він щонайменше в 4 рази перевищує такий у навколишніх тканинах;
- виявлення вогнищ підвищеної фіксації радіофармпрепарату залежить від різниці вогнища та фонової ділянки, артефактів, параметрів ширини вікна та кольорової шкали, досвіду оператора.
Таким чином, при оконтурюванні біологічних і цільових об’ємів для проведення радіотерапії застосовують поєднання напівкількісних методик визначення меж інтенсивності ПЕТ-сигналу та візуальний аналіз КТ-даних.
Висновок
Впровадження МІРТ дозволяє підвищити ефективність радіотерапії пухлин анальної та ректальної зон із мінімізацією опромінення критичних органів. Оскільки і досі не визначено єдиного ідеального методу візуалізації точних меж пухлин, на практиці застосовують поєднання візуального та автоматичного оконтурювання за даними одразу декількох функціональних і структурних візуалізаційних модальностей (КТ, МРТ, ПЕТ).
Список використаної літератури
1. IAEA The Role of PET/CT in Radiation Treatment Planning for Cancer Patient Treatment / IAEA-TECDOC-1603. — October 2008.
2. Myerson R., Garofalo M., Naqa I.E. еt al. (2007) Elective clinical target volumes in anorectal cancer. Washington University: An RTOG Consensus Panel Contouring Atlas.
3. Arbea L., Ramos L.I., Martínez-Monge R. еt al. (2010) Intensity-modulated radiation therapy (IMRT) vs. 3D conformal radiotherapy (3DCRT) in locally advanced rectal cancer (LARC): dosimetric comparison and clinical implications. Rad. Oncol., 5: 17.
4. Buijsen J. (2015) Rectal cancer: steps towards tailored treatment. Schimmert, Uitgeverij BOXPress, ‘s-Hertogenbosch.
5. Grigsby P.W. (2009) FDG-PET/CT: new horizons in anal cancer. Elsevier Masson: Gastroenterologie Clinique et Biologique, 33: 456–458.
6. Radu C. (2012) Optimizing radiotherapy in rectal cancer patients. Digital Comprehensive Summaries of Uppsala Dissertations from the Faculty of Medicine, 775: 57.
7. Yan Yang Wang, Hong Zhe (2013) Clinical application of multimodality imaging in radiotherapy treatment planning for rectal cancer. Cancer Imaging, 13(4): 495–501.
8. Buijsen J., van den Bogaard J., van der Weide H. еt al. (2012) FDG-PET-CT reduces the interobserver variability in rectal tumor delineation. Radiother. Oncol., 102: 371–376.
9. Jun Shang, Wei Kong, Yan-Yang Wang (2014) VMAT planning study in rectal cancer patients. Radiat. Oncol., 9: 219.
10. Withofs N., Bernard C., van der Rest C. еt al. (2014) FDG PET/CT for rectal carcinoma radiotherapy treatment planning: comparison of functional volume delineation algorithms and clinical challenges. J. Аpplied Clinical Medical Physics, 15(5): 2014.
11. Mok H., Crane C.H., Matthew B. еt al. (2011) Palmer intensity modulated radiation therapy (IMRT): differences in target volumes and improvement in clinically relevant doses to small bowel in rectal carcinoma. Radiat. Oncol., 6: 63.
12. Parekh A., Tam Truong M., Pashtan I. еt al. (2013) Acute gastrointestinal toxicity and tumor response with preoperative intensity modulated radiation therapy for rectal cancer. Gastrointest. Cancer Res., 6: 137–143.
13. Gregoire V., Haustermans K., Geets X. еt al. (2007) PET-based treatment planning in radiotherapy: a new standard? J. Nucl. Med., 48: 68S–77S.
14. Ford E.C., Herman J., Yorke E. еt al. (2009) 18F-FDG PET/CT for image-guided and intensity-modulated radiotherapy. J. Nucl. Med., 50(10): 1655–1665.
15. Schinagl D.A., Kaanders J.H., Oyen W.J. (2006) From anatomical to biological target volumes: the role of PET in radiation treatment planning. Mini symposium: PET — the future, Cancer Imaging: S107–S116.
16. Burnet N.G., Thomas S.J., Burton K.E. еt al. (2004) Defining the tumour and target volumes for radiotherapy. Cancer Imaging, 4: 153–161.
17. Niyazi M., Landrock S., Elsne A. еt al. (2013) Automated biological target volume delineation for radiotherapy treatment planning using FDG-PET/CT. Radiat. Oncol., 8: 180.
Роль 18-ФДГ ПЭТ/КТ в планировании радиотерапии опухолей аноректальной локализации: состояние проблемы
Национальный институт рака, Киев
Всеукраинский центр радиохирургии клинической больницы «Феофания», Киев
Резюме. 3D-Конформная радиотерапия и модулированная по интенсивности радиотерапия — основные методики лучевого лечения пациентов с опухолями аноректальной локализации. Компьютерно-томографическая симуляция — основная методика в планировании радиотерапии, которая имеет ряд ограничений, например: низкую контрастность мягких тканей полости таза, частичный объемный эффект. Магнитно-резонансная томография и позитронно-эмиссионная томография преодолели подобные ограничения и обеспечивают дополнительную ценную информацию для планирования радиотерапии опухолей аноректальной локализации. Также следует отметить, что позитронно-эмиссионную томографию возможно использовать для уточнения стадирования, что также способствует достижению консенсуса при оконтуривании целевых объемов. Однако остается ряд нерешенных проблем для введения этого метода в рутинное применение в клинической онкологической практике.
ПЭТ/КТ, радиотерапия, опухоли прямой кишки, опухоли анального канала.
Адреса:
Солодянникова Оксана Іванівна
03022, Київ, вул. Ломоносова, 33/43
Національний інститут раку
E-mail: iloi@ua.fm














Leave a comment