Лансурф® як кардіолагідна альтернатива класичним фторпіримідинам
Резюме. Класичні фторпіримідини — 5-флуороурацил (5-ФУ) і капецитабін — широко застосовуються в онкології, проте їх прийом обмежується токсичністю, зокрема розвитком долонно-підошовного синдрому та кардіотоксичних ускладнень. Повторне призначення після епізоду кардіотоксичності супроводжується високим ризиком її рецидиву, що ускладнює подальшу терапію. У цьому контексті особливий інтерес становить трифлуридин / типірацил (TAS-102, Лансурф®) — пероральний комбінований препарат, схвалений для лікування хімієрефрактерного метастатичного колоректального раку. Його механізм дії базується на інкорпорації трифлуридину в ДНК пухлинних клітин та інгібуванні тимідилатсинтази, при цьому метаболізм препарату не залежить від активності дигідропіримідиндегідрогенази (DPD), що вигідно вирізняє його від 5-ФУ та капецитабіну і розширює можливості застосування у пацієнтів із дефіцитом DPD. Крім того, застосування препарату не супроводжується розвитком вираженого долонно-підошовного синдрому, що покращує переносимість лікування і збереження якості життя хворих. Кардіотоксичність при застосуванні препарату Лансурф® є мінімальною — аналіз численних клінічних досліджень не виявив значущого підвищення ризику серцево-судинних ускладнень порівняно з плацебо, що дозволяє розглядати лікарський засіб як кардіолагідний фторпіримідин. Отже, препарат Лансурф® є клінічно обґрунтованою альтернативою класичним фторпіримідинам із кращою переносимістю, нижчим ризиком кардіотоксичності та незалежністю від статусу DPD.
DOI: 10.32471/clinicaloncology.2663-466X.35769
Кардіотоксичність протипухлинної терапії є однією з найважливіших проблем сучасної онкології, оскільки поєднує 2 провідні чинники смертності у світі — онкологічні та серцево-судинні захворювання. Водночас у цьому контексті особливого значення набуває питання кардіобезпеки, яке часто залишається недостатньо висвітленим у клінічних дослідженнях. Це пов’язано з тим, що частина кардіотоксичних ускладнень має відстрочений характер і може проявлятися через місяці або роки після завершення терапії. Крім того, обмежена тривалість спостереження та відносно невелика кількість учасників у деяких дослідженнях зменшують можливість виявлення пізніх побічних ефектів. У результаті окремі прояви кардіотоксичності стають очевидними вже після широкого впровадження препаратів у клінічну практику.
Кардіотоксичність у онкології: від антрациклінів до фторпіримідинів
За рекомендаціями Європейського товариства медичної онкології (European Society for Medical Oncology — ESMO) 2022 р., до протипухлинних препаратів із потенційною кардіотоксичною дією належать антрациклінові агенти, алкілуючі препарати, цисплатин, фторурацил, капецитабін, доцетаксел, вінбластин, моноклональні антитіла, інгібітори тирозинкінази, імунотерапевтичні та ендокринні лікарські засоби. Частота кардіотоксичності загалом невисока, але певний відсоток пацієнтів, особливо за наявності факторів ризику (вік, супутні хвороби, комбінації препаратів), все ж уражується.
Антрациклінові препарати здебільшого викликають порушення скоротливості міокарда та лівошлуночкову недостатність із кумулятивним дозовим ризиком, тоді як фторпіримідини частіше спричиняють коронарний вазоспазм без чіткого дозового ліміту. Для антрациклінів існують стандартизовані рекомендації щодо діагностики, моніторингу, лікування та профілактики кардіотоксичності; для фторпіримідинів такі підходи менш розроблені. Концепція «дозволеної кардіотоксичності» дозволяє продовжувати лікування при легких або контрольованих формах кардіотоксичних проявів, що ефективно застосовується при антрацикліновій терапії. Для фторпіримідинів кардіотоксичність частіше є гострою та потенційно небезпечною для життя, що обмежує можливість використання цієї стратегії [1].
Кардіотоксичність фторпіримідинів: епідеміологія, фактори ризику, клінічні прояви та стратегії ведення
Фторпіримідини, зокрема 5-ФУ та його пероральний аналог капецитабін, уже десятиліттями посідають ключове місце як у монотерапії, так і в комбінаціях для лікування злоякісних новоутворень шлунково-кишкового тракту, грудної залози, голови, шиї та ін. [2]. Їх дія ґрунтується на пригніченні тимідилатсинтази та включенні фторпіримідинових нуклеотидів у ДНК і РНК пухлинних клітин [3]. Застосування 5-ФУ і капецитабіну може супроводжуватися розвитком побічних ефектів, зокрема мієлосупресії, мукозиту, діареї, долонно-підошовного синдрому, проявів нейро- і кардіотоксичності [4, 5].
Епідеміологія
Кардіотоксичність фторпіримідинів часто недооцінюється, проте не є рідкісною: за даними численних досліджень, її частота коливається в межах 1,2–18%, а окремі роботи повідомляють про показники до 30% [5]. Сьогодні точна поширеність кардіотоксичності, асоційованої з 5-ФУ або капецитабіном, залишається невизначеною через значну варіабельність результатів. У більшості випадків кардіотоксичність є оборотною за умови раннього виявлення та припинення терапії. Однак можливий розвиток тяжких серцевих подій і летальність, рівень якої варіює в діапазоні 2,2–13% [6], переважно внаслідок інфаркту міокарда, застійної серцевої недостатності або тяжких аритмій.
Фактори ризику кардіотоксичності фторпіримідинів
Ризик кардіотоксичності фторпіримідинів підвищується під впливом численних факторів, пов’язаних із характеристиками пацієнта або лікуванням. Виявлення таких факторів допомагає визначити пацієнтів із високим ризиком та прогнозувати можливі ускладнення.
Серед характеристик пацієнта, що потенційно впливають на розвиток кардіотоксичності при отриманні хворими фторпіримідинів, розглядають вік, чоловічу стать, чорну расу та підвищений індекс маси тіла (ІМТ) [5]. Однак їхній вплив на розвиток кардіотоксичності фторпіримідинів залишається дискусійним.
Не менш важливим є й тип протипухлинної терапії: профілі серцево-судинної токсичності 5-ФУ та капецитабіну загалом вважаються подібними, оскільки більшість досліджень не виявили суттєвих відмінностей у частоті, типі чи ступені тяжкості кардіотоксичних подій [5]. Водночас у великому проспективному дослідженні (527 пацієнтів) симптоматична кардіотоксичність частіше відмічалася при застосуванні капецитабіну (33,8%) порівняно з 5-ФУ (25%; p=0,0042), тоді як у ретроспективному аналізі виявлено вищий ризик подій при внутрішньовенному введенні 5-ФУ порівняно з пероральним капецитабіном [7]. Супутня терапія може суттєво впливати на серцево-судинний ризик. Наприклад, схеми з бевацизумабом або панітумумабом асоціювалися з вищою частотою ускладнень: панітумумаб — з аритміями, бевацизумаб — з ішемічними подіями [8]. Комбінація капецитабіну з бевацизумабом та оксаліплатином також підвищувала частоту кардіотоксичності порівняно з монотерапією, тоді як додавання іринотекану не підвищувало загальну частоту подій, але асоціювалося з побічними ефектами ≥III ступеня тяжкості. Важливу роль у розвитку кардіотоксичності при отриманні фторпіримідинів відіграють доза, режим і спосіб введення. Безперервна інфузія 5-ФУ частіше асоціюється з ускладненнями, ніж болюсне введення, а вищі дози зумовлюють зростання ризику, що підтверджує дозозалежний характер токсичності. Більшість серцево-судинних подій, зокрема коронарний вазоспазм, виникають під час першого циклу лікування, що підкреслює необхідність ретельного моніторингу з початку терапії [5].
Механізми та патофізіологія кардіотоксичності
Точні механізми кардіотоксичності, індукованої фторпіримідинами, залишаються недостатньо з’ясованими. Серед основних запропонованих механізмів розглядають коронарний вазоспазм, пряму міокардіальну токсичність, ендотеліальну дисфункцію та порушення гомеостазу еритроцитів і заліза [5].
Клінічна картина
Спектр серцевих проявів, пов’язаних з фторпіримідинами, є широким. Найчастіше пацієнти повідомляють про стенокардіоподібний біль у грудній клітці, що відмічається у понад 50% випадків кардіотоксичності 5-ФУ. Тип болю може залежати від способу введення: болюсні інфузії зазвичай викликають типовий біль, пов’язаний із вазоспазмом, що з’являється одразу після першого циклу з характерними змінами на електрокардіограмі (ЕКГ), тоді як безперервні інфузії частіше спричиняють атипову стенокардію з циклічними рецидивами. Хоча коронарний вазоспазм вважається основним механізмом, спектр проявів включає аритмії та випадки без чітких вазоспастичних тригерів. Часто також фіксували брадикардію, включно з атріовентрикулярними блокадами та блокадою ніжок пучка Гіса, а також фібриляцію, тріпотіння передсердь, надшлуночкову та шлуночкову тахікардію, фібриляцію шлуночків. Рідше повідомляли про тяжкі події, зокрема ішемію або інфаркт міокарда, дилатаційну кардіоміопатію, застійну серцеву недостатність, кардіогенний шок, зупинку серця та раптову смерть, а також артеріальну гіпертензію та злоякісну артеріальну гіпертензію. У деяких випадках виявляли перикардит, міоперикардит та рідкісну кардіоміопатію такоцубо [5].
Діагностика
Біомаркери є потенційним інструментом раннього виявлення серцевого пошкодження, але їхня роль при кардіотоксичності фторпіримідинів обмежена. Тропоніни T та I, BNP, NT-proBNP та копептин можуть відображати серцеве ураження, проте часто їх рівень залишається нормальним навіть за наявності клінічних симптомів. Підвищення маркерів може бути неспецифічним і виникати при інших серцевих або системних станах, що ускладнює прогнозування кардіотоксичності. ЕКГ рекомендована всім пацієнтам перед та під час лікування фторпіримідинами для оцінки серцево-судинного ризику. Найчастіше зміни на ЕКГ пов’язані з ішемією, порушенням провідності та аритміями, але в багатьох випадках вони виявляються лише після розвитку клінічних симптомів. Безсимптомні зміни також можливі, що підкреслює обмеженість ЕКГ у ранній діагностиці. Трансторакальна ехокардіографія (ТТЕ) рекомендована пацієнтам із серцевими захворюваннями в анамнезі або в разі виникнення нових симптомів. Більшість досліджень не виявляють значних змін систолічної чи діастолічної функції протягом лікування 5-ФУ, а невеликі порушення швидкостей скоротливості зазвичай виявляються тільки після розвитку кардіотоксичності.
Отже, у клінічній практиці ускладнення від фторпіримідинів часто діагностуються пізно, коли серцеве ураження вже сформоване. Це підкреслює потребу в розвитку більш чутливих методів ранньої діагностики та стратифікації ризику для своєчасного запобігання ускладненням [5].
Моніторинг та управління
Скринінг та моніторинг
Усі пацієнти, які отримують фторпіримідини, потребують базової оцінки серцево-судинного ризику з обов’язковим виявленням і корекцією модифікованих факторів ризику, зокрема гіперліпідемії, артеріальної гіпертензії та цукрового діабету. Перед початком терапії рекомендовано виконати базову ЕКГ і провести стратифікацію ризику за шкалою систематичної оцінки коронарного ризику 2 (Systematic Coronary Risk Evaluation 2 — SCORE2) / систематичної оцінки коронарного ризику 2 для осіб старшого віку (Systematic Coronary Risk Evaluation 2 Older Persons — SCORE2-OP) або еквівалентним інструментом. Пацієнтам із симптоматичними серцево-судинними захворюваннями в анамнезі слід виконати базову ТТЕ до початку лікування. У хворих із високим або дуже високим ризиком обструктивної ішемічної хвороби серця доцільним є попередній скринінг на ішемію без затримки хімієтерапії із проведенням КТ-коронарографії, ядерної перфузійної томографії, стрес-ехокардіографії або магнітно-резонансної томографії (МРТ) серця (за можливості). Під час лікування необхідно активно здійснювати контроль за виникненням нової стенокардії чи інших кардіальних симптомів. У разі їх розвитку рекомендовано проведення ЕКГ, визначення рівня тропоніну та виконання ТТЕ. За клінічними показаннями можуть застосовуватися додаткові методи обстеження, зокрема КТ-коронарографія або холтерівський моніторинг [5].
Лікування кардіотоксичності фторпіримідину
Чітких стандартизованих рекомендацій щодо лікування кардіотоксичності, спричиненої фторпіримідинами, наразі немає. Однак у разі розвитку серцевих симптомів і підтвердженої токсичності рекомендовано негайно припинити застосування 5-ФУ або капецитабіну, оскільки більшість клінічних та електрокардіографічних змін є оборотними після відміни препарату. Подальше лікування має відповідати чинним рекомендаціям залежно від конкретного серцево-судинного синдрому.
Рішення щодо повторного призначення повинно бути суворо індивідуалізованим, оскільки існує високий ризик рецидиву симптомів, особливо при коронарному вазоспазмі, що може сягати 90% і супроводжуватися значним рівнем смертності. Проте серед можливих підходів при розгляді повторного застосування фторпіримідинів (рис. 1) обговорюють зниження дози, застосування кардіопротективних препаратів, перехід на болюсні режими введення, уникнення значних фізичних навантажень, корекцію факторів ризику та ретельний моніторинг. Альтернативною стратегією є повне виключення фторпіримідинів зі схеми лікування [5]. Варто зазначити, що наразі переконливих даних щодо ефективності кардіопротективної терапії саме в контексті фторпіримідин-індукованої кардіотоксичності недостатньо [5, 6, 9].
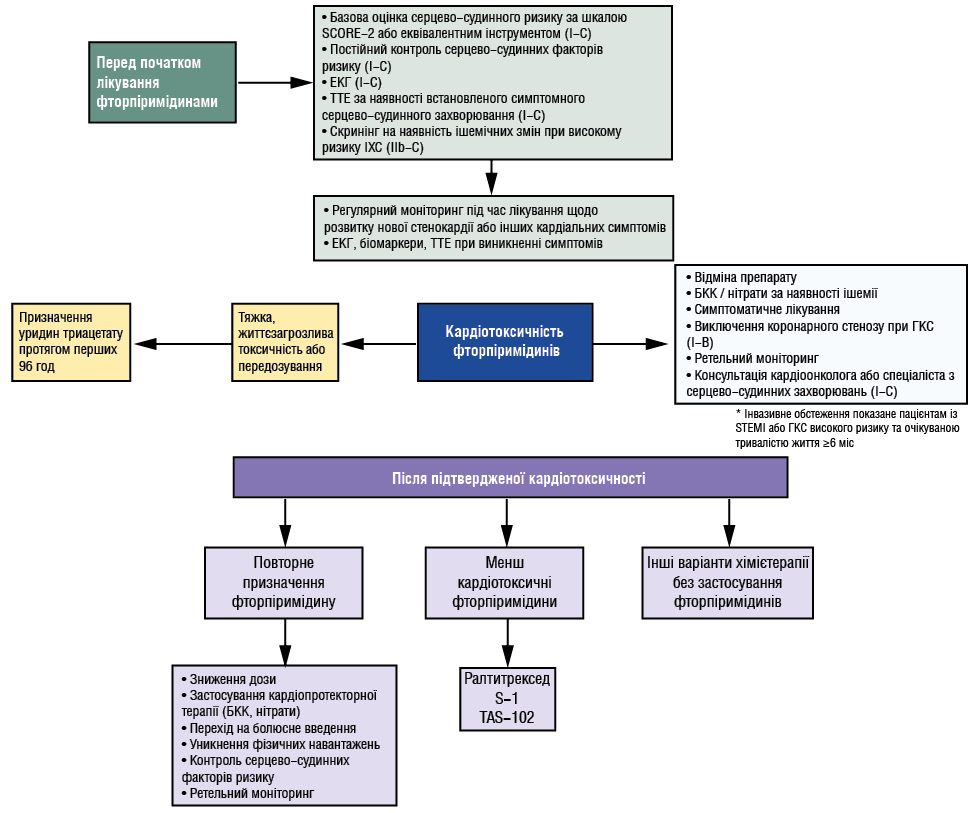
Рис. 1. Узагальнення стратегій моніторингу та ведення кардіотоксичності, спричиненої фторпіримідинами
Примітки: БКК — блокатори кальцієвих каналів; ГКС — глюкокортикостероїди; ІХС — ішемічна хвороба серця.
Перспективи застосування протипухлинних лікарських засобів з мінімальною кардіотоксичністю
Перспективним виглядає застосування менш кардіотоксичних протипухлинних препаратів. В Україні TAS-102 (трифлуридин / типірацил) офіційно зареєстровано під торговельною назвою Лансурф®*. Лансурф® є комбінованим лікарським засобом, що складається з трифлуридину та інгібітора тимідинфосфорилази типірацилу, об’єднаних у молярному співвідношенні 1:0,5. Трифлуридин реалізує протипухлинну дію через 2 основні механізми: інгібування тимідилатсинтази, подібно до 5-ФУ, а також включення трифосфатної форми трифлуридину у ДНК із подальшим формуванням одноланцюгових розривів (рис. 2). Додавання типірацилу запобігає швидкій деградації трифлуридину, підвищує його концентрацію в плазмі крові та посилює протипухлинну активність. Рекомендована доза становить 35 мг/м² двічі на добу протягом 28-денного циклу: прийом препарату протягом 5 днів із подальшою 2-денною перервою (такий 2-тижневий режим), після чого передбачено 14-денний період відпочинку [10].
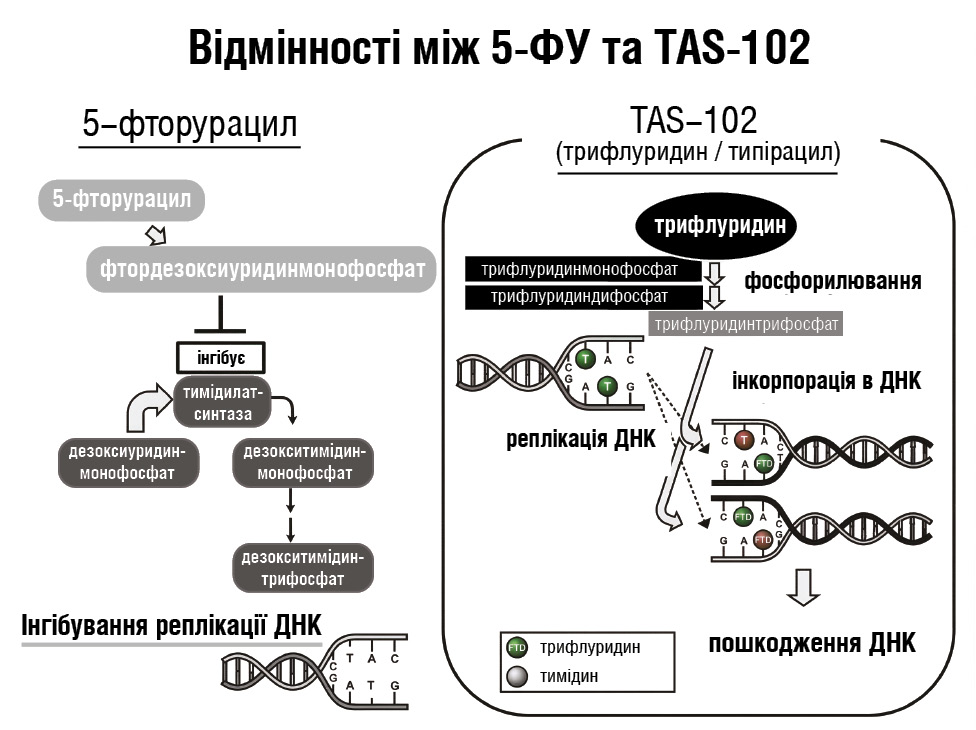
Рис. 2. Механізм дії TAS-102 порівняно з 5-ФУ
Проведено аналіз досліджень І, ІІ та ІІІ фаз з метою оцінки частоти та характеру серцево-судинних подій при застосуванні TAS-102 [11–16]. До огляду включалися лише дослідження з використанням затвердженого режиму препарату. У 4 дослідженнях І фази (загалом 121 пацієнт), включно з монотерапією TAS-102 та комбінацією з іринотеканом, кардіотоксичних подій не зафіксовано [11–14]. У дослідженні ІІ фази (112 хворих, TAS-102 проти плацебо) також не повідомлялося про серцево-судинні ускладнення [15]. У ключовому дослідженні ІІІ фази RECOURSE (800 осіб) TAS-102 сприяв підвищенню загальної виживаності на 1,8 міс, а коефіцієнт ризику смерті в групі TAS-102 порівняно з групою плацебо становив 0,68 (95% довірчий інтервал (ДІ) 0,58–0,81; p <0,001). Ця перевага є особливо значущою з огляду на те, що понад 90% пацієнтів у дослідженні мали захворювання, резистентне до фторпіримідинів на момент їх останнього застосування, а більше ніж у 50% хвороба прогресувала на тлі режиму терапії, який включав фторпіримідин як один із компонентів. Частота стоматиту ІІІ–IV ступеня, долонно-підошовного синдрому та коронарного спазму, які традиційно асоціюються з фторпіримідинами, становила менше ніж 1% у пацієнтів, які отримували препарат. Основними проявами токсичності ІІІ–IV ступеня були гематологічні: нейтропенія ≥3 ступеня (38%), фебрильна нейтропенія (4%) та анемія ≥3 ступеня (18%). Серед негематологічних побічних ефектів відзначали діарею ІІІ ступеня (3%). Тобто загалом наявні дані свідчать про низький ризик кардіотоксичності та сприятливіший профіль безпеки (препарат практично не асоціюється з розвитком долонно-підошовного синдрому) TAS-102 при збереженні клінічно значущої протипухлинної ефективності [16]. На основі аналізу вищезазначених досліджень автори огляду [10] дійшли висновку про те, що нижча кардіотоксичність TAS-102 порівняно з іншими фторпіримідинами зумовлена його відмінним механізмом дії (інкорпорація трифлуридину в ДНК без активації аутофагії), селективністю щодо пухлинних клітин та відсутністю метаболізму через DPD із утворенням кардіотоксичних метаболітів.
У метааналізі TAS-102, що охопив 869 публікацій, 17 клінічних досліджень і 1877 пацієнтів, виявлено, що порівняно з плацебо препарат не підвищує ризик інфаркту міокарда (відношення шансів (ВШ) = 1,97; 95% ДІ 0,22–17,89), артеріальної гіпертензії (ВШ=0,73; 95% ДІ 0,37–1,44), відчуття серцебиття (ВШ=1,51; 95% ДІ 0,30–7,56), зупинки серцево-легеневої діяльності (ВШ=0,83; 95% ДІ 0,11–6,32) або синкопе (ВШ=1,50; 95% ДІ 0,06–37,14), що свідчить про відсутність статистично значущого зростання кардіоваскулярних ризиків. Жодного випадку смерті від кардіотоксичності не зафіксовано. На відміну від інших фторпіримідинів, TAS-102 є кардіолагідним препаратом [17].
Окремого значення набуває проблема дефіциту дигідропіримідиндегідрогенази (DPD) — ферменту, що метаболізує до 80–90% фторпіримідинів. Фермент кодується геном DPYD; мутації цього гена призводять до часткового або повного дефіциту DPD. У разі зниження або відсутності активності ферменту відбувається накопичення токсичних метаболітів, що може спричинити тяжку токсичність (мукозит, діарею, панцитопенію, нейротоксичність), а також в окремих випадках і летальні випадки. Гетерозиготний поліморфізм (3–8%) зумовлює частковий дефіцит DPD і потребує зниження дози фторпіримідинів на 25–50%, тоді як гомозиготний варіант (0,3–0,5%) спричиняє повний дефіцит і є протипоказанням до їх застосування [18, 19]. Згідно з настановами ESMO тестування на дефіцит DPD є рекомендованою опцією перед початком терапії (зокрема фторпіримідинами при колоректальному раку) [20], тоді як настанови Національної онкологічної мережі США (National Comprehensive Cancer Network — NCCN) рекомендують розглянути таке тестування як доцільне перед початком фторпіримідин-залежної терапії, особливо після обговорення з пацієнтом ризиків і переваг [21]. Дефіцит DPD можна виявити шляхом генотипування відомих алелей ризику DPYD*2A, DPYD c.1679T>G, c.1236G>A/HapB3 та c.2846A>T або фенотипування — визначення активності ферменту DPD у мононуклеарних клітинах периферичної крові. Щороку 5-ФУ та капецитабін стають причиною сотень летальних випадків та тисяч епізодів тяжкої токсичності в Європі; тестування на DPD може запобігти щонайменше 30% таких ускладнень [22].
В українських офіційних інструкціях до капецитабіну та 5-ФУ повний дефіцит DPD визначений як протипоказання до застосування цих препаратів [23, 24], що суттєво обмежує можливості лікування частини пацієнтів. У цьому контексті особливий інтерес становить Лансурф®, схвалений для терапії пацієнтів із метастатичним колоректальним раком, які раніше отримували лікування на основі 5-ФУ або мають протипоказання до нього*. Механізми дії 5-ФУ і препарату Лансурф® відрізняються. Трифлуридин, на відміну від 5-ФУ, який інактивується DPD більш ніж на 85%, метаболізується тимідинфосфорилазою та не залежить від активності DPD (див. рис. 2). Це дозволяє розглядати його як потенційно більш безпечну терапевтичну опцію для пацієнтів із дефіцитом DPD без підвищеного ризику тяжкої токсичності та без необхідності попередньої корекції дози [22]. Крім того, у когортному ретроспективному дослідженні 6 пацієнтів із метастатичним колоректальним раком і підтвердженим дефіцитом DPD, які отримували препарат Лансурф® у стандартній дозі, лікування загалом добре переносилося: у жодного з пацієнтів не відмічалося шлунково-кишкової або гематологічної токсичності ≥III ступеня тяжкості, що потребувала б редукції дози. Це перше дослідження, яке описує застосування стандартних доз TAS-102 у пацієнтів із дефіцитом DPD [22].
Таким чином, порівняно з 5-ФУ та капецитабіном, препарат Лансурф® має низку важливих клінічних переваг. Лансурф® практично не асоціюється з розвитком долонно-підошовного синдрому, що суттєво підвищує переносимість лікування. Це сприяє збереженню якості життя пацієнтів, які часто важко переносять це ускладнення. Частота виникнення кардіотоксичності на фоні прийому препарату Лансурф® є нижчою порівняно з 5-ФУ і капецитабіном. Дія комбінації трифлуридин / типірацил не залежить від ферменту DPD, що знижує ризик тяжкої токсичності у пацієнтів із його дефіцитом. З метою мінімізації потенційно небезпечних для життя ускладнень препарат Лансурф® може розглядатися як ефективна альтернатива класичним фторпіримідинам з більш сприятливим профілем безпеки.
Список ВИКОРИСТАНОЇ літератури
1. Porter, C., Azam, T. U., Mohananey, D., Kumar, R., Chu, J., Lenihan, D., … Okwuosa, T. (2022). Permissive Cardiotoxicity: The Clinical Crucible of Cardio-Oncology. Cardio Oncology, 4(3), 302–312. doi: 10.1016/j.jaccao.2022.07.005.
2. Depetris, I., Marino, D., Bonzano, A., Cagnazzo, C., Filippi, R., Aglietta, M., & Leone, F. (2018). Fluoropyrimidine-induced cardiotoxicity. Critical reviews in oncology/hematology, 124, 1–10. doi: 10.1016/j.critrevonc.2018.02.002.
3. Longley, D. B., Harkin, D. P., & Johnston, P. G. (2003). 5-fluorouracil: mechanisms of action and clinical strategies. Nature reviews cancer, 3(5), 330–338. doi: 10.1038/nrc1074.
4. Brutcher, E., Christensen, D., Smith, M. H., Koutlas, J. B., Sellers, J. B., Timmons, T., & Thompson, J. (2018). 5-Fluorouracil and Capecitabine: Assessment and treatment of uncommon early-onset severe toxicities associated with administration. Clinical Journal of Oncology Nursing, 22(6). doi: 10.1188/18.CJON.627-634.
5. Zalaquett, Z., Shukla, N., Hajj, J., El Helou, M. C., Moudgil, R., & Collier, P. (2026). Cardiovascular Toxicity of Fluoropyrimidines: What We Know. Mayo Clinic Proceedings. 101(1), 136–155. doi: 10.1016/j.mayocp.2025.08.019.
6. Dyhl-Polk, A., Vaage-Nilsen, M., Schou, M., Vistisen, K. K., Lund, C. M., Kümler, T., … & Nielsen, D. L. (2020). Incidence and risk markers of 5-fluorouracil and capecitabine cardiotoxicity in patients with colorectal cancer. Acta Oncologica, 59(4), 475–483. doi: 10.1080/0284186X.2019.1711164.
7. Chedid El Helou, M., Laderian, B., El Hajjar, A. H., Mushtaq, A., Sadler, D., Moudgil, R., … & Collier, P. (2024). Cardiovascular toxicity of fluoropyrimidines: Experience from a quaternary referral center. Journal of Clinical Oncology, 42, e24028(2024). doi: 10.1200/JCO.2024.42.16_suppl.e24028.
8. Abdel-Rahman, O. (2019). 5-fluorouracil-related cardiotoxicity; findings from five randomized studies of 5-fluorouracil-based regimens in metastatic colorectal cancer. Clinical colorectal cancer, 18(1), 58–63. doi: 10.1016/j.clcc.2018.10.006.
9. Lombardi, P., Aimar, G., Peraldo-Neia, C., Bonzano, A., Depetris, I., Fenocchio, E., … & Leone, F. (2022). Fluoropyrimidine-induced cardiotoxicity in colorectal cancer patients: a prospective observational trial (CHECKPOINT). Oncology Reports, 49(2), 31. doi: 10.3892/or.2022.8468.
10. Petrelli, F., Barni, S., Bertocchi, P., & Zaniboni, A. (2016) TAS-102, the first «cardio-gentle» fluoropyrimidine in the colorectal cancer landscape? BMC Cancer, 16(1), 386. doi: 10.1186/s12885-016-2409-8.
11. Ohtsu, A., Yoshino, T., Boku, N., Onozawa, Y., Fukutomi, A., Hironaka, S., … & Sasaki, T. (2012). Phase I study of TAS-102 treatment in Japanese patients with advanced solid tumours. British journal of cancer, 107(3), 429–434.
12. Doi, T., Yoshino, T., Fuse, N., Boku, N., Yamazaki, K., Koizumi, W., … Ohtsu, A. (2015). Phase I study of TAS-102 and irinotecan combination therapy in Japanese patients with advanced colorectal cancer. Investigational new drugs, 33(5), 1068–1077.
13. Overman, M. J., Varadhachary, G., Kopetz, S., Thomas, M. B., Fukushima, M., Kuwata, K., … Abbruzzese, J. L. (2008). Phase 1 study of TAS-102 administered once daily on a 5-day-per-week schedule in patients with solid tumors. Investigational new drugs, 26(5), 445–454.
14. Bendell, J. C., Rosen, L. S., Mayer, R. J., Goldman, J. W., Infante, J. R., Benedetti, F., … & Patel, M. R. (2015). Phase 1 study of oral TAS-102 in patients with refractory metastatic colorectal cancer. Cancer chemotherapy and pharmacology, 76(5), 925–932.
15. Yoshino, T., Mizunuma, N., Yamazaki, K., Nishina, T., Komatsu, Y., Baba, H., … Ohtsu, A. (2012). TAS-102 monotherapy for pretreated metastatic colorectal cancer: a double-blind, randomised, placebo-controlled phase 2 trial. The Lancet Oncology, 13(10), 993–1001.
16. Mayer, R. J., Van Cutsem, E., Falcone, A., Yoshino, T., Garcia-Carbonero, R., Mizunuma, N., … Ohtsu, A. RECOURSE Study Group. (2015). Randomized trial of TAS-102 for refractory metastatic colorectal cancer. New England Journal of Medicine, 372(20), 1909–1919. doi: 10.1056/NEJMoa1414325.
17. Lopez, C. A., Azimi-Nekoo, E., Chung, S. Y., Newman, J., Shen, J., & Saif, W. M. (2020). Meta-analysis and systematic review of the cardiotoxicity of TAS-102. J. Clin. Oncol., 38, e16053(2020).
18. Henricks, L. M., Lunenburg, C. A., de Man, F. M., Meulendijks, D., Frederix, G. W., Kienhuis, E., … Schellens, J. H. (2018). DPYD genotype-guided dose individualisation of fluoropyrimidine therapy in patients with cancer: a prospective safety analysis. The Lancet Oncology, 19(11), 1459–1467. doi: 10.1016/S1470-2045(18)30686-7.
19. Knikman, J. E., Lopez‐Yurda, M., Meulendijks, D., Deenen, M. J., Schellens, J. H., Beijnen, J., … & Guchelaar, H. J. (2024). A nomogram to predict severe toxicity in DPYD wild‐type patients treated With capecitabine‐based anticancer regimens. Clinical Pharmacology & Therapeutics, 115(2), 269–277. doi: 10.1002/cpt.3100.
20. Cervantes, A., Adam, R., Roselló, S., Arnold, D., Normanno, N., Taïeb, J., … ESMO Guidelines Committee. (2023). Metastatic colorectal cancer: ESMO Clinical Practice Guideline for diagnosis, treatment and follow-up. Annals of Oncology, 34(1), 10–32.
21. Venook, A. P. (2025). Updates in Metastatic Colorectal Cancer. Journal of the National Comprehensive Cancer Network, 23(Supplement), e255017.
22. Schouten, J. F., Willems, J., Sanders, S. J., Creemers, G. J., & Deenen, M. J. (2021). Standard-dose trifluridine/tipiracil as safe treatment alternative in metastatic colorectal cancer patients with DPD deficiency. Clinical Colorectal Cancer, 20(4), 359–363. doi: 10.1016/j.clcc.2021.09.004.
23. ІНСТРУКЦІЯ для медичного застосування лікарського засобу 5-ФТОРУРАЦИЛ «ЕБЕВЕ» (5-FLUOROURACIL «EBEWE») (http://www.drlz.com.ua).
24. ІНСТРУКЦІЯ для медичного застосування лікарського засобу КСЕЛОДА® (XELODA®) (http://www.drlz.com.ua).
Адреса для листування:
Лялькін Сергій Анатолійович
03022, Київ, вул. Здановської Юлії, 33/43
Державне некомерційне підприємство «Національний інститут раку»
E-mail: slyalkin@yahoo.com
Correspondence:
Sergiі Lyalkin
33/43 Yulii Zdanovskoi str., Kyiv, 03022
Nonprofit Organization National Cancer Institute
E-mail: slyalkin@yahoo.com
На замовлення ТОВ «Серв’є Україна».
*Показання, протипоказання, спосіб застосування та дози, особливі групи пацієнтів, особливості застосування, побічні реакції та інше — повну інформацію див. в інструкції для медичного застосування лікарського засобу Лансурф® 15 мг/6,14 мг, Лансурф® 20 мг/8,19 мг. РП № UA/16712/01/01-02 від 10.02.2023 р. Зміни внесено наказом МОЗ України від 8.02.2024 р. № 214.
LSF-С1-2 (2025-2027, 2 years)-70














Leave a comment