Легенева онкологія: нова ера в терапії
Резюме. Науково-практичну конференцію «Легенева онкологія: нова ера в терапії», що відбулася 20 червня 2025 р. у м. Київ, присвячено новітнім підходам лікування раку легень на основі застосування таргетних препаратів. Підсумкове сесійне засідання заходу розпочав Ярослав Васильович Шпарик, завідувач відділення хімієтерапії Львівського онкологічного регіонального лікувально-діагностичного центру, кандидат медичних наук, програмною доповіддю «Новітні можливості терапії пацієнтів з метастатичним EGFRm НДКРЛ. У фокусі комбінація ТКІ + ПХТ», де освітлено перспективи та проблеми терапії раку легень за допомогою комбінації препарату осимертиніб з хімієтерапією (ХТ), що подовжує виживаність пацієнтів з EGFR-позитивним недрібноклітинним раком легень (НДКРЛ).
DOI: 10.32471/clinicaloncology.2663-466X.34768
Автор представив епідеміологічні дані щодо раку легень в Україні за 2022–2023 рр., зокрема наведено питому вагу основних 10 нозологічних форм злоякісних новоутворень у структурі захворюваності та смертності від онкопатології населення України, з окремими даними для чоловіків та жінок. Відмежовано дані для чоловіків віком 45–64 років та чоловіків усіх вікових груп щодо нозологічної структури загальних контингентів хворих на злоякісні новоутворення. Серед основних форм злоякісних пухлин саме рак легень (бронхів, трахеї) має значну питому вагу як у структурі захворюваності, так і смертності. Рак трахеї, бронхів, легень є найпоширенішим серед чоловіків як у структурі захворюваності (14,2%), так і смертності (21,1%) від злоякісних новоутворень в Україні у 2022–2023 рр. У чоловіків віком 45–64 років рак цієї нозології також лідирує у структурі захворюваності (15,6%), а у 2023 р. посідав одне з провідних місць серед чоловіків (6,4%) у загальній структурі злоякісних новоутворень.
 Надалі доповідач розглянув поширеність генетичних мутацій за окремими гістологічними підтипами НДКРЛ. Серед аденокарцином, які становлять 55% випадків НДКРЛ, найпоширенішими мутаціями є KRAS (23%), EGFR (19%), інші EGFR (2%), ALK (7%) та HER2 (2%). При плоскоклітинному раку (34% усіх випадків НДКРЛ) серед мутацій виділяються PIK3CA (34%), FGFR1 (17%), FGFR2 (3%), DDR2 (4%) та EGFR (5%). В якості додаткового біомаркера для НДКРЛ також важливим є визначення експресії PD-L1. Найбільш поширеними мутаціями EGFR (EGFRm) серед українських пацієнтів з НДКРЛ є Del 19ex (48,1%) та L858R (51,9%), і вони частіше трапляються у пацієнтів із середнім віком 59,2 року. Представлена автором інфографіка демонструє кількість направлень на тестування та частку EGFRm-позитивних зразків у різних вікових групах, причому найбільша кількість направлень фіксується у віковій групі 61–70 років.
Надалі доповідач розглянув поширеність генетичних мутацій за окремими гістологічними підтипами НДКРЛ. Серед аденокарцином, які становлять 55% випадків НДКРЛ, найпоширенішими мутаціями є KRAS (23%), EGFR (19%), інші EGFR (2%), ALK (7%) та HER2 (2%). При плоскоклітинному раку (34% усіх випадків НДКРЛ) серед мутацій виділяються PIK3CA (34%), FGFR1 (17%), FGFR2 (3%), DDR2 (4%) та EGFR (5%). В якості додаткового біомаркера для НДКРЛ також важливим є визначення експресії PD-L1. Найбільш поширеними мутаціями EGFR (EGFRm) серед українських пацієнтів з НДКРЛ є Del 19ex (48,1%) та L858R (51,9%), і вони частіше трапляються у пацієнтів із середнім віком 59,2 року. Представлена автором інфографіка демонструє кількість направлень на тестування та частку EGFRm-позитивних зразків у різних вікових групах, причому найбільша кількість направлень фіксується у віковій групі 61–70 років.
Які ж основні фактори, що впливають на прогноз у пацієнтів з EGFRm НДКРЛ та необхідність інтенсифікації терапії? Це наявність метастазів у центральній нервовій системі (ЦНС), мутація L858R у 21-му екзоні, а також високе пухлинне навантаження. Відомо, що ураження ЦНС знижує загальну виживаність (ЗВ) з 16,0 до 11,9 міс, а мутація L858R знижує виживаність без прогресування (ВБП) з 21,4 до 14,4 міс. У підсумку ці несприятливі фактори потребують посилення терапії для пацієнтів з EGFRm НДКРЛ.
Результати дослідження FLAURA та FLAURA2, надані автором, дозволяють оцінити ефективність та безпеку препарату осимертиніб у пацієнтів з поширеним НДКРЛ з EGFRm, зважаючи на відмінності у їхньому дизайні. Зокрема, дослідження FLAURA — це рандомізоване подвійне сліпе дослідження III фази, що порівнює застосування осимертинібу зі стандартною терапією інгібіторами тирозинкінази рецептора епідермального фактора росту (EGFR TKI) (гефітиніб або ерлотиніб), FLAURA2 — рандомізоване відкрите дослідження III фази, що порівнює осимертиніб поєднано з ХТ (платина + пеметрексед) з монотерапією осимертинібом. Первинні кінцеві точки для FLAURA — ВБП, для FLAURA2 — ВБП та ВБП у пацієнтів з метастазами в ЦНС. Вторинні кінцеві точки для обох досліджень включають ЗВ, частоту об’єктивної відповіді та тривалість відповіді. Дослідження FLAURA2 охоплювало пацієнтів з більш несприятливим прогнозом, про що свідчать наступні відмінності порівняно з FLAURA: метастази в головний мозок у FLAURA2 визначалися на етапі залучення у всіх хворих, тоді як у FLAURA — не у всіх. У FLAURA2 40–42% пацієнтів мали метастази в головний мозок, тоді як у FLAURA — 19–23%. Пацієнти FLAURA2 характеризувалися вищим пухлинним навантаженням (середній розмір пухлини становив 64–65 мм) порівняно з FLAURA (55–57 мм). У FLAURA2 53–54% пацієнтів мали екстраторакальні метастази, тоді як у FLAURA — 34–37% осіб.
Відомо, що комбінація EGFR TKI з ХТ (поліхімієтерапією (ПХТ)) працює ефективніше, оскільки вона долає резистентність пухлинних клітин до EGFR TKI та забезпечує повнішу елімінацію пухлини. У деяких пацієнтів пухлинні клітини можуть розвивати резистентність до лікування EGFR TKI, що призводить до прогресування хвороби, тоді як ХТ, додана до EGFR TKI, дозволяє знищити ті з них, які стали стійкими до EGFR TKI. Комплексний вплив такої терапії полягає в тому, що EGFR TKI впливають на одну популяцію пухлинних клітин, тоді як ХТ впливає на резистентні клони, що дозволяє досягти стійкої відповіді та елімінації персистивних пухлинних клітин (рис. 1). Така комбінація покращує загальні клінічні результати лікування, які відмічаються при застосуванні лише EGFR TKI. Тож комбінація осимертинібу з ХТ діє синергічно, затримуючи розвиток резистентності та підвищуючи рівень відповіді порівняно з монотерапією осимертинібом. Окрім того, не всі пацієнти, що приймали осимертиніб, можуть отримати ХТ після прогресування патології, тому її комбінація з осимертинібом у 1-й лінії забезпечує більш ефективне лікування.
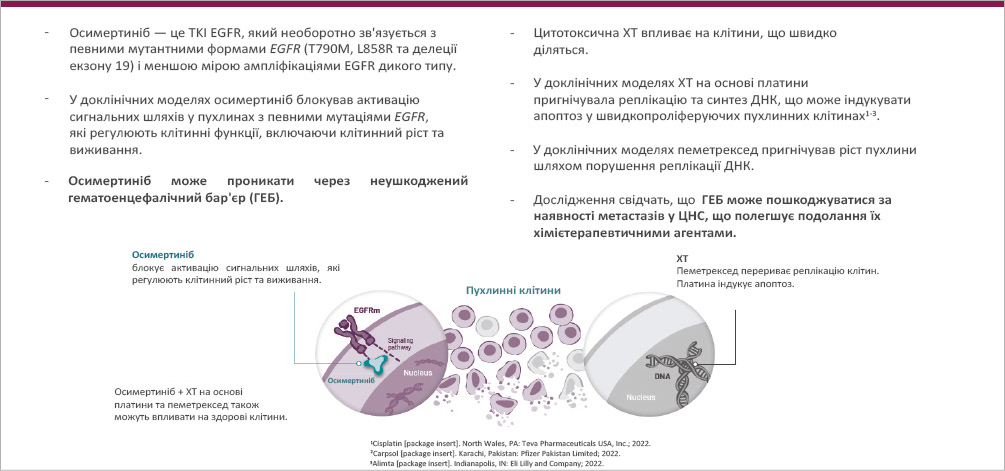
Рис. 1. Застосування осимертинібу в комплексі з хімієтерапією. Довідкова інформація
 Результати досліджень FLAURA та FLAURA2, як зазначив доповідач, свідчать про переваги осимертинібу в лікуванні НДКРЛ у пацієнтів з високим ризиком та несприятливим прогнозом. Так, у дослідженні FLAURA виявлено ранню та стійку перевагу осимертинібу у ВБП зі зниженням ризику прогресування або смерті на 54% порівняно з іншими інгібіторами тирозинкінази першого покоління. У дослідженні FLAURA2 встановлено, що комбінація осимертинібу з ХТ збільшила перевагу у ВБП, знизивши ризик прогресування або смерті на 38% порівняно з монотерапією осимертинібом. Медіана ВБП у дослідженні FLAURA2 для комбінованої терапії осимертинібом з ХТ становила 29,4 міс, тоді як для монотерапії осимертинібом у дослідженні FLAURA вона становила 18,9 міс. Так, FLAURA2 підтверджує ефективність комбінованої терапії осимертинібом + ХТ як першої лінії лікування для пацієнтів з EGFRm (Ex19del / L858R) НДКРЛ. Зокрема, ВБП при комбінованій терапії становить 29,4 міс, що на 9,5 міс більше порівняно з монотерапією осимертинібом (19,9 міс). Середня ВБП, за даними дослідника, у пацієнтів з мутацією L858R при комбінованій терапії становила 24,7 міс, що на 10,8 міс більше, ніж при монотерапії осимертинібом (13,9 міс). Тож пацієнти з високим ризиком / несприятливим прогнозом та EGFRm НДКРЛ можуть отримати значну користь від інтенсивнішої терапії.
Результати досліджень FLAURA та FLAURA2, як зазначив доповідач, свідчать про переваги осимертинібу в лікуванні НДКРЛ у пацієнтів з високим ризиком та несприятливим прогнозом. Так, у дослідженні FLAURA виявлено ранню та стійку перевагу осимертинібу у ВБП зі зниженням ризику прогресування або смерті на 54% порівняно з іншими інгібіторами тирозинкінази першого покоління. У дослідженні FLAURA2 встановлено, що комбінація осимертинібу з ХТ збільшила перевагу у ВБП, знизивши ризик прогресування або смерті на 38% порівняно з монотерапією осимертинібом. Медіана ВБП у дослідженні FLAURA2 для комбінованої терапії осимертинібом з ХТ становила 29,4 міс, тоді як для монотерапії осимертинібом у дослідженні FLAURA вона становила 18,9 міс. Так, FLAURA2 підтверджує ефективність комбінованої терапії осимертинібом + ХТ як першої лінії лікування для пацієнтів з EGFRm (Ex19del / L858R) НДКРЛ. Зокрема, ВБП при комбінованій терапії становить 29,4 міс, що на 9,5 міс більше порівняно з монотерапією осимертинібом (19,9 міс). Середня ВБП, за даними дослідника, у пацієнтів з мутацією L858R при комбінованій терапії становила 24,7 міс, що на 10,8 міс більше, ніж при монотерапії осимертинібом (13,9 міс). Тож пацієнти з високим ризиком / несприятливим прогнозом та EGFRm НДКРЛ можуть отримати значну користь від інтенсивнішої терапії.
У підсумку осимертиніб є ефективним проти багатьох викликів, що підтверджується даними дослідження FLAURA2. Дослідження FLAURA2 фіксує перевагу осимертинібу щодо ВБП у пацієнтів з мутаціями Ex19del та L858R. Застосування осимертинібу в комбінації з платиною / пеметрекседом значно подовжує медіану виживаності без прогресування (МВБП) порівняно з монотерапією осимертинібом на 8,5 міс для пацієнтів з Ex19del та на 10,8 міс для хворих з L858R.
Додатково для пацієнтів без відомих метастазів у ЦНС на початку лікування комбінована терапія осимертиніб + платина / пеметрексед подовжує ВБП на 6,6 міс порівняно з монотерапією осимертинібом. Для осіб з відомими метастазами в ЦНС на початку лікування комбінована терапія осимертиніб + платина / пеметрексед подовжує ВБП на 11,1 міс порівняно з монотерапією осимертинібом.
Так, у дослідженні FLAURA2 встановлено значну перевагу комбінованої терапії осимертинібом з платиною / пеметрекседом у подовженні ВБП у пацієнтів як з метастазами в ЦНС, так і без них. Відповідь метастазів у ЦНС при застосуванні осимертинібу порівняно з гефітинібом / ерлотинібом зафіксована з частотою 41% для осимертинібу та більш низькою — для іншого лікування, тоді як при застосуванні осимертинібу в комбінації з платиною та пеметрекседом частота відповіді становила 59%. Частота випадків прогресування при ураженні ЦНС була нижчою в групі комбінованої терапії (осимертиніб + препарат платини та пеметрексед) порівняно з монотерапією осимертинібом, а розрахункова ймовірність прогресування метастазів у ЦНС через 24 міс становила 9% для комбінованої терапії та 23% — для монотерапії осимертинібом.
Автор окремо наголосив на даних щодо зниження ризику смерті, зокрема осимертиніб зумовив зниження ризику смерті на 20% порівняно з іншим лікуванням з медіаною виживаності 38,6 проти 31,8 міс. У дослідженні FLAURA2 представлено другий проміжний аналіз, в якому комбінована терапія (осимертиніб + ХТ) проявила перевагу в ЗВ.
Які наступні опції лікування отримували пацієнти в групі осимертиніб + ПХТ після прогресування? Згідно з наданою інфографікою, після прогресування під час ініціальної терапії в групі осимертиніб + ПХТ (осимертиніб + ХТ) пацієнти отримували такі наступні опції лікування: терапія 2-ї лінії (ХТ — 35% пацієнтів, схеми лікування, що містять інші ТКІ EGFR, — 20% хворих). Отримали 3-тю лінію терапії — 20%, не отримували наступного лікування — 17%, продовжують лікування в дослідженні — 3% пацієнтів. Загалом у групі осимертиніб + ХТ — 46% осіб (57 зі 123), а в групі осимертиніб — 60% (91 зі 151) пацієнтів розпочали 2-гу лінію терапії після прогресування під час ініціальної терапії.
Доповідач пропонує аудиторії розглянути дилему — як зробити вибір між двома стратегіями лікування? Монотерапія препаратом осимертиніб має перевагу у вигляді нижчої токсичності. Комбінована терапія осимертиніб + ХТ потенційно забезпечує сильніший контроль над захворюванням та потребує оцінки ризиків. Тож вибір оптимальної стратегії лікування для пацієнтів з НДКРЛ, що мають EGFRm, полягає в урахуванні балансу між ефективністю та токсичністю терапії. Необхідно зважати, що комбінована терапія осимертиніб + ХТ забезпечує ефективніший контроль хвороби, особливо у пацієнтів з високим ризиком та метастазами в ЦНС, значно підвищує ВБП хвороби у пацієнтів з поширеним EGFRm-позитивним НДКРЛ. Також комбінована терапія має більш низький ризик прогресування захворювання в ЦНС порівняно з монотерапією осимертинібом, а профіль переносимості комбінації осимертиніб + ХТ є відомим та контрольованим.
Насамкінець, в якості підсумку, автор представив найвагоміші результати клінічних досліджень різних режимів лікування НДКРЛ з EGFRm осимертинібом:
- FLAURA2 фіксує найдовшу ВБП — 29,4 міс — при застосуванні комбінованої терапії в першій лінії метастатичного процесу.
- У FLAURA встановлено ВБП на рівні 18,9 міс при монотерапії у 1-й лінії метастатичного процесу.
- AURA3 свідчить про ВБП на рівні 10,1 міс при монотерапії у 2-й лінії метастатичного процесу.
- У ADAURA виявлено вражаючу виживаність без ознак захворювання (ВБОЗ) — 65,8 міс — на резектабельних стадіях.
 Наступна доповідь — Ольги Володимирівни Кузнецової, доцентки кафедри хірургії, променевої діагностики, терапії, радіаційної медицини та онкології Одеського національного медичного університету (ОНМедУ), на тему «Практичні аспекти застосування таргетної терапії у пацієнтів з метастатичним EGFRm НДКРЛ» присвячена розгляду клінічного випадку пацієнтки Б. з діагнозом аденокарциноми легень. 6 квітня 2021 р. пацієнтці виконано відеоторакоскопію, клиновидну резекцію нижньої долі лівої легені та біопсію парієтальної плеври. Діагноз за патогістологічним висновком (ПГВ): підтверджено G2 аденокарциному з емболами в судинах пухлини. Імуногістохімічне дослідження (ІГД) виявило аденокарциному легень ацинарної та мікропапілярної будови, з позитивними EGFR та PD-L1, мікросателітно-стабільну, ALK-негативну.
Наступна доповідь — Ольги Володимирівни Кузнецової, доцентки кафедри хірургії, променевої діагностики, терапії, радіаційної медицини та онкології Одеського національного медичного університету (ОНМедУ), на тему «Практичні аспекти застосування таргетної терапії у пацієнтів з метастатичним EGFRm НДКРЛ» присвячена розгляду клінічного випадку пацієнтки Б. з діагнозом аденокарциноми легень. 6 квітня 2021 р. пацієнтці виконано відеоторакоскопію, клиновидну резекцію нижньої долі лівої легені та біопсію парієтальної плеври. Діагноз за патогістологічним висновком (ПГВ): підтверджено G2 аденокарциному з емболами в судинах пухлини. Імуногістохімічне дослідження (ІГД) виявило аденокарциному легень ацинарної та мікропапілярної будови, з позитивними EGFR та PD-L1, мікросателітно-стабільну, ALK-негативну.
Авторка представила схему лікувальної тактики при НДКРЛ, яка залежить від визначення активувальних мутацій та експресії PD-L1, та підкреслила її ключові моменти, а саме:
- Перед початком лікування необхідно отримати результати молекулярно-генетичного тестування (МГТ). Схема включає визначення гістологічного підтипу пухлини (аденокарцинома, плоскоклітинний рак) та виявлення мутацій (EGFR, ALK, ROS1, BRAF, NTRK).
- Залежно від статусу мутації призначається відповідне лікування (наприклад осимертиніб при EGFR+, алектиніб при ALK+). У випадку відсутності активуючих мутацій лікування визначається на основі експресії PD-L1.
Описаний клінічний випадок пацієнтки з аденокарциномою лівої легені представлений доповідачкою в якості прикладу персоналізованого підходу лікування.
Пацієнту встановлено діагноз: аденокарцинома лівої легені IV стадії з метастазами в ребра та хребет, EGFR+ та PD-L1-позитивна. Проведено паліативне хірургічне лікування, променева терапія на метастази в кістки, рекомендована ХТ за протоколом паклітаксел / карбоплатин та таргетна терапія осимертинібом у дозі 80 мг/д. Пацієнтка відмовилася від імунотерапії через фінансові причини.
Відомо, що мутації EGFR є негативним прогностичним фактором у пацієнтів з І–ІІІ стадіями НДКРЛ типу солідної аденокарциноми, оскільки вони підвищують ризик рецидиву або смерті на 33% порівняно з пацієнтами без EGFRm (дикий тип), а крива ВБОЗ для пацієнтів з EGFRm значно нижча, ніж для осіб з диким типом. Наведені дані отримані на основі дослідження 933 пацієнтів з НДКРЛ після радикальної резекції пухлини. Підвищення ризику рецидиву у хворих з EGFRm після радикальної резекції НДКРЛ є значним (відносний ризик (ВР) = 1,33; p=0,006). Застосування осимертинібу значно подовжує ВБП: половина пацієнтів у групі осимертинібу залишалися живими без прогресування протягом 18,9 міс, тоді як у групі ерлотинібу / гефітинібу цей показник становив 10,2 міс. Прийом осимертинібу знижує ризик рецидиву або смерті на 54% порівняно з препаратами 1-го покоління. Ці дані свідчать про перевагу осимертинібу як препарату першої лінії для лікування поширеного НДКРЛ з EGFRm.
Результати дослідження FLAURA щодо ЗВ пацієнтів з поширеним НДКРЛ у неазійській (європейській) популяції свідчать, що осимертиніб значно подовжує медіану ЗВ на 19 міс порівняно з TKI EGFR 1-го покоління (43,3 проти 24,3 міс) та знижує відносний ризик смерті на 46%, що вказує на значну перевагу осимертинібу як препарату першої лінії терапії у пацієнтів з поширеним НДКРЛ з EGFRm.
Надалі авторкою представлені результати комп’ютерної томографії (КТ) грудної клітки. Описаний стан пацієнтки після торакоскопії, клиновидної резекції нижньої частки лівої легені та біопсії парієтальної плеври. Зазначено, що органи середостіння зміщені вліво і свіжі інфільтративні зміни відсутні.
Спираючись на Рекомендації Національної мережі багатопрофільних онкологічних закладів США (National Comprehensive Cancer Network — NCCN) 1L, які відображають алгоритм лікування НДКРЛ з EGFRm з делецією в 19-му екзоні або L858R у 21-му екзоні, доповідачка підкреслила, що переважним варіантом першої лінії терапії є застосування осимертинібу. Якщо EGFRm виявлена під час І лінії системної терапії, можливе додавання осимертинібу до пеметрекседу + (цисплатину або карбоплатину) (неплоскоклітинний НДКРЛ) або переривання поточної терапії та початок прийому осимертинібу або амівантамабу-vmjw / лазертинібу.
У розглянутому клінічному випадку EGFRm виявлені під час системної терапії. КТ-знімки легень у різних проєкціях (аксіальні та сагітальні зрізи) візуалізують патологічні зміни. При диспансерному динамічному спостереженні результати КТ-досліджень виявляють відсутність ознак первинної пухлини легень та прогресування захворювання в кістках скелета. Прийом бісфосфонатів припинено через токсичність. Стабілізація процесу стала результатом лікування протягом 4 років (з травня 2021 р.) за допомогою осимертинібу (80 мг/добу). Наразі стан пацієнтки задовільний, зберігається належна якість життя та фізична активність, вона працює вчителькою в Німеччині, підтримує онлайн-зв’язок з українським клінічним онкологом.
 Завідувач комунального некомерційного підприємства «Подільський регіональний центр онкології Вінницької обласної Ради», м. Вінниця, Сергій Миколайович Притуляк представив доповідь на тему «Складні випадки при поширеному НДКРЛ. Комбінована терапія. Хірургія ускладнень».
Завідувач комунального некомерційного підприємства «Подільський регіональний центр онкології Вінницької обласної Ради», м. Вінниця, Сергій Миколайович Притуляк представив доповідь на тему «Складні випадки при поширеному НДКРЛ. Комбінована терапія. Хірургія ускладнень».
На початку доповіді автор наголосив на епідеміологічних даних щодо раку легень в Україні за 2022–2023 рр., які свідчать, що на обліку в онкодиспансерах перебувало 36 547 пацієнтів з раком легень (26 295 чоловіків, 10 252 жінки), а кількість нових випадків у 2022 р. зменшилася на 14,8% порівняно з 2021 р. і становить 9164 нових випадки. Причому розподіл за стадіями серед виявлених випадків становив: I стадія — 15,5%, II стадія — 30,3%, IV стадія — 43,8%. Тож не дивно, що 53,3% хворих, уперше отримавши діагноз у 2022 р., не пережили і року.
Наразі існує низка незадоволених медичних потреб у лікуванні раку легень, зокрема у пацієнтів з EGFRm-позитивним НДКРЛ. Насамперед, попри переваги ХТ, фіксується прогресування хвороби через гетерогенність пухлини або розвиток набутої резистентності до лікування. Також часто виявляють метастази в ЦНС, що знижує виживаність та якість життя пацієнтів, тому вкрай важливою є ефективність лікування та запобігання подальшому прогресуванню пухлини. Відомо, що монотерапія ТКІ EGFR при мутації L858R асоційована з гіршим прогнозом порівняно з мутацією ex19del, що вказує на важливість нових варіантів лікування для пацієнтів з EGFRm-позитивним НДКРЛ, особливо з несприятливим прогнозом.
Клінічний випадок, наведений доповідачем, є прикладом застосування нових підходів у розв’язанні таких проблем. Клінічні дані пацієнта свідчать про:
- Діагноз: рак середньочасткового бронха правої легені, IV стадія, з метастазами в нижню частку правої легені.
- Гістологія: недрібноклітинна карцинома легень, імунофенотип та морфологія відповідають аденокарциномі.
- Результати обстежень: бронхоскопія підтверджує рак у центральній зоні, а КТ виявляє ознаки пухлини з інвазією в плевру, вторинні вузлики та ураження лімфовузлів середостіння, а також гепатомегалію.
- Симптоми: кровохаркання.
Представлені автором дані Настанови NCCN (версія 7.2024) вказують на сучасні можливості лікування НДКРЛ, зокрема у пацієнтів з мутаціями або делеціями в генах EGFR. Наведено схему, що деталізує терапію першої лінії для хворих з делецією в 19-му екзоні або мутацією 21-го екзону гена EGFR. Рекомендовані варіанти терапії включають осимертиніб як переважний варіант, а також інші варіанти, такі як ерлотиніб, афатиніб, гефітиніб, дакомітиніб, рамуцирумаб та бевацизумаб. У разі прогресування захворювання після першої лінії терапії рекомендована подальша системна терапія з можливими варіантами, що включають ХТ або інші цільові препарати. Окремо визначені варіанти з підтримуючою терапією, перервами або заміною схеми лікування.
Тож, відповідно до рекомендацій NCCN, пацієнту призначено паліативну ПХТ за схемою пеметрексед + карбоплатин, проведено 1 курс лікування, після чого виявлено EGFRm (19-й екзон) за результатами молекулярного тестування. Додано препарат осимертиніб (80 мг) щоденно до основної схеми лікування і проведено ще 4 курси терапії в комбінованому режимі, оскільки осимертиніб у комбінації з ХТ може діяти синергічно, уповільнюючи розвиток резистентності.
Автор представив результати лікування, які включають регрес основного вогнища на 42%, повний регрес метастатичного вогнища в нижній частці легені, нормалізацію лімфовузлів середостіння.
Відоме дослідження FLAURA2 — це відкрите рандомізоване дослідження III фази, яке оцінює застосування осимертинібу з ХТ (препаратами платини та пеметрекседом) або без неї як терапії першої лінії при НДКРЛ. У межах дослідження пацієнти з місцево-поширеним або метастатичним НДКРЛ з EGFRm (Ex19del, L858R), які не отримували попередньої системної терапії, пройшли лікування комбінацією осимертиніб з ХТ (препарат платини та пеметрексед), що значно поліпшило відповідь пухлини. Зокрема, частота загальної відповіді для комбінованої терапії становила 83% (95% довірчий інтервал (ДІ) 78–87), тоді як для монотерапії осимертинібом — 76% (95% ДІ 70–80). Медіана тривалості відповіді (95% ДІ) для комбінованої терапії становила 24,0 міс (20,5–27,8), а для монотерапії — 15,3 міс (12,7–18,4).
Комбінація осимертинібу з ХТ (препарати платини та пеметрексед) значно подовжила ВБП у пацієнтів з НДКРЛ та EGFRm порівняно з монотерапією осимертинібом. Середня ВБП для комбінованої терапії становила 29,4 міс, тоді як для монотерапії осимертинібом — 19,9 міс. Через 24 міс показники ВБП були вищими у групі, яка отримувала комбіновану терапію. У підсумку комбінація осимертинібу з ПХТ (препарати платини та пеметрексед) значно подовжила ВБП у хворих з EGFRm раком легень незалежно від типу мутації (Ex19del або L858R) порівняно з монотерапією осимертинібом. Так, дослідження підтверджує ефективність комбінованої терапії осимертинібом та ПХТ як нової опції лікування для пацієнтів з EGFRm раком легень.
Результати аналізу 4-річної ЗВ також свідчать на користь комбінованого лікування осимертинібом з платиною та пеметрекседом (ПХТ) порівняно з монотерапією осимертинібом. Так, медіана ЗВ у групі комбінованого лікування була вищою (47,5 міс) порівняно з монотерапією (37,6 міс) (рис. 2).
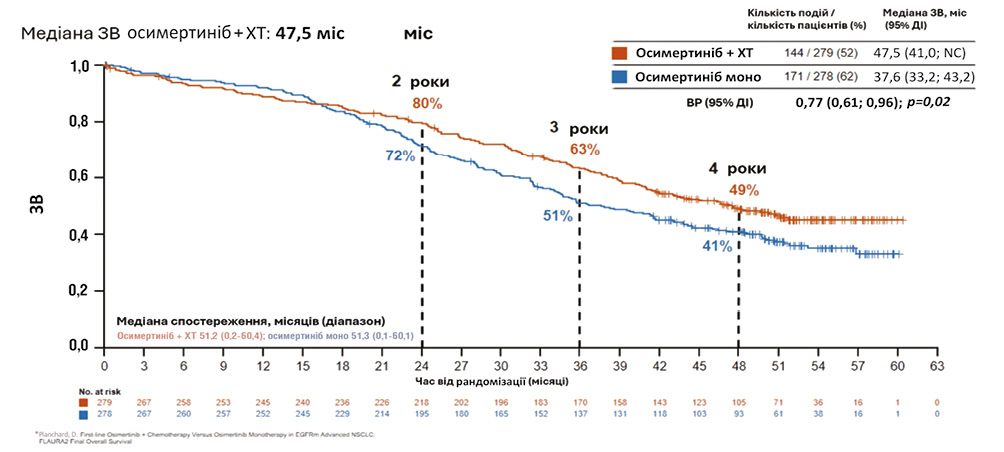
Рис. 2. FLAURA2. Дані ЗВ*
Примітка: NC (Not Calculable) — не обчислюється. Це часто трапляється, коли більше ніж половина пацієнтів ще живі на момент кінцевого спостереження.
Важливим аспектом терапії є профіль безпеки та переносимість лікування, зокрема комбінації осимертинібу, препарату платини та пеметрекседу. Встановлено, що частота та тяжкість побічних реакцій були найвищими під час індукційної терапії і поступово знижувалися з часом. Значне зменшення кількості побічних явищ ≥III ступеня відмічалося у групі осимертинібу, препарату платини та пеметрекседу: на 50% у 49% пацієнтів (n=135) протягом 0–3 міс і на 24% у 62 хворих (n=62) впродовж 3–9 міс. Медіана тривалості ХТ платиною становила 2,8 міс, пеметрекседом — 8,3 міс, а осимертинібом — 22,3 міс, більшість пацієнтів завершили щонайменше 4 цикли ХТ платиною (76% з 211 осіб).
Повертаючись до наведеного раніше клінічного випадку, доповідач зазначив, що після позитивної динаміки попереднього лікування та збільшення кількості випадків кровохаркання, вирішено провести хворому VATS-середню лобектомію для усунення джерела легеневої кровотечі. Передопераційний діагноз пацієнта — центральний рак середньочасткового бронха правої легені IV стадії з метастазами. Оперативне лікування виконано 9.09.2024 р. у вигляді VATS-середньої лобектомії з лімфодисекцією, післяопераційний період пройшов без ускладнень. Імуногістохімічне дослідження після операції підтвердило повний патоморфоз пухлини та лімфатичних вузлів. Автор підкреслив, що хірургічне лікування кровохаркання може проводитися двома основними методами:
- Відкрита торакотомія: традиційна техніка резекції легень з великим розрізом та розсуванням ребер. Це найпоширеніший доступ, що передбачає перебування в стаціонарі від 5 до 7 днів, а тривалість операції становить 2–6 год.
- VATS (відеоасистована торакоскопічна хірургія) — це мінімально інвазивна методика, яка використовує кілька невеликих розрізів для введення інструментів та камери. Вона забезпечує швидше відновлення, менш виражений біль, нижчий рівень ускладнень та післяопераційної смертності, а час перебування в стаціонарі скорочується на 2 дні порівняно з торакотомією. Тривалість операції VATS становить 2–3 год.
У післяопераційний період пацієнт отримав 4 курси ПХТ, що включали пеметрексед та карбоплатин у комбінації з осимертинібом.
Тримісячний період після операції є важливим для контролю процесу загоєння та виявлення будь-яких відхилень. Дослідження із використанням спіральної комп’ютерної томографії органів грудної клітки (СКТ ОГК), проведеної через 3 міс після оперативного втручання, підтвердило позитивний результат. Зазначено, що СКТ ОГК є високоінформативним методом візуалізації, який дозволяє отримати детальні зображення легень, серця, судин, дихальних шляхів, ребер та лімфатичних вузлів грудної клітини. Дослідження виконується для оцінки стану ОГК після хірургічного втручання, виявлення можливих ускладнень або оцінки динаміки змін.
Наразі пацієнт продовжує монорежимну терапію осимертинібом у дозі 80 мг/добу, загальна тривалість лікування становить 14 міс.
 Тему наступної доповіді присвячено застосуванню комбінації ТКІ + ПХТ у пацієнтів з НДКРЛ з EGFRm. Доповідь представив Владислав Андрійович Ганул, торакальний хірург, клінічний онколог Державного некомерційного підприємства «Національний інститут раку», м. Київ.
Тему наступної доповіді присвячено застосуванню комбінації ТКІ + ПХТ у пацієнтів з НДКРЛ з EGFRm. Доповідь представив Владислав Андрійович Ганул, торакальний хірург, клінічний онколог Державного некомерційного підприємства «Національний інститут раку», м. Київ.
Автором розглянуто переваги новітніх підходів у лікуванні НДКРЛ на прикладі клінічних випадків.
Клінічний випадок № 1: пацієнтка, 71 рік. Діагноз: рак верхньої частки правої легені, стадія IVB з метастазами в головний мозок, шийні лімфовузли та легені. Гістологія: аденокарцинома G2, позитивна за EGFR (19-й екзон), негативна за ALK та KRAS, PDL-1 — 5%.
Керуючись рекомендаціями Настанови NCCN, версія 4.2025, щодо вибору тактики лікування НДКРЛ (Non-Small Cell Lung Cancer) за наявності EGFRm у вигляді делеції 19-го екзону або EGFRm 21-го екзону L858R, мультидисциплінарна комісія (МДК) визначила тактику лікування, яка включала осимертиніб у монорежимі як початкову терапію. Тривалість лікування осимертинібом становила 9 міс, у результаті зафіксовано повний регрес метастазів у головний мозок та частковий регрес основної пухлини та метастазів у легені. Зрізи КТ, продемонстровані автором, свідчать про частковий регрес пухлини, тобто про позитивну динаміку лікування та зменшення розмірів або поширення пухлини.
На жаль, через 9 міс після початку терапії відмічається прогресування хвороби. Виявлено збільшення основного новоутворення та метастатичні вогнища в легенях. При цьому прогресування пухлини в головному мозку не зафіксовано.
Відомо, що перебіг НДКРЛ з EGFRm в контексті поліклональності пухлини характеризується зменшенням обсягу чутливих клонів новоутворення, виявляється часткова відповідь. Після закінчення застосування TKI EGFR збільшується обсяг резистентних клонів, що призводить до загострення хвороби та прогресування захворювання, незважаючи на можливий ретритмент TKI EGFR. Причина прогресування полягає в гетерогенності пухлини, що викликає відсутність відповіді на лікування або розвиток набутої резистентності.
Як наведено раніше, у дослідженні FLAURA2, представленому на Всесвітній конференції з раку легень 2024 р. (World Conference on Lung Cancer), виявлено, що осимертиніб у комбінації з ХТ підвищує ВБП у пацієнтів з EGFRm поширеним НДКРЛ. Переваги комбінованої терапії були особливо вираженими у пацієнтів з високим пухлинним навантаженням (ураження ≥3 метастатичних анатомічних ділянок). Отже, комбінована терапія значно підвищує ВБП у хворих з великою кількістю метастазів. Для пацієнтів з ≥3 метастатичними ділянками медіана ВБП становила 24,5 міс для комбінованої терапії проти 13,6 міс для монотерапії. При цьому у пацієнтів з <3 метастатичними ділянками значної різниці у ВБП між групами не зафіксовано.
Спираючись на клінічні дослідження FLAURA / FLAURA2, автор розглядає в якості терапії після осимертинібу моноплатиновмісну ХТ, моноХТ, імунотерапію (наприклад атезолізумаб у комбінації) та таргетну терапію (наприклад комбінація інгібіторів BRAF / MEK або ALK TKI).
Рішенням МДК пацієнту додано ХТ за схемою карбоплатин + пеметрексед через відсутність клінічно значущого прогресування. Після 3 циклів ХТ відмічається майже повний регрес усіх вогнищ у легенях, нових вогнищ не виявлено.
Клінічний випадок № 2 описує лікування пацієнта віком 63 років з діагнозом центрального раку правої легені IV стадії (T3N2M1). Виявлено метастази у праву легеню, лімфатичні вузли середостіння, плевру та головний мозок. Молекулярне дослідження (NGS) свідчить про аденокарциному легень з мутацією 57681 20-го екзону гена EGFR. Мутацій у генах ALK та KRAS не виявлено, PD-L1 — 1%.
Надалі доповідач зупинився на виборі тактики лікування НДКРЛ, зокрема порівнянні препаратів афатиніб та осимертиніб відповідно до рекомендацій Настанови NCCN, версія 4.2025. Зазначено, що вибір терапії залежить від часу виявлення EGFRm: до системної терапії першої лінії або під час неї. Відомо, що лише у близько 0,59% пацієнтів з НДКРЛ трапляється мутація EGFR S768I. Вибір між осимертинібом та афатинібом залежить від індивідуальних клінічних характеристик хворого, зокрема наявності метастазів у головний мозок. Обидва препарати можуть бути ефективними для лікування мутацій S768I, але осимертиніб може мати перевагу в контексті загальної переносимості та ефективності при метастазах у головний мозок.
В актуальних дослідженнях вивчаються відмінності в клінічних результатах між осимертинібом та афатинібом як першої лінії лікування, а також механізми резистентності до препаратів TKI EGFR 3-го покоління. Обґрунтування доцільності застосування осимертинібу в комбінації з ХТ, за висновками автора, полягає в наступному:
- Осимертиніб є інгібітором тирозинкінази EGFR, що необоротно зв’язується з мутантними формами EGFR і блокує сигнальні шляхи, які регулюють клітинний ріст та виживання пухлинних клітин.
- Осимертиніб здатний проникати через непошкоджений гематоенцефалічний бар’єр (ГЕБ), що є важливою перевагою при метастазах у ЦНС.
- Цитотоксична ХТ впливає на клітини, які швидко діляться, пригнічуючи реплікацію та синтез ДНК (наприклад ХТ на основі платини або пеметрексед), що індукує апоптоз у пухлинних клітинах.
- Комбінація дозволяє досягти синергічного ефекту, оскільки ГЕБ може пошкоджуватися при метастазах у ЦНС, полегшуючи подолання його хімієтерапевтичними агентами.
МДК визначила тактику лікування пацієнта, яка включала послідовну хімієпроменеву терапію (лікування розпочато з променевої терапії на головний мозок). Призначено 6 курсів карбоплатину та пеметрекседу, а також осимертиніб. Наразі пацієнт уже отримав 6 курсів ХТ (карбоплатин + пеметрексед) і продовжує приймати осимертиніб у дозуванні 80 мг/добу в монорежимі.
 Цікавий клінічний випадок у контексті сучасної таргетної терапії розглянула у своїй доповіді Ольга Василівна Герасименко, керівниця Центру онкології Клінічної лікарні «Феофанія» Державного управління справами, клінічна онкологиня.
Цікавий клінічний випадок у контексті сучасної таргетної терапії розглянула у своїй доповіді Ольга Василівна Герасименко, керівниця Центру онкології Клінічної лікарні «Феофанія» Державного управління справами, клінічна онкологиня.
Пацієнтка з діагнозом немуцинозної аденокарциноми верхньої частки лівої легені з EGFRm 19del(+), менінгіома лівої лобної частки. Проведено відеоасистовану медіастинальну лімфаденектомію, а також ХТ (цисплатин, пеметрексед, осимертиніб) з досягненням повної метаболічної відповіді.
За допомогою МРТ головного мозку виявлено менінгіому лівої лобної частки та прояви мікроангіопатії без ознак гострого вогнищевого чи вторинного ураження головного мозку. Проведено відеоасистовану медіастинальну лімфаденектомію, у лімфовузлах виявлено ріст карциноми, що, враховуючи клінічні дані та морфологічну картину, ймовірно, є немуцинозним варіантом аденокарциноми легень. Проведене імуногістохімічне дослідження для уточнення первинного гістогенезу, завдяки якому встановлено позитивну реакцію на цитокератин 7, TTF-1 та напсин А, тоді як цитокератин 20 зумовив негативну реакцію в клітинах пухлини, тобто імунологічний профіль пухлини відповідає карциномі з первинною локалізацією в легенях. Патологогістологічний діагноз: немуцинозна аденокарцинома легень з ураженням лімфатичних вузлів групи № 7, 4R, 2R, 4L.
Рішенням МДК хворій призначено проведення ехокардіографії (Ехо-КГ), 4 курсів ПХТ за схемою цисплатин + пеметрексед / паклітаксел + карбоплатин та рекомендовано КТ ОГК, органів черевної порожнини (ОЧП), органів малого таза (ОМТ) з внутрішньовенним контрастуванням або позитронно-емісійну комп’ютерну томографію (ПЕТ-КТ), а також визначення молекулярного статусу пухлини (NGS lung) з виявленням EGFRm 19del(+), негативним ALK та позитивним PD-L1 після 4 курсів ПХТ.
Авторка розглянула концепцію комбінованої терапії в лікуванні раку, зокрема, коли виникає резистентність до окремих видів лікування. Відомо, що осимертиніб — ТКІ, що впливає на EGFRm-клітини, зумовлює зменшення пухлини. Резистентні до ТКІ клони починають рости, незважаючи на лікування осимертинібом, що призводить до пухлинного росту. Тому існує потреба в комбінованій терапії, коли додається ХТ, щоб подолати резистентність і зменшити пухлину.
Доповідачка також звернулася до результатів клінічного дослідження FLAURA2, яке вивчає ефективність та переносимість комбінації осимертинібу з платиною та пеметрекседом порівняно з монотерапією осимертинібом у пацієнтів з поширеним EGFRm НДКРЛ. Вона зупинилася на основних моментах дизайну дослідження та розглянула найвагоміші результати. Підкреслено, що комбінація осимертинібу з ПХТ зумовлює вищий рівень загальної відповіді (83 з 95% ДІ 78–87%) порівняно з монотерапією осимертинібом (76 з 95% ДІ 70–80%). Медіана тривалості відповіді значно довша при комбінованій терапії осимертинібом з ПХТ (24 міс з 95% ДІ 20,9–27,8), ніж при монотерапії осимертинібом (15,3 міс з 95% ДІ 12,7–19,4). Так, комбінована терапія осимертинібом з ПХТ зумовлює кращі показники як за рівнем загальної відповіді, так і за медіаною тривалості відповіді порівняно з монотерапією осимертинібом. Комбінація осимертиніб + ХТ значно збільшує перевагу у ВБП, додаючи 9,5 міс порівняно з монотерапією осимертинібом. Також встановлено, що у осіб з метастазами в ЦНС медіана ВБП для осимертинібу + ПХТ становить 24,9 міс, тоді як медіана ВБП для монотерапії осимертинібом — 13,8 міс. ВР становить 0,47, що вказує на значне зниження ризику прогресування захворювання або смерті при комбінованій терапії. Для хворих без метастазів у ЦНС медіана ВБП для осимертинібу + ПХТ становить 27,6 міс, а медіана ВБП для монотерапії осимертинібом — 21,0 міс. ВР становить 0,75, що також вказує на перевагу комбінованої терапії, хоча менш виражену, ніж у пацієнтів з метастазами в ЦНС.
Важливо, що комбінована терапія осимертинібом та ПХТ значно підвищує медіану ВБП у пацієнтів з EGFRm L858R та 19del. Для EGFRm Exon 19del медіана ВБП при комбінованій терапії становить 27,9 проти 19,4 міс при монотерапії, для EGFRm L858R — 24,7 проти 13,9 міс. Показники ВР=0,60 та 0,63 для 19del та L858R, відповідно, вказують на зниження ризику прогресування захворювання або смерті при застосуванні комбінованої терапії.
Профіль безпеки, представлений авторкою, містить інформацію про безпеку прийому осимертинібу в комбінованій та монотерапії. Так, медіана тривалості застосування осимертинібу становила 22,3 міс у групі комбінованої терапії та 19,3 міс — в групі монотерапії. У групі комбінованої терапії хворі отримували в середньому 12 циклів пеметрекседу, а 76% пацієнтів завершили 4 цикли ХТ на основі платини. Найбільш поширеними небажаними явищами в обох групах є діарея, висип, нудота та зниження апетиту. Деякі явища, такі як анемія та тромбоцитопенія, частіше трапляються в групі комбінованої терапії.
Динаміка побічних явищ протягом лікування свідчить, що найвища частота та тяжкість побічних ефектів відмічалися під час індукційної терапії на основі платини протягом перших 3 міс. Частота побічних ефектів II–III ступеня знизилася на ~50% між 0–3-м місяцями (n=135; 49%) та 3–9-м місяцями (n=62; 24%). Найпоширеніші побічні явища III–IV ступеня в групі осимертиніб + ПХТ були асоційовані з гематологічною токсичністю, такою як тромбоцитопенія та зниження рівня нейтрофілів. Частота тяжких побічних явищ ≥III ступеня знижувалася після індукційної дози порівняно з монотерапією осимертинібом. Тож профіль безпеки комбінованої терапії осимертиніб + ПХТ є керованим, а побічні ефекти переважно пов’язані з додаванням ХТ. Окрім того, комбінована терапія осимертинібом дозволяє редукцію дози ХТ у разі виникнення побічних явищ, що потребують управління.
Щодо представленого клінічного випадку, то рішення МДК щодо лікування пацієнтки з прогресуючим НДКРЛ з EGFRm включало ХТ (цисплатин + пеметрексед) +/− променева терапія з подальшою імуноонкологічною терапією. За оптимальний варіант (з урахуванням мутаційного статусу) ухвалено комбінацію цисплатину (75 мг/м2) + пеметрексед (500 мг/м2) 1 раз на 21-й день + осимертиніб (80 мг щоденно) протягом 4 циклів з подальшим підтримуючим режимом осимертинібу (80 мг) + пеметрексед. Рекомендовано контроль ефективності лікування у вигляді КТ ОГК, ОЧП, ОМТ з внутрішньовенним контрастуванням або ПЕТ-КТ після 4 курсів. Через побічні явища перерва в прийомі препаратів тривала 10 діб, після чого лікування було відновлено зі стандартної дози 80 мг/добу. Після 4 курсів лікування за допомогою ПЕТ-КТ від 18.10.2023 р. виявлено позитивну динаміку.
Надалі авторка розглянула вплив початкового вибору терапії на прогноз пацієнтів з EGFRm-позитивним НДКРЛ. Так, осимертиніб у комбінації з ХТ (FLAURA2) зумовлює медіану ВБП — 29,4 міс; монотерапія осимертинібом (FLAURA) забезпечує медіану ВБП 18,9 міс з подальшим можливим застосуванням осимертинібу при прогресуванні; ерлотиніб / гефітиніб (FLAURA) зумовлює медіану ВБП 10,2 міс з подальшими варіантами лікування залежно від статусу мутації T790M; ХТ має медіану ВБП — 5,2 міс.
Отже, результати представлених клінічних досліджень свідчать, що комбінація осимертинібу з ХТ відкриває нову еру в лікуванні EGFRm-позитивного НКДРЛ, забезпечуючи суттєве подовження виживаності пацієнтів та ефективніший контроль захворювання порівняно з монотерапією.
Євгенія Гончарук














Leave a comment