Значення імунотерапії препаратом альфа-/бета-дефензинів у розвитку епітеліїту у хворих на орофарингеальний рак
Гірна Г.А.1, Костишин І.Д.1, Рожко М.М.1, Лукач E.В. 2, Андріїв А.В.1
- 1Івано-Франківський національний медичний університет
- 2Інститут отоларингології ім. професора О.С. Коломійченка НАМН України, Київ
Резюме. Найпоширенішим ускладненням променевої терапії у хворих на рак ротової порожнини і ротоглотки є запальні зміни епітелію слизової оболонки ротової порожнини і підслизової основи у 80% випадків. Для ефективного лікування хворих і мінімізації токсичного ефекту променевої терапії нами використовувався імунний агент альфа-/бета-дефензинів та було проведено аналіз розвитку ступеня та форми епітеліїту. Клінічне спостереження проводили за хворими у двох групах: 1-ша — 25 пацієнтів, які на 1-му етапі спеціального лікування отримували променеву терапію та імунотерапію альфа-/бета-дефензинами; 2-га (променева) — 20 хворих, яким проводили променеву терапію без імунотерапії, які становили групу порівняння. Результатом застосування імунотерапевтичного агента альфа-/бета-дефензинів є зменшення частоти і ступеня епітеліїту у хворих на рак ротової порожнини і ротоглотки під час та після завершення променевого лікування. У 3 (12%) хворих 1-ї групи не виникло епітеліїту, епітеліїт І ступеня (катаральний) відмічали у 11 (44%) хворих, у 10 (40%) розвинувся епітеліїт ІІ ступеня (вогнищевий), у 1 (4%) — ІІІ (плівчастий). У групі порівняння у всіх хворих виявляли більш виражений епітеліїт різного ступеня і форми: в 1 (5%) пацієнта відмічали епітеліїт І ступеня (катаральний), у 3 (15%) — ІІ ступеня (вогнищевий), у 16 (80%) — ІІІ (плівчастий), тобто з епітеліїтом було на 15 хворих більше, ніж у 1-й групі. Окремо проводилося визначення впливу на розвиток тяжчого (ІІІ, ІV) ступеня епітеліїту, форми росту пухлини, її гістологічної диференціації, локалізації. Дані не підтвердили цієї залежності. Представлені показники спостереження вказують на позитивну динаміку від імунотерапії, більшість хворих завершили лікування із менш обтяжливим ступенем епітеліїту.
Одержано 27.01.2021
Прийнято до друку 12.04.2021
DOI: 10.32471/clinicaloncology.2663-466X.43-3.28502
Зв’язок публікації з плановими науково-дослідними роботами. Робота є фрагментом науково-дослідної роботи кафедри стоматології Навчально-наукового інституту післядипломної освіти Івано-Франківського національного медичного університету «Клінічна ефективність комплексного лікування захворювань твердих тканин зубів та пародонту у населення екологічно несприятливих регіонів», державний реєстраційний номер 0118U004144.
Вступ
Основними методами лікування хворих на рак ротової порожнини і ротоглотки є: хірургічний, променевий, хіміотерапевтичний в різних послідовностях. Променева терапія є компонентом комбінованого чи комплексного лікування, тому найчастіше застосовуваним [1]. Найбільш поширеним ускладненням променевої терапії є запальні зміни епітелію слизової оболонки порожнини рота та ротоглотки і підслизової основи у 80% випадків, що називається епітеліїтом [2, 3]. Розрізняють катаральну, вогнищеву (острівцеву), плівчасту і виразково-некротичну його форми, та, відповідно, 4 ступені епітеліїту, залежно від переважання фази запалення слизової орофарингеальної ділянки [4]. Розвиток цієї патології супроводжується болем, появою ерозій слизової оболонки ротової порожнини, втратою апетиту, погіршенням харчування, зменшенням маси тіла. Для пацієнтів серед усіх ускладнень епітеліїт є найбільш виснажливим і погіршує якість життя. Іноді доводиться припинити лікування через виражений епітеліїт. Це є однією з причин, яка впливає на результати терапії [5].
Променева терапія поглиблює імунодефіцит, який наявний у онкологічних хворих. У такому стані порушується функціонування ланок імунної системи, що проявляється їх патологічною реакцією на розвиток інфекції. Враховуючи виникнення такої дисфункції, включення імунотерапії до основної схеми лікування пацієнтів онкологічного профілю є доцільним [6].
Для ефективного лікування хворих шляхом мінімізації токсичного ефекту променевої терапії використовуються лікарські засоби різних фармакологічних груп, у тому числі імунопрепарати. Нами вперше пропонується використання імунного агента альфа-/бета-дефензинів як препарату супроводу променевої терапії.
Імунопрепарат альфа-/бета-дефензинів — комплекс пептидів і вільних амінокислот, отриманий шляхом специфічного протеолізу білків тваринного походження. Вивчали його ефективність в онкології як протипухлинного засобу та у якості препарату супроводу спеціального лікування для зменшення вираженості побічної дії хіміопроменевого лікування [7, 8]. Препарат, маючи виражені антитоксичні ефекти, прискорює відновлювальні процеси та корегує порушення функцій імунної системи. Він впливає на медіатори запалення, пригнічує продукцію прозапальних цитокінів (інтерлейкін-4 — IL-4), підвищує активність основних клітин неспецифічного захисту — фагоцитів, також природних кілерів, знижує сенсибілізацію організму до чужорідного білка, підвищує резистентність, достовірно збільшує кількість Т-супресорів, Т-хелперів-2, підвищує рівень сироваткового інтерферону-γ. Також він нормалізує показники сироваткового фактора некрозу пухлини-α, який, у свою чергу, впливає на гладкі клітини. Імунний агент альфа-/бета-дефензинів, крім безпосереднього впливу на ланки імунної системи, також діє опосередковано, через систему нейроендокринної регуляції [9, 10].
Мета дослідження: оцінити ускладнення і їх ступінь вираженості у хворих на рак ротової порожнини і ротоглотки, яким проводили променеву терапію 1-м етапом лікування на фоні імунотерапії препаратом альфа-/бета-дефензинів.
Об’єкт і методи
Нами проведено променеву терапію на 1-му етапі спеціального лікування 45 пацієнтам з вперше діагностованим плоскоклітинним раком ротової порожнини і ротоглотки в Комунальному некомерційному підприємстві «Прикарпатський клінічний онкологічний центр Івано-Франківської обласної ради». Лікування здійснювалося за показаннями пацієнтам віком до 85 років з різними стадіями. Променева терапія була компонентом спеціального чи паліативного лікування, проводилася на апараті «Cobalt-60» до сумарної дози 36–40 Гр (разова вогнищева доза (РВД) — 2–2,5 Гр, 5 сеансів на тиждень) за 1-й етап лікування. Усі хворі знали про можливість проведення додатково імунотерапії, було надано інформацію про показання до її застосування, властивості, ефективність, можливі ускладнення. У разі згоди (письмової) хворі отримували променеве лікування та імунотерапію, вони формували 1-шу групу (25 хворих). Хворі, яким не проводили імунотерапію, ввійшли до 2-ї порівняльної групи (20 хворих). Імунопрепарат альфа-/бета-дефензинів вводили хворим за схемою: 2,0 мл 2 рази на добу внутрішньом’язово за 2 дні до початку спеціального лікування протягом 5 днів, а в наступні 10 днів протягом лікування — 1 раз на добу.
Дослідження проводилося з дотриманням принципів Гельсінської декларації. Протокол випробування було затверджено комісією з питань етики Івано-Франківського національного медичного університету щодо дотримання етичних принципів (протокол від 16.11.2017 р. № 94/17). Для проведення дослідження було отримано інформовану згоду пацієнтів.
Перед лікуванням усім хворим за показаннями проводилася санація порожнини рота (професійна гігієна ротової порожнини), за необхідності (наявності коронок із різних металів) виготовлялися захисні пластмасові капи. Протягом променевої терапії хворі місцево отримували супровідну терапію, яка включала використання антисептиків: полоскання розчинами екстрактів квіток ромашки, квіток нагідок та деревію, лікарськими травами — мати-й-мачуха, календула, ромашка або шавлія. Також використовувалися антисептики у вигляді льодяників чи таблеток декаметоксину, ацетиламінонітропропоксибензолу. Серед радіопротекторів нами застосовувалися мазь цинку гіалуронату, з якої готували суміш для змащування слизової оболонки ротової порожнини, і крем, до складу якого входили оливкова олія, міристил міристат, мелеат соєвої олії, цетеарил оливат тощо, яким змащували ділянки шкіри, що входили в зону опромінення. З кератепластиків для слизової оболонки ротової порожнини і шкіри застосовувалися різні варіанти: декспантенол, ретинол, олійний екстракт з м’якоті плодів шипшини рідкий, метронідазол, хлоргексидин [11, 12].
Серед 25 хворих 1-ї групи була тільки 1 (4%) жінка. Середній віковий показник — 58,5 років, але найнижчою віковою межею було 33 роки, а найвищою — 79 років. Першорядними причинами виникнення раку порожнини рота чи ротоглотки є зловживання алкоголем і куріння. З анамнезу відомо, що 17 (68%) хворих надмірно вживали алкоголь протягом життя, а 4 (16%) — помірно і стільки ж (16%) не зловживали спиртними напоями. 21 (84%) хворий — хронічні курці із середнім стажем куріння 36,5 років, які палили більше 1 пачки сигарет на день.
2-га група налічувала 20 хворих, серед яких було 5 (25%) жінок і 15 (75%) чоловіків. Вікові межі — 44–82, із середнім показником — 61,3 років. Не зловживали алкоголем тільки 3 (15%) хворих, 15 (75%) вживали спиртні напої надмірно, а 2 (10%) — помірно. Також причиною розвитку злоякісної пухлини в цій групі були хронічна травма в 2 (10%) хворих гострими краями каріозних зубів і в 2 (10%) — протезом. 15 (75%) хворих були хронічними курцями зі стажем у середньому 38,7 років і палили більше 1 пачки.
Серед хворих 1-ї групи тільки в 1 (4%) була І стадія раку порожнини рота, 5 (20%) хворих мали ІІ стадію, 9 (36%) хворих — ІІІ. Найбільше було хворих із ІVА стадією — 9 (36%), і 1 (4%) хворий із ІVВ.
Серед хворих групи порівняння із ІІІ стадією — 10 (50%) хворих, 9 (45%) із ІVА стадією та 1 (5%) пацієнт із ІVВ стадією. Розподіл пацієнтів з онкопатологією ротової порожнини та ротоглотки за стадіями у групах представлено в табл. 1.
| Стадія | Група 1, N=25 | Група 2, N=20 | ||||||
| ротова порожнина, n=13 | ротоглотка, n=12 | ротова порожнина, n=12 | ротоглотка, n=8 | |||||
| n | % | n | % | n | % | n | % | |
| T1N0M0 | 1 | 4 | ||||||
| T1N1M0 | 1 | 5 | ||||||
| T2N0M0 | 2 | 8 | 3 | 12 | ||||
| T2N1M0 | 2 | 10 | ||||||
| T2N2M0 | 1 | 4 | ||||||
| T3N0M0 | 1 | 4 | 1 | 4 | 1 | 5 | 1 | 5 |
| T3N1M0 | 3 | 12 | 4 | 16 | 2 | 10 | 3 | 15 |
| T3N2M0 | 2 | 8 | 2 | 10 | 3 | 15 | ||
| T3N3M0 | 1 | 5 | ||||||
| T4N0M0 | 1 | 5 | ||||||
| T4N1M0 | 2 | 8 | 1 | 4 | ||||
| T4N2M0 | 3 | 12 | 3 | 15 | ||||
| T4N3M0 | 1 | 4 | ||||||
Розподіл хворих у групах залежно від диференціації пухлини та форми росту відображено в табл. 2.
| Показник | Група 1, N=25 | Група 2, N=20 | ||||||
| ротова порожнина, n=13 | ротоглотка, n=12 | ротова порожнина, n=12 | ротоглотка,n=8 | |||||
| n | % | n | % | n | % | n | % | |
| G1 | 5 | 20 | 3 | 12 | 5 | 25 | 0 | 0 |
| G2 | 6 | 24 | 4 | 16 | 5 | 25 | 7 | 35 |
| G3 | 2 | 8 | 5 | 20 | 2 | 10 | 1 | 5 |
| Екзофіт | 0 | 0 | 1 | 4 | 1 | 5 | 2 | 10 |
| Ендофіт | 10 | 40 | 6 | 24 | 6 | 30 | 4 | 20 |
| Мезофіт | 3 | 12 | 5 | 20 | 4 | 20 | 3 | 15 |
У 1-й групі розподіл хворих за локалізацією пухлини був наступним: 3 (12%) хворих мали пухлину бокового відділу дна порожнини рота, 4 (16%) — фронтального відділу дна рота. Плоскоклітинний рак слизової оболонки альвеолярного відростка нижньої щелепи відмічали у 2 (8%) пацієнтів, а верхньої щелепи — у 1 (4%). Онкопатологію м’якого піднебіння було зафіксовано у 6 (24%) хворих і у 1 (4%) — твердого. У 1 (4%) пацієнта пухлина розвинулася в ретромолярній ділянці, ще в 1 (4%) хворого — в корені і боковій частині язика. У 5 (20%) хворих визначено поширений рак ротоглотки. У більшості хворих пухлина поширювалася на сусідні анатомічні ділянки, тільки у 6 (24%) поширення не відмічали (рис. 1).
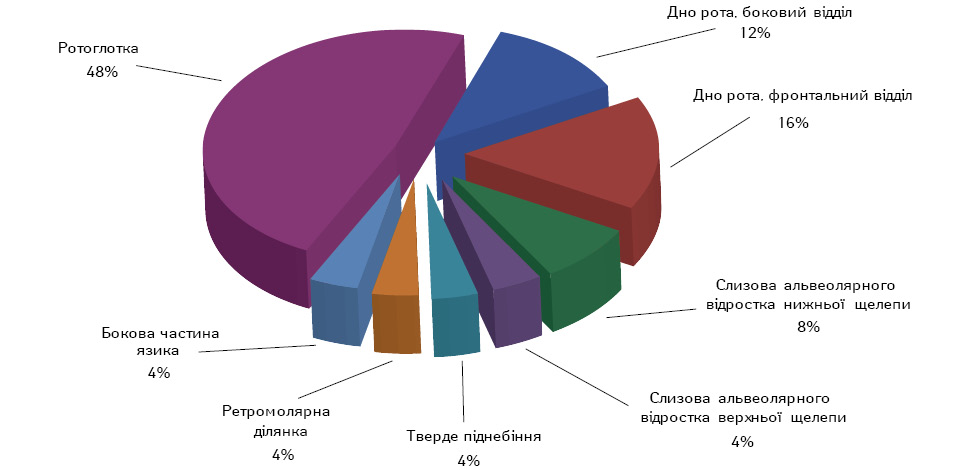
Серед хворих 2-ї групи із раком бокового відділу дна порожнини рота було 4 (20%), а фронтального відділу — 3 (15%) пацієнти, із пухлиною язика — 3 (15%). По 1 (5%) хворому було із пухлиною ретромолярної ділянки, слизової оболонки альвеолярного відростка нижньої щелепи, м’якого піднебіння, кореня язика. Пухлини ротоглотки великих розмірів мали 6 (30%) хворих (рис. 2), 15 (75%) — пухлини великого розміру, що поширювалися на кілька сусідніх ділянок, і у 5 (25%) не відмічали поширення.
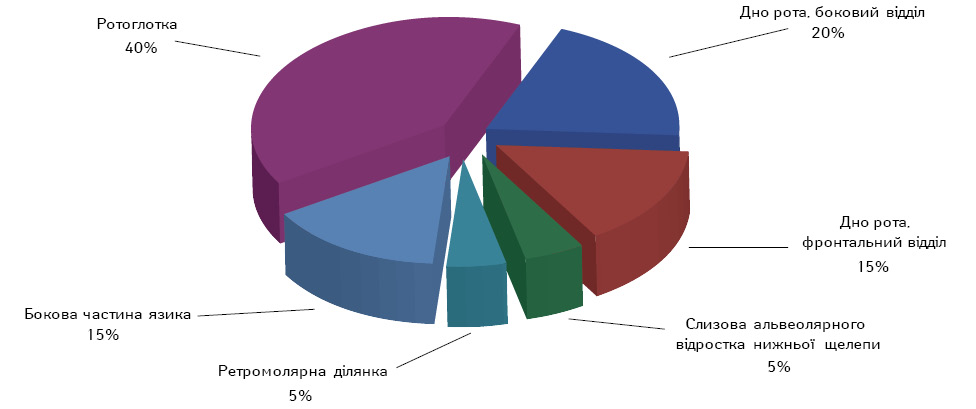
1-м етапом хворі 1-ї групи отримали курс променевого лікування та імунотерапії препаратом альфа-/бета-дефензинів. З усіх хворих паліативне лікування проводили 4 (16%). Більша частина хворих, а саме 18 (72%), отримали заплановану дозу 40 Гр, 1 (4%) навіть 44 Гр, 4 (16%) пацієнти — 38 Гр, 1 (4%) — 34 Гр, 1 (4%) хворий завершив 1-й етап променевого лікування на 26 Гр.
Хворі 2-ї групи отримували променеве лікування без імунотерапії. 9 (45%) пацієнтів плановано отримували паліативну терапію. Після 1-го етапу дистанційної гамматерапії 12 (60%) хворих одержали дозу 40 Гр, по 3 (15%) пацієнти — нижчу — 38 Гр і 36 Гр, також по 1 (5%) — 22 Гр та 20 Гр.
Результати і обговорення
Поява ускладнень, їх ступінь і форми оцінювалася у хворих на рак порожнини рота і ротоглотки, які отримували променеве лікування з імунотерапією та без неї. Також дані було представлено, враховуючи локалізацію, стадію пухлини та інші її особливості.
У період спостереження за пацієнтами впродовж лікування у хворих 1-ї групи виникав різного ступеня і форми променевий епітеліїт і тільки у 3 (12%) його не відмічали. Епітеліїт І ступеня (катаральний) було виявлено у 11 (44%) пацієнтів, у 10 (40%) — ІІ ступеня (вогнищевий) і в 1 (4%) — ІІІ (плівчастий).
У групі порівняння у всіх хворих також відмічали епітеліїт різного ступеня і форми. В 1 (5%) хворого виявлено епітеліїт І ступеня (катаральний), у 3 (15%) — ІІ ступеня (вогнищевий) та в 16 (80%) — ІІІ (плівчастий), що зображено на рис. 3. Таке порівняння показує позитивний ефект імунотерапії препаратом альфа-/бета-дефензинів на розвиток епітеліїту під час променевого етапу лікування.
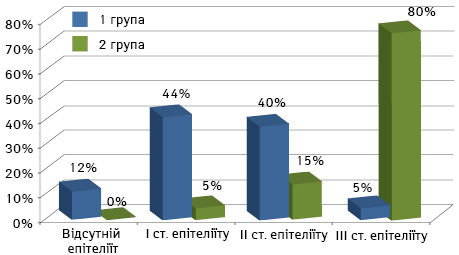
Аналіз виникнення певного ступеня епітеліїту залежно від стадії раку порожнини рота чи ротоглотки в 1-й групі хворих показав, що із І стадією було виявлено 1 пацієнта, і у нього розвинувся епітеліїт ІІ ступеня (вогнищевий). Із ІІ стадією було 2 хворих (8%), у яких не відмічали епітеліїту, і у 3 (12%) виник епітеліїт І ступеня (катаральний). Найбільше було хворих із ІІІ та ІV стадіями, відповідно, вищою була і частота ускладнень. Серед пацієнтів з ІІІ стадією відмічено по 4 (16%) з епітеліїтом І і ІІ ступеня (катаральний, вогнищевий) та 1 (4%) — ІІІ ступеня (плівчастий). Серед хворих із ІV стадією найбільше було із ІІ ступенем епітеліїту (вогнищевим) — 5 (20%), із катаральним — 4 (16%) і в 1 (4%) пацієнта не відмічали такої патології.
Порівнюючи 1-шу і 2-гу групи, можна відмітити, що в 2-й групі хворих із І і ІІ стадіями не було. Але із ІІІ стадією було майже стільки ж хворих, як і в 1-й групі, і серед них більше хворих із ІІІ ступенем епітеліїту — 8 (40%) проти 1 (4%) в 1-й групі. З епітеліїтом І і ІІ ступеня було відмічено по 1 (5%) хворому. Аналізуючи ступінь епітеліїту у хворих з ІІІ стадією, можна зазначити, що в групі пацієнтів, які не отримували імунотерапію, частіше виникав тяжчий ступінь епітеліїту, а саме ІІІ, ніж у групі, що отримувала імунотерапію, де частіше фіксували епітеліїт І і ІІ ступеня. Кількість хворих із ІV стадією в групі порівняння була такою ж самою, як і в дослідницькій. Явища епітеліїту ІІ ступеня (вогнищевий) були відмічені у 4 (20%) хворих, а ІІІ ступеня (плівчастий) — у 6 (30%). Це також відображає негативну динаміку, тобто наявність ІІІ ступеня епітеліїту, водночас у 1-й групі його не виявляли.
Таке порівняння показує, що розвиток тяжчого ступеня епітеліїту не залежить від стадії захворювання і виникає в меншої кількості хворих, яким призначали терапію імунним агентом альфа-/бета-дефензинів (рис. 4).
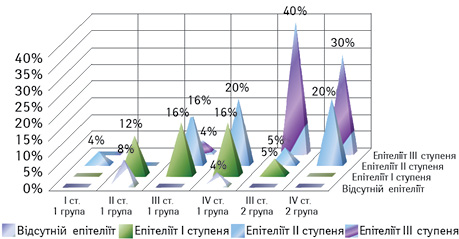
Серед хворих 1-ї групи, у яких було діагностовано плоскоклітинний рак G1, у 2 (8%) пацієнтів відмічали І ступінь епітеліїту, у 5 (20%) — ІІ ступінь і в 1 (4%) — ІІІ. Порівнюючи з 2-ю групою, де було 2 (10%) хворих із ІІ ступенем і 3 (15%) — із ІІІ, слід зазначити, що в цій групі було більше пацієнтів з ІІІ ступенем і не було з І ступенем (рис. 5).
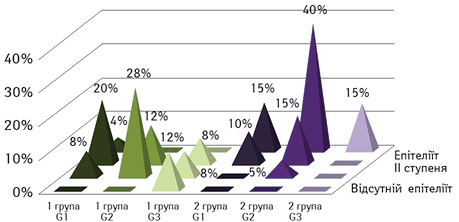
Пацієнти дослідницької групи із плоскоклітинним раком G2 мали наступне співвідношення за розвитком епітеліїту: 7 (28%) хворих, у яких розвинувся епітеліїт І ступеня, і 3 (12%) — у яких відмічали ІІ ступінь, ІІІ ступеня епітеліїту в цих хворих не виявляли. У групі порівняння було дещо інакше співвідношення: тільки 1 (5%) хворий з І ступенем, 3 (15%) — з ІІ ступенем і 8 (40%) — з ІІІ.
Низькодиференційований рак порожнини рота і ротоглотки у 1-й групі відмічено у 7 хворих, серед яких у 3 (12%) лікування пройшло без ускладнень і явищ радіоепітеліїту, у 2 (8%) був І ступінь і в 2 — ІІ ступінь. В групі порівняння було всього 3 (15%) хворих із плоскоклітинним раком G3, у яких розвинувся епітеліїт ІІІ ступеня. Як видно з рис. 3, найбільше спостерігалося хворих із ІІІ ступенем епітеліїту і диференціацією пухлини G2 у групі хворих без імунотерапії, а епітеліїт І ступеня серед усіх пацієнтів відмічали в цій групі в найменшій кількості — 5%. У основній групі найбільше було хворих із І ступенем, також із плоскоклітинним G2. У цій групі не відмічали епітеліїту в 12% хворих. Тяжкого ступеня епітеліїт зафіксовано у 2-й групі хворих незалежно від диференціації пухлини (рис. 5).
Згідно з даними (рис. 6), в 1-й групі з ендофітним ростом пухлини було 2 (8%) хворих, у яких не відмічали епітеліїту, з початковим ступенем, тобто І — 7 (28%) хворих, з ІІ — 6 (24%) і тільки в 1 хворого виявлено епітеліїт ІІІ ступеня. Показники 1-ї групи були дещо кращими порівняно з 2-ю, оскільки в останній тільки у 3 (15%) пацієнтів виявляли епітеліїт ІІ ступеня і в 7 (35%) — ІІІ.
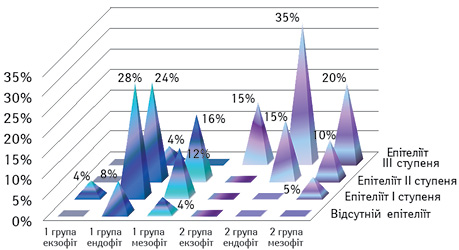
Екзофітну форму росту пухлини мав тільки 1 хворий 1-ї групи і 3 пацієнти 2-ї групи, відповідно, в 4% хворих виник епітеліїт І ступеня і в 15% — ІІІ. Кількість хворих із змішаним ростом ракової пухлини у двох групах була майже однаковою, але пацієнти із тяжчим, ІІІ ступенем епітеліїту, були тільки у 4 (20%) осіб з групи порівняння. У групі хворих, яким проводили променеве лікування й імунотерапію, був 1 (4%) хворий без епітеліїту протягом лікування, 3 (12%) — з епітеліїтом І ступеня і 4 (16%) — ІІ ступеня. У 2-й групі явища катарального епітеліїту відмічали у 1 (5%) хворого і вогнищевий епітеліїт ІІ ступеня — у 2 (10%). Аналізуючи розвиток ускладнень залежно від форми росту пухлини, можна відзначити, що найбільше було хворих з ендофітною пухлиною в обох групах, але в 2-й групі, яка не отримувала імунотерапію, у більшої кількості хворих відмічали епітеліїт ІІІ ступеня (плівчаста форма). Такий аналіз показує, що форма росту пухлини не має впливу на розвиток того чи іншого ступеня і форми епітеліїту, а імунотерапія впливає.
Порівняльний аналіз наявності епітеліїту залежно від локалізації пухлини показує, що в 1-й групі хворих з раком ротоглотки було 6 пацієнтів (24%) з І ступенем, 3 (12%) — з ІІ, і у 3 (12%) він не розвинувся. А у 8 (40%) хворих 2-ї групи також з раком ротоглотки був тільки епітеліїт ІІІ ступеня. У пацієнтів із пухлиною дна порожнини рота в 1-й групі були дещо кращі результати, тільки 2 (8%) хворих з І ступенем епітеліїту і 1 (4%) — з ІІІ, у той час, як у 2-й групі було 2 (10%) хворих із ІІІ ступенем і по 1 (5%) з І і ІІ. У всіх хворих 1-ї групи з раком фронтального відділу дна порожнини рота відмічали епітеліїт ІІ ступеня. У групі порівняння у 2 осіб(10%) — ІІ ступінь і в 1 (5%) — ІІІ. По 1 хворому було у групах із пухлиною ретромолярної ділянки і в хворого 1-ї групи розвинувся тільки епітеліїт І ступеня, а 2-ї групи — ІІІ ступеня.
Більшість хворих отримали заплановану дозу променевої терапії 44–36 Гр.
Порівнюючи хворих між групами, які отримали дозу 44–40 Гр, визначено, що в 3 (12%) хворих 1-ї групи до кінця лікування не розвинувся епітеліїт, по 7 (28%) хворих мали І та 8 (32%) — ІІ ступінь і тільки 3 (12%) — ІІІ. В 2-й групі було більше хворих з ІІІ ступенем — 40%, а 15% — мали ІІ ступінь радіоепітеліїту.
Хворі 1-ї групи, які одержали 38–36 Гр, також мали нижчий ступінь епітеліїту, І і ІІ — по 12 і 8% відповідно і не було ІІІ ступеня, а в 2-й групі у 5 осіб (25%) його відмічали (рис. 7, 8).
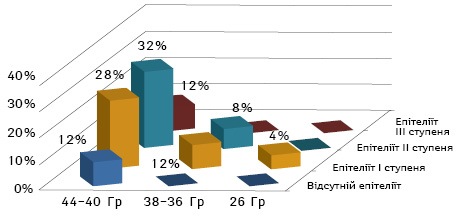
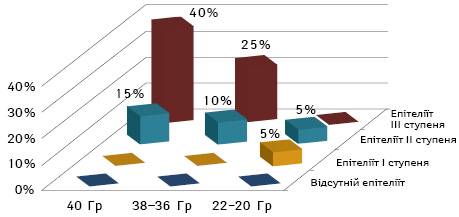
Такий критерій порівняння показав, що при однакових дозах лікування епітеліїт ІІІ ступеня розвинувся в більшої кількості хворих 2-ї групи і в ній не фіксували І ступеня, що показує позитивний ефект імунотерапії в 1-й групі.
Висновки
1. Включення імунопрепарату альфа-/бета-дефензинів в схему лікування хворих на рак порожнини рота і ротоглотки є ефективним, оскільки значно зменшує частоту і ступінь радіоепітеліїту: на 65% хворих більше мали епітеліїт ІІІ ступеня в групі, яка не отримувала імунотерапію.
2. Не виявлено залежності між розвитком тяжчого ступеня і форми епітеліїту від стадії, диференціації, форми, локалізації пухлини, але відмічено вплив включення імунотерапії в лікування.
3. У хворих, у схему лікування яких включали імунотерапію альфа-/бета-дефензинами, доза променевої терапії не вплинула на розвиток тяжчого ступеня і форми епітеліїту так, як це відбулося у пацієнтів, яким не призначали імунотерапевтичний агент.
Перспективи подальших досліджень. Спостереження в клініці за позитивним впливом імунопрепарату альфа-/бета- дефензинів на розвиток радіоепітеліїту будуть висвітлені з врахуванням даних місцевого і системного імунітету в подальших наукових працях.
Список використаної літератури
1. Думанський, Ю. В., Шевченко, А. І., Галайчук, І. Й., Розуменко, В. Д., & Крижанівська, А. Є. (2019). Онкологія. (2-ге вид.). Київ: Медицина.
2. Janaine, S., Nasiloski, K. S., & Gomes, A. P. (2014). Oral complications in patients receiving head and neck radiation therapy: a literature review. Rio Grande do Sul Dental Journal, 62(4), 395–400. doi:org/10.1590/1981-863720140004000007573.
3. Гірна, Г. А., Рожко, М. М., & Костишин, І. Д. (2017). Вплив променевої терапії на стан тканин і функцію органів щелепно-лицевої ділянки. Современная стоматология, 5(89), 26–35.
4. Bowen, J., Al-Dasooqi, N., & Bossi, P. (2019). The pathogenesis of mucositis: updated perspectives and emerging targets. Support Care Cancer, 27(10), 4023–33. doi: 10.1007/s00520-019-04893-z.
5. Коробко, Є. В., & Процик, В. С. (2015). Зміни якості життя хворих на рак ротової порожнини під впливом індукційної хіміотерапії та променевої терапії. Журнал вушних, носових і горлових хвороб, 6, 48–54. doi:http://www.lorlife.kiev.ua/2015/2015_6_48.pdf.
6. Іванкова, В. С., Нестеренко, Т. М., Барановська, Л. М., & Хруленко, Т. В. (2016). Профілактичні заходи запобігання пізнім променевим ускладненням при консервативному хіміопроменевому лікуванні місцево-поширених форм раку шийки матки. Український радіологічний журнал, 24, 59–63.
7. Литвиненко, А. А. (2012). Роль иммунокоррекции в комплексном лечении рака молочной железы. Здоровье женщины, 1(67), 134–7. doi:http://nbuv.gov.ua/UJRN/Zdzh_2012_1_12.
8. Сивкович, С. А. (2002). Аспекты лечения больных злокачественными лимфомами. Провизор, 19, 43–4. doi: http://immunologs.com.ua/uploads/files/articles/234/ 4-propes-2010-151010.pdf#page=27.
9. Мамчур, В. И., & Левых, А. Э. (2012). Дефензины — эндогенные пептиды с антиинфекционными и противоопухолевыми свойствами (обзор литературы). Таврический медико-биологический вестник, 5(58), 315–21. doi:http://dspace.nbuv.gov.ua/bitstream/handle/123456789/45235/70-Mamchur.pdf?sequence=1.
10. Захаренко, В. В., Найштетик, В. Я., Кудрявцева, И. Г., Шарыкина, Н. И., Карацуба, Т. А., & Хавич, А. А. (2004). Фармакологические свойства препарата Пропес (экспериментальные исследования). Онкология, 6(3), 36–7. doi:http://immunologs.com.ua/uploads/ files/articles/234/4-propes-2010-151010. pdf#page=47.
11. Костишин, І. Д., Іванкова, В. С., Гірна, Г. А., & Ткач, В. Є. (2017). Сучасний погляд на методи профілактики і лікування уражень слизової порожнини рота і шкіри при променевому лікуванні злоякісних пухлин ротоглотки. Променева діагностика і променева терапія, 2, 66–77. doi:http://medlib.dp. gov.ua/ jirbis2/ images/ fond_publications/ promeneva-diagnostika/ promeneva- diagnistika- promeneva-terapiya_2017_2.pdf.
12. Фелдій, П. Г. (2004). Профілактика та лікування місцевих променевих ушкоджень верхніх дихальних шляхів у ЛОР-онкологічних хворих. (Автореф. дис. канд. мед. наук). Інститут отоларингології ім. О.С. Коломійченка. Київ.
Адреса:
Гірна Галина Анатоліївна
77500, Івано-Франківська обл., м. Долина, вул. Івана Франка, 43
E-mail: halynagіrna@gmail.com
Сorrespondence:
Girna Halyna
43 Ivan Franko Str., Dolyna 77500, Ivano-Frankivsk region
E-mail: halynagіrna@gmail.com














Leave a comment