Знеболення при високотравматичних торакальних операціях. Опис проблеми на прикладі серії клінічних випадків
Резюме. Високотравматичні торакальні операції — це операції зі значним пошкодженням каркасу грудної клітки, які часто супроводжуються резекцією ребер, груднини, ключиці, іноді пошкодженням хребців. Планування знеболення пацієнтів, яким виконуються такі операції, має бути персоналізоване та здійснюватися з урахуванням факторів, пов’язаних як із самою операцією (видом хірургічної травми, доступом, прогнозованою крововтратою), так і з вихідним функціональним статусом пацієнта. У цій статті представлена серія із 4 клінічних випадків хворих з відмінними вихідними станами, яким були виконані високотравматичні торакальні операції з різним ступенем пошкодження каркасу грудної клітки. Описані клінічні приклади можуть бути використані як модель для розробки анестезіологічних стратегій у пацієнтів, яким виконуються високотравматичні торакальні операції.
Одержано 29.01.2026
Прийнято до друку 6.02.2026
DOI: 10.32471/clinicaloncology.2663-466X.35543
ВСТУП
Високотравматичні торакальні операції — це операції зі значним пошкодженням каркасу грудної клітки, після яких наявний виражений больовий синдром та відмічається суттєве обмеження екскурсії легень. Такі операції мають нетиповий перебіг, вони супроводжуються різною хірургічною травмою, і вибір знеболення пацієнтів, яким виконуються такі операції, потребує персоналізованого планування з урахуванням хірургічних аспектів та індивідуальних особливостей пацієнта.
До факторів, що стосуються самої операції, належить насамперед вид хірургічної травми. Варто брати до уваги запланований об’єм резекції елементів каркасу грудної клітки, адже такі операції часто супроводжуються резекцією ребер, груднини, ключиці, іноді пошкодженням хребців. Другий аспект, на який треба зважати при виборі знеболення при високотравматичних торакальних операціях, це вид хірургічного доступу [1]. Для виконання таких операцій часто в якості доступу здійснюється поперечна стернотомія з двобічною торакотомією, що є одним із найбільш травматичних доступів у хірургії загалом. Також варто зважати на те, чи буде виконуватися резекція легень і в якому об’ємі вона запланована. Крім того, необхідно спрогнозувати об’єм можливої крововтрати. Цей аспект також важливий при плануванні знеболення, адже пацієнти, які інтраопераційно мали значну крововтрату, як правило, з вищою ймовірністю матимуть проблеми з гемодинамікою в післяопераційний період, що певним чином може впливати на можливість застосування торакальної епідуральної анестезії (ТЕА) або проведення аналгоседації, оскільки використання цих методів знеболення може бути асоційованим з артеріальною гіпотензією [2, 3].
Серед характеристик пацієнта, які значною мірою впливають на планування знеболення, варто виділити вихідний функціональний статус пацієнта, ступінь пошкодження каркасу грудної клітки та запланований об’єм резекції легень. Інтегральна оцінка цих факторів дозволяє передбачити, чи потребуватиме пацієнт проведення подовженої штучної вентиляції легень (ШВЛ) в післяопераційний період. Крім того, варто зважати на можливість використання регіонарних методів анестезії та потребу в проведенні аналгоседації у певного пацієнта.
Метою роботи є представлення клінічного досвіду знеболення торакальних операцій, що супроводжуються високим травматизмом і значним пошкодженням каркасу грудної клітки, на прикладі 4 клінічних випадків.
МАТЕРІАЛИ ТА МЕТОДИ дослідження
У статті представлено опис серії клінічних випадків знеболення високотравматичних операцій, проведених у відділенні пухлин легень та середостіння Державного некомерційного підприємства «Національний інститут раку» (Київ) у 2024–2025 рр.
КЛІНІЧНИЙ ВИПАДОК № 1
Пацієнт: жінка, 33 роки.
Діагноз: гігантська ліпосаркома переднього середостіння (рис. 1).
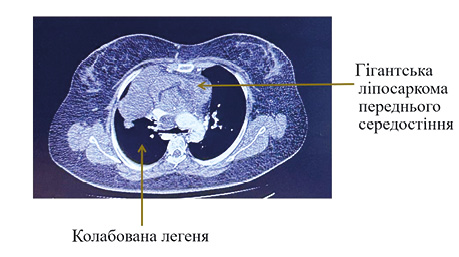
Рис. 1. Передопераційний знімок ком’ютерної томографії (КТ), який демонструє ступінь компресії легені пухлиною
Оперативне втручання: видалення гігантської ліпосаркоми переднього середостіння з перев’язкою та резекцією лівої плечеголовної вени (рис. 2).
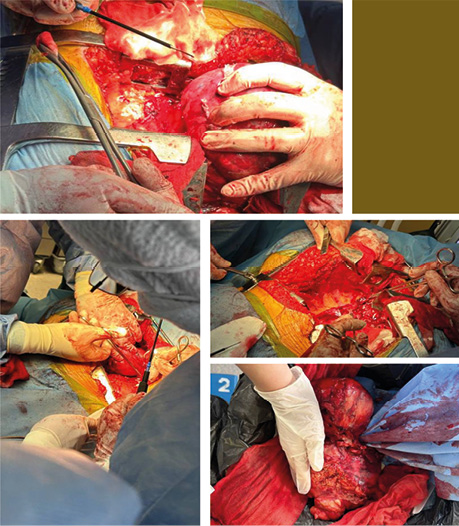
Рис. 2. Видалення гігантської ліпосаркоми переднього середостіння
Хірургічний доступ: поперечна стернотомія з двобічною торакотомією, доповнена серединною стернотомією від 4-го міжребер’я до яремної вирізки.
Крововтрата: 1500 мл.
Незважаючи на свій молодий вік, пацієнтка мала поганий функціональний стан, що насамперед пов’язано із синдромом верхньої порожнистої вени (ВПВ), який розвинувся на тлі основного процесу. Крім того, за даними функції зовнішнього дихання (ФЗД), пацієнтка мала значно знижені дихальні резерви (життєва ємність легень (ЖЄЛ) 1,81 л / 49,45%, об’єм форсованого видиху за 1-шу секунду (ОФВ1) 1,01 л / 31,87%), а також був наявний екзогенний синдром Іценко — Кушинга, який розвинувся на тлі тривалого прийому глюкокортикостероїдів, ожиріння II ступеня.
У післяопераційний період існував досить високий ризик розвитку післяопераційної пневмонії з огляду на наявну компресію дихальних шляхів та лівої легені пухлиною, а також тривалий час перебування лівої легені в колабованому стані. Зважаючи на велику хірургічну травму та високу ймовірність розвитку післяопераційної пневмонії, передбачалося проведення подовженої ШВЛ. При виборі методу знеболення опція застосування ТЕА не розглядалася через наявність у пацієнтки синдрому ВПВ. З огляду на ризик значної крововтрати (не відомий до операції ступінь судинної інвазії), проведено відповідну підготовку (завчасна заготівля препаратів крові, адекватний венозний доступ (v. femoralis dextra et sinistra), Cell Saver, симпатоміметична підтримка).
Після операції пацієнтка була доставлена у відділення анестезіології та інтенсивної терапії (ВАІТ) для проведення подовженої ШВЛ у режимі постійного позитивного тиску в дихальних шляхах з підтримкою тиском (Continues Positive Airway Pressure / Pressure Support Ventilation — CPAP / PS). Під час проведення ШВЛ пацієнтці виконано кілька санаційних бронхоскопій. Хвора перебувала на подовженій ШВЛ протягом 18 год, під час ШВЛ проводилася аналгоседація із застосуванням пропофолу, мідазоламу, фентанілу. На 2-гу добу після операції пацієнтка була екстубована. Починаючи з 2-ї доби, знеболення проводилося шляхом дробного введення морфіну із застосуванням інших аналгетиків відповідно до концепції мультимодальної анальгезії. У пацієнтки була значна інтраопераційна крововтрата, проте завдяки підготовці з нею вдалося впоратися та адекватно компенсувати.
Результати лікування цієї пацієнтки виявилися кращими, ніж очікувалося. Упродовж 1-ї доби жінка перебувала у ВАІТ на подовженій ШВЛ, на 2-гу добу хвора була екстубована, на 3-тю — переведена до профільного відділення, на 11-ту —виписана зі стаціонару.
КЛІНІЧНИЙ ВИПАДОК № 2
Пацієнт: чоловік, 38 років.
Діагноз: пухлина переднього середостіння.
Оперативне втручання: видалення пухлини середостіння з тимусектомією, резекцією ВПВ, правої та лівої плечеголовних вен, дуги непарної вени, правого діафрагмального та блукаючого нервів, ділянки перикарда та пластика перикарда сіткою.
Хірургічний доступ: поперечна стернотомія з двобічною торакотомією (рис. 3).
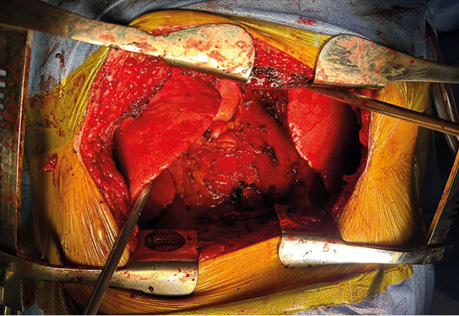
Рис. 3. Поперечна стернотомія з двобічною торакотомією
Крововтрата: 1500 мл.
Функціональний статус пацієнта в цьому випадку був кращим порівняно з першим кейсом. Проте також був наявний синдром ВПВ (рис. 4) через її майже повну оклюзію на тлі основного процесу.
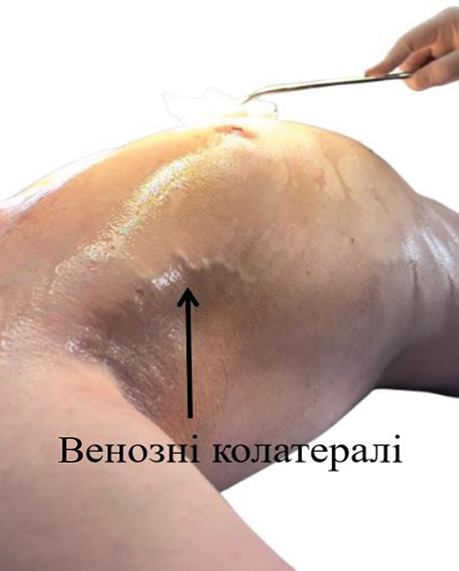
Рис. 4. Розвинені венозні колатералі як прояв синдрому ВПВ
У пацієнта, зважаючи на його кращий функціональний статус, розвиток післяопераційної пневмонії був менш очікуваним. Проте, беручи до уваги значну хірургічну травму, планувалося проведення подовженої ШВЛ. Через наявний синдром ВПВ застосування ТЕА, як і в попередньому випадку, було неможливим. З огляду на залучення у процес крупних судин передбачалася значна крововтрата.
Клінічні рішення у веденні цього пацієнта багато в чому були подібні до першого випадку. У цьому випадку пацієнту після операції також проводилася подовжена ШВЛ у режимі СPAP / PS, однак її тривалість була меншою (4 год). Аналгоседація забезпечувалася шляхом подовженої в/в інфузії пропофолу та реміфентанілу. Після екстубації інфузія реміфентанілу була подовжена ще на добу. Менеджмент крововтрати був аналогічний першому випадку.
Підсумовуючи результати лікування, протягом перших 4 год пацієнт перебував на подовженій ШВЛ з проведенням аналгоседацї, протягом доби після екстубації продовжувалася інфузія реміфентанілу, на 3-тю добу пацієнт був переведений до профільного відділення, на 15-ту — виписаний зі стаціонару.
КЛІНІЧНИЙ ВИПАДОК № 3
Пацієнт: чоловік, 68 років.
Діагноз: хондросаркома грудної стінки справа з поширенням на груднину, верхню частку правої легені.
Оперативне втручання: видалення пухлини грудної стінки з резекцією 1–3-го ребер справа, ручки та верхньої третини тіла груднини, верхньої частки правої легені, пластикою грудної стінки пропіленовою сіткою (рис. 5).
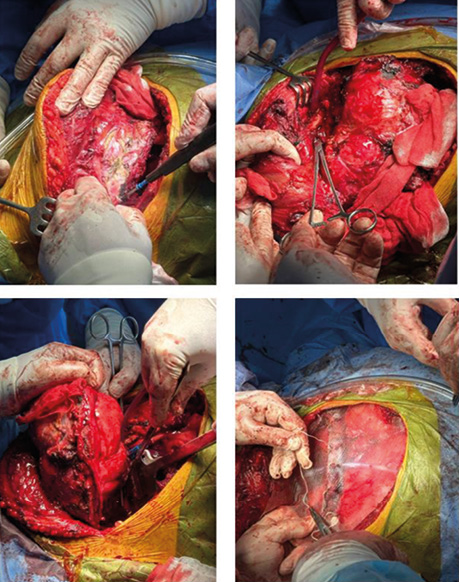
Рис. 5. Видалення пухлини грудної стінки
Хірургічний доступ: передньобокова торакотомія справа по 4-му міжребер’ю.
Крововтрата: 2200 мл.
Пацієнт мав супутню кардіальну патологію (фібриляцію передсердь (ФП)), хронічне обструктивне захворювання легень (ХОЗЛ) на тлі багаторічного паління.
У такого пацієнта, з огляду на значну хірургічну травму та ХОЗЛ, ми очікували розвиток післяопераційної пневмонії, планували проведення подовженої ШВЛ. Звертаючись до питання вибору методу знеболення, варто зазначити, що в цьому разі опція застосування ТЕА була технічно можливою, проте сумнівною в плані адекватного поширення місцевого анестетика та охоплення всієї хірургічної травми, а саме 1–3-го ребер, резекція яких мала відбутися (рис. 6).
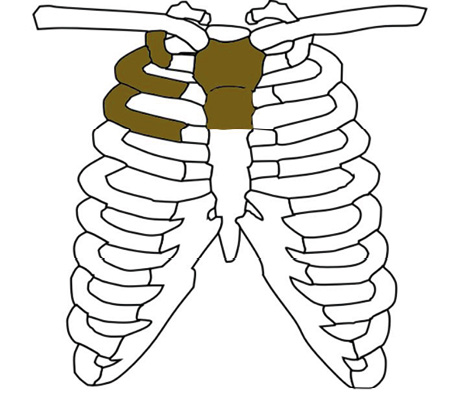
Рис. 6. Запланований об’єм резекції елементів каркасу грудної клітки
Клінічні рішення в менеджменті цього випадку були де в чому подібні до перших 2 випадків. Після завершення операції пацієнта було доправлено до ВАІТ для проведення подовженої ШВЛ у режимі СPAP / PS, яка тривала 5 год, виконували санаційні бронхоскопії з огляду на наявне у пацієнта ХОЗЛ. Аналгоседацію проводили із застосуванням пропофолу та реміфентанілу. ТЕА не застосовували протягом 1-ї доби з огляду на потребу у проведенні симпатоміметичної підтримки в перші години після операції та недоступність пацієнта продуктивному контакту через проведення ШВЛ та аналгоседації. Після екстубації, досягнення контакту з хворим та стабілізації показників гемодинаміки було розпочате застосування ТЕА, яка була абсолютна ефективна та забезпечувала адекватне знеболення всієї хірургічної рани.
Узагальнюючи, протягом перших 5 год пацієнт перебував на подовженій ШВЛ та отримував аналгоседацію у складі пропофолу з реміфентанілом. Подовжене в/в введення реміфентанілу тривало протягом 1-ї доби після операції. На 2-гу добу інфузія реміфентанілу була призупинена, натомість розпочато епідуральне знеболення. На 3-тю добу пацієнт був переведений до профільного відділення, на 17-ту — виписаний зі стаціонару.
КЛІНІЧНИЙ ВИПАДОК № 4
Пацієнт: дівчина, 14 років.
Діагноз: множинні паравертебральні нейрофіброми на рівні Th1-Th7 хребців з поширенням у грудну порожнину та праві відділи хребтового каналу (рис. 7).
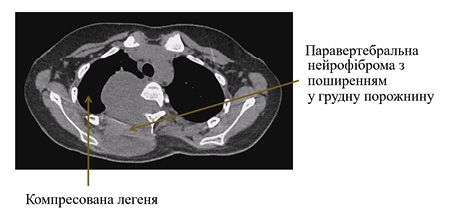
Рис. 7. Передопераційний знімок КТ, який демонструє ступінь компресії легені пухлиною
Оперативне втручання: видалення нейрофіброми на рівні Th1-Th7 хребців справа з транспедикулярною стабілізацією на рівні Th2-Th5 хребців, резекцією 3, 4, 5-го ребер справа, 1–2-го сегментів правої легені (рис. 8).
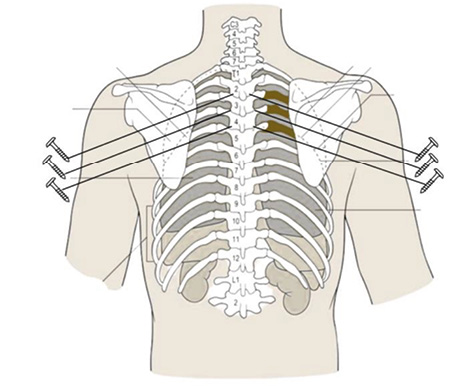
Рис. 8. Схема хірургічної травми
Хірургічний доступ: задня торакотомія справа.
Крововтрата: 1200 мл.
Як і в попередніх випадках, за даними візуалізаційних методів була наявна певна компресія легені пухлиною, тому існувала ймовірність розвитку післяопераційної пневмонії. Значна хірургічна травма та ризик розвитку післяопераційної пневмонії визначили необхідність у проведенні подовженої ШВЛ. Застосування ТЕА в цьому клінічному випадку не мало б сенсу через порушення цілісності епідурального простору при виконанні транспедикулярної стабілізації, ламінектомії.
Тактика ведення цієї пацієнтки в післяопераційний період включала проведення подовженої ШВЛ протягом 11 год із застосуванням аналгоседації у складі пропофолу, реміфентанілу, дексмедетомідину. Подовжена в/в інфузія реміфентанілу тривала протягом перших 36 год. Менеджмент крововтрати був подібний до такого в попередніх випадках.
Завдяки описаній вище тактиці на ранок 2-ї доби хвору було екстубовано, на 3-тю добу переведено до профільного відділення, на 16-ту — виписано зі стаціонару.
ОБГОВОРЕННЯ
Знеболення пацієнтів, яким виконуються високотравматичні торакальні операції зі значним пошкодженням каркасу грудної клітки, є складним викликом для анестезіолога. Ведення таких пацієнтів, зокрема забезпечення адекватного контролю над післяопераційним больовим синдромом, має бути персоналізованим.
Золотим стандартом регіонарної анестезії для торакальних операцій прийнято вважати ТЕА [4]. Проте можливість і доцільність її застосування зумовлена конкретною клінічною ситуацією. Так, в 1 і 2-му клінічних випадках опція проведення ТЕА була неможливою через наявний у пацієнтів синдром ВПВ. Цей синдром розвивається внаслідок тромботичної обструкції або зовнішньої компресії ВПВ, найчастіше пухлинами переднього середостіння. З метою забезпечення адекватного відтоку крові відбувається розвиток системи венозних колатералей у верхній половині тулуба [5]. У такому випадку не виключене розширення й вен епідурального венозного сплетення, кров по яких відтікає в систему ВПВ (рис. 9, 10) [6]. Тому при спробі встановлення епідурального катетера у пацієнтів із синдромом ВПВ існує високий ризик розвитку епідуральної гематоми.
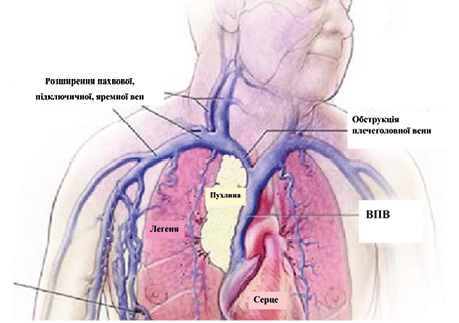
Рис. 9. Синдром ВПВ [5]
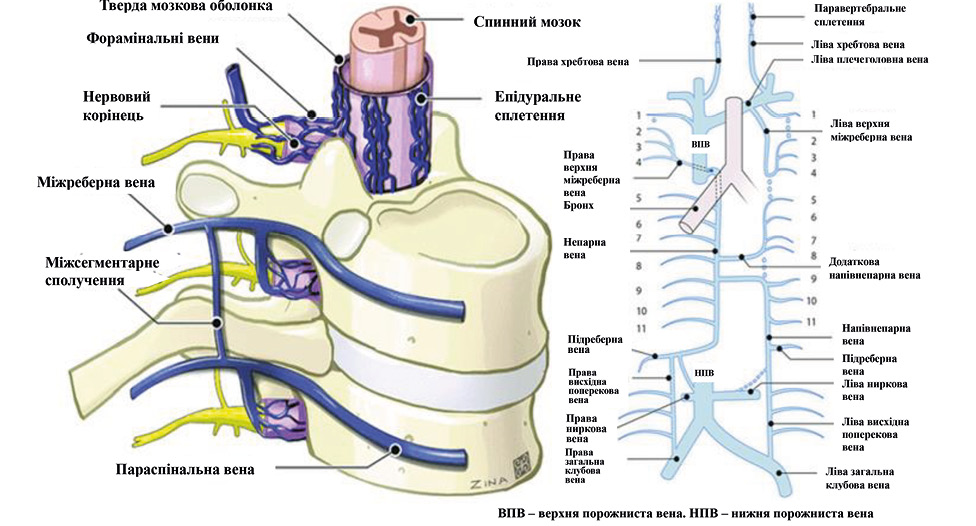
Рис. 10. Відтік крові від епідурального венозного сплетення [6]
Якщо в 1 і 2-му випадках відмова від ТЕА пов’язана із особливостями пацієнтів (синдромом ВПВ), то в клінічному випадку № 4 вона була зумовлена видом хірургічної травми (нейрохірургічний етап комбінованої операції — виконання транспедикулярної стабілізації, ламінектомії [7], що супроводжувалося порушенням цілісності епідурального простору). Покладатися лише на ТЕА як надійний метод післяопераційного знеболення не видається можливим у випадку, коли в післяопераційний період планується проведення ШВЛ та аналгоседація, адже в той часовий проміжок, коли пацієнт седований, оцінити інтенсивність больового синдрому може бути проблематично. Інша проблема — охоплення аналгетичним ефектом зони хірургічної рани у пацієнтів, яким виконують резекцію «верхніх» ребер, ключиці, ручки груднини тощо — в таких випадках ТЕА не завжди може забезпечити повноцінне знеболення всієї рани [8]. Але в тих випадках, коли застосування ТЕА можливе, цей метод може бути дуже допоміжним, особливо в контексті відлучення від ШВЛ та профілактики респіраторних ускладнень [9].
Спільними для всіх 4 випадків є проведення після операції подовженої ШВЛ в допоміжному режимі СPAP / PS від 4 до 18 год з огляду на велику хірургічну травму та можливий ризик розвитку післяопераційної пневмонії внаслідок компресії легені пухлиною та перебування легені в колабованому стані. У публікації S. Lampridis та співавт. [10] описано досвід проведення респіраторної підтримки у пацієнтів після операцій з резекції та реконструкції грудної клітки та наголошено на її важливості, адже респіраторні ускладнення є одними з найчастіших ускладнень після резекції та реконструкції грудної стінки і трапляються у 37% хворих, які перенесли такі операції. Таку високу частоту можна пояснити порушенням структурної цілісності грудної стінки, що може перешкоджати дихальній функції. Респіраторні ускладнення після резекції та реконструкції грудної стінки включають пневмонію (1,1–11,3%), гостру дихальну недостатність (2,3–5,4%), ателектаз, гострий респіраторний дистрес-синдром, тромбоемболію легеневої артерії, плевральний випіт та пневмоторакс.
Під час проведення подовженої ШВЛ пацієнтам проводилася аналгоседація, яка виконувала 2 функції: адаптацію до ШВЛ та аналгезію. Для забезпечення аналгоседації використовували подовжену в/в інфузію пропофолу в комбінації з фентанілом та мідазоламом у 1-му випадку та поєднано з реміфентанілом — в інших. У 2 випадках з представлених 4 подовжена в/в інфузія реміфентанілу (0,025–0,05 мкг/кг/хв) тривала і після екстубації пацієнтів для контролю над больовим синдромом. Досвід застосування реміфентанілу у незаінтубованих пацієнтів наведено в публікації R. Le Floch та співавт. [11]. Автори описують застосування реміфентанілу для знеболення пацієнтів з опіками під час заміни пов’язок. Перев’язки проводилися на тлі збереженого спонтанного дихання пацієнтів.
Поєднання допоміжної вентиляції з поверхневою аналгоседацією препаратами короткої дії дозволило здійснити відлучення від ШВЛ в максимально короткі терміни [12], а хороший контроль над больовим синдромом у перші 2 післяопераційні доби мінімізував респіраторні порушення, пов’язані з пошкодженням каркасу грудної стінки.
Зважаючи на результати лікування, можна стверджувати, що тактика стосовно ведення кожного пацієнта була адекватною та відповідала певній клінічній ситуації. Усі пацієнти були переведені з ВАІТ до профільного відділення на 3-тю добу, ніхто з них не перебував у стаціонарі більше ніж 3 тиж, незважаючи на величезну хірургічну травму.
ВИСНОВКИ
Торакальні операції, що супроводжуються високим травматизмом і значним пошкодженням каркасу грудної клітки, як ніякі інші, потребують адекватного якісного знеболення. Знеболення вищевказаних операцій з огляду на їхню специфіку має бути персоналізовано підібране під кожний клінічний випадок з урахуванням хірургічної травми та індивідуальних особливостей кожного пацієнта.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
1. Sugarbaker, D. J., Bueno, R., Burt, B. M., & Mentzer, S. J. (2015). Adult chest surgery (2nd ed.). New York (NY): McGraw-Hill Education.
2. Hamilton, C., Alfille, P., Mountjoy, J., & Bao, X. (2022). Regional anesthesia and acute perioperative pain management in thoracic surgery: a narrative review. Journal of Thoracic Disease, 14(6), 2276–2296. doi: 10.21037/jtd-21-1740.
3. Heybati, K., Xie, G., Deng, J., Walkey, A. J., Gajic, O., & Yadav, H. (2025). Hemodynamic Effects of Guideline-Based Sedation in Mechanically Ventilated Adults: A Multicenter Observational Analysis. Critical Care Explorations, 7(9), e1313. doi: 10.1097/CCE.0000000000001313.
4. Sarridou, D. G., Mouratoglou, S. A., Mitchell, J. B., Cox, F., Boutou, A., Braoudaki, M., … Walker, C. P. R. (2023). Post-Operative Thoracic Epidural Analgesia and Incidence of Major Complications according to Specific Safety Standardized Documentation: A Large Retrospective Dual Center Experience. Journal of Personalized Medicine, 13(12), 1672. doi: 10.3390/jpm13121672.
5. Wilson, L. D., Detterbeck, F. C., & Yahalom, J. (2007). Clinical practice. Superior vena cava syndrome with malignant causes. New England Journal of Medicine, 356(18), 1862–1869. doi: 10.1056/NEJMcp067190.
6. Borg, N., Cutsforth-Gregory, J., Oushy, S., Huynh, T., Savastano, L. E., Cloft, H. J., … Brinjikji, W. (2022). Anatomy of Spinal Venous Drainage for the Neurointerventionalist: From Puncture Site to Intervertebral Foramen. American Journal of Neuroradiology, 43(4), 517–525. doi: 10.3174/ajnr.A7409.
7. Shi, B., Zheng, X., Min, S., Zhou, Z., Ding, Z., & Jin, A. (2014). The morphology and clinical significance of the dorsal meningovertebra ligaments in the cervical epidural space. Spine Journal, 14(11), 2733–2739. doi: 10.1016/j.spinee.2014.04.014.
8. Visser, W. A., Liem, T. H., van Egmond, J., & Gielen, M. J. (1998). Extension of sensory blockade after thoracic epidural administration of a test dose of lidocaine at three different levels. Anesthesia & Analgesia, 86(2), 332–335. doi: 10.1097/00000539-199802000-00022.
9. Priestley, M. C., Cope, L., Halliwell, R., Gibson, P., Chard, R. B., Skinner, M., & Klineberg, P. L. (2002). Thoracic epidural anesthesia for cardiac surgery: the effects on tracheal intubation time and length of hospital stay. Anesthesia & Analgesia, 94(2), 275–282. doi: 10.1097/00000539-200202000-00009.
10. Lampridis, S., Minervini, F., & Scarci, M. (2024). Management of complications after chest wall resection and reconstruction: a narrative review. Journal of Thoracic Disease, 16(1), 737–749. doi: 10.21037/jtd-23-621.
11. Le Floch, R., Naux, E., Pilorget, A., & Arnould, J. F. (2006). Use of remifentanil for analgesia during dressing change in spontaneously breathing non-intubated burn patients. Annals of Burns and Fire Disasters, 19(3), 136–139.
12. Rozendaal, F. W., Spronk, P. E., Snellen, F. F., Schoen, A., van Zanten, A. R., Foudraine, N. A., … Bakker, J. (2009). UltiSAFE investigators. Remifentanil-propofol analgo-sedation shortens duration of ventilation and length of ICU stay compared to a conventional regimen: a centre randomised, cross-over, open-label study in the Netherlands. Intensive Care Medicine, 35(2), 291–298. doi: 10.1007/s00134-008-1328-9.
Адреса для листування:
Перконос Андрій
03022, Київ, вул. Здановської Юлії, 33/43
Державне некомерційне підприємство «Національний інститут раку»
E-mail: andre@protoka.kiev.ua
Correspondence:
Andrii Perkonos
33/43 Yulii Zdanovskoi str., Kyiv, 03022
Nonprofit Organization National Cancer Institute
E-mail: andre@protoka.kiev.ua














Leave a comment