Общие вопросы онкоурологии
Особенности диагностики и лечения опухолей надпочечников
А.Ю. Воропай
Харьковский областной клинический онкологический центр, Харьков, Украина
Внедрение в клиническую практику новых методов диагностики привело к выявлению большого количества гормонально неактивных, клинически «немых» опухолей надпочечников. Ведущую роль в диагностике занимает УЗИ, КТ, ЯМРТ и, конечно же, исследование гормонального фона. При этом нередко выявляются опухоли надпочечников злокачественной структуры. Отдельную проблему представляют вторичные опухоли надпочечников метастатического характера. В затруднительных случаях показана тонкоигольная биопсия.
Цель исследования — изучить диагностические особенности и лечебную тактику при опухолях надпочечников различной структуры.
В исследование включены больные с опухолями надпочечников. Использованы биохимические, ультразвуковые и рентгенологические методы исследования.
В клинике обследовано 12 больных с установленными опухолями надпочечников. 10 больным произведено оперативное лечение — адреналэктомию. У оставшихся 2 пациентов — метастатическое вторичное поражение из первичных очагов в легких и почке, причем у 1 — двустороннее. У 3 гистологически выявлена аденокарцинома, у остальных 7 — доброкачественные опухоли (у 6 — аденома, у 1 — феохромоцитома).
Выводы:
- для диагностики опухолей надпочечников используются УЗИ, КТ и/или ЯМРТ;
- обязательное изучение гормональной активности опухоли;
- гормональная активность не подтверждает и не исключает злокачественность;
- выполнение тонкоигольной биопсии позволяет исключить вторичное метастатическое поражение надпочечника и верифицировать диагноз.
Оптимизированные подходы в онкоурологии в лечении пациентов со скелетными осложнениями
К.В. Гаевой, Н.Я. Скиба, С.В. Гончар, В.Е. Литвиненко, А.В. Мокеев
Полтавский областной клинический онкологический диспансер, Полтава, Украина
Частота возникновения костных метастазов при раке предстательной железы (РПЖ) — 45–47%, раке мочевого пузыря (РМП) — 4%, раке почки (РП) — 20–25%. Основной проблемой в лечении костных метастазов в урологии для большинства врачей является то, что ключевым моментом для начала лечения выступает боль в костях, а профилактика скелетных осложнений не представляет собой побуждающий фактор для начала лечения, нет четкого понимания цели лечения и четких коммуникаций с пациентами на эту тему. Наиболее распространенными скелетными осложнениями в результате метастазирования являются патологические переломы и трещины костей, сдавление спинного мозга, гиперкальциемия на фоне злокачественных опухолей, болевой синдром. Роль бисфосфонатов в лечении костных метастазов — предупредить или отсрочить развитие скелетных осложнений, уменьшить выраженность болевого синдрома, улучшить качество жизни. Самое важное — сохранить больному автономность передвижения и бытовую независимость от других людей.
Цель исследования: оценка эффективности применения бисфосфонатов — памидроновой и золедроновой кислоты при лечении больных РПЖ, РМП, РП с впервые выявленными костными метастазами.
В исследование было включено 122 больных с костными метастазами. Больные были разделены на 2 группы. В 1-ю группу (n=93) вошли больные, которые получали памидроновую кислоту по 90 мг в/в 1 раз в 28 дней на протяжении 24 мес (повторные курсы при восстановлении боли в костях). Во 2-ю группу (n=29) вошли больные, которые получали лечение золедроновой кислотой по 4 мг в/в 1 раз в 28 дней на протяжении 24 мес, препараты кальция с витамином D. Терапия сопровождения для больных на РПЖ — бикалутамид по 50 мг в день, аналоги лютеинизирующего гормона рилизинг-гормона — трипторелин 3,75 мг в/м 1 раз в месяц или 11,25 мг 1 раз в 3 мес.
У больных, которые получали лечение памидроновой кислотой, не отмечалось значительного снижения интенсивности болевого синдрома и развития осложнений костных метастазов. У больных, которые получали золедроновую кислоту, отмечалась позитивная динамика, которая проявлялась значительным уменьшением выраженности болевого синдрома, нормализация уровня кальция крови (2,23–2,5), по результатам контрольной томографии и сцинтиграфии костей скелета отмечалось уменьшение деструкции в областях поражения. Также позитивным моментом является удобство и скорость введения, безопасность применения.
Золедроновая кислота является эффективным бисфосфонатом, который оказывает максимальное действие не только при остеолитических, но и при остеобластических метастазах, какие чаще всего образуются при опухолях урогенитального тракта. Золедроновая кислота значительно уменьшает количество костных осложнений у пациентов, продлевает время до появления первого костного осложнения, прогрессии костно-метастатической болезни, от чего зависит показатель качества жизни больных раком с костными метастазами.
Чрескожная нефростомия, малоинвазивный метод дренирования верхних мочевых путей у больных со злокачественными опухолями органов малого таза
Б.А. Дуда
Научно-исследовательский институт онкологии Республики Молдова, Кишинев, Республика Молдова
В последнее время в онкологии все чаще сталкиваются с проблемами пассажа мочи, возникающими при злокачественных опухолях органов малого таза (ЗООМТ), которые занимают одно из лидирующих мест в структуре онкологической заболеваемости и составляют в совокупности более 25%.
Своевременная диагностика и определение тактики лечения обструкции мочеточников у больных со ЗООМТ представляют собой одну из наиболее актуальных и нерешенных проблем в онкологии. Распространению рака на мочевую систему способствуют анатомическая близость органов малого таза и обилие лимфатических сосудов.
У больных со ЗООМТ в запущенных стадиях, таких как: рак шейки матки, рак тела матки, рак яичника, рак мочевого пузыря, рак предстательной железы, ректосигмоидальный рак, забрюшинные внеорганные опухоли с наличием метастатических изменений забрюшинных лимфатических узлов — стриктуры мочеточников могут протекать бессимптомно и зачастую приводят к выраженным функциональным и морфологическим изменениям стенки мочеточника и паренхимы почки, что вызывает развитие гидронефротической трансформации почки. Ее прогрессирование неизбежно приводит к необратимому снижению функции почки, хронической почечной недостаточности (ХПН), инвалидизации больных.
Единственными возможными в этой ситуации методами коррекции стенозов мочеточника, позволяющими продлить жизнь пациентов и улучшить ее качество, являются малоинвазивные способы дренирования верхних мочевых путей (ВМП). Наиболее распространенным методом является выполнение чрескожной пункционной нефростомии (ЧПНС).
Цель исследования — определить показания и эффективность ЧПНС у больных со ЗООМТ с обструкциями ВМП.
В Институте Онкологии в отделении урологии с 2006 по 2011 гг. было выполнено 124 нефростомии 97 пациентам с уретерогидронефрозом (УГН): левостороннюю — 28, правостороннюю — 42 и двустороннюю — 27 пациентам. Проведен клинический анализ больных с УГН по локализациям новообразований: шейки, тела матки и яичника — 30 (31,1%), мочевого пузыря — 43 (44,1%), предстательной железы — 6 (6,1%), прямой и сигмовидной кишки — 7 (7,2%), забрюшинные внеорганные опухоли с наличием метастатических измененных забрюшинных лимфатических узлов — 11 (11,3%), из которых с ятрогенной травмой мочеточника — 5 больных. Возраст пациентов составил от 20 до 80 лет (средний — 50 лет). Первичные — 32 (32,98%), вторичные — 65 (67,02%) больных.
Распределение больных с ЧПНС по стадиям: I стадия — 2, II стадия — 8, III стадия — 55, IV стадия — 32 больных. У 80 пациентов выявлена XПН, из них у 42 (43,29%) пациентов произведено дренирование ВМП по жизненным показателям в 1-й день госпитализации. Операцию проводили с помощью ультразвукового сканера КОМБИЗОН-320 с применением пункционной насадки. Функциональную способность почки изучали по клиренсу эндогенного креатинина и мочевины. Средний уровень мочевины при выявлении УГН в группе больных до ЧПНС составил 22,25 ммоль/л (от 3,5 до 81,9 ммоль/л), после операции медиана снизилась до 16,08 ммоль/л (от 2,9 до 66,3 ммоль/л). У 24 (24,76%) пациентов уровень мочевины снизился до нормы.
Средний уровень креатинина до ЧПНС составил 632,59 ммоль/л (от 74,4 до 2843,0 ммоль/л), после медиана снизилась до 340,19 ммоль/л (от 68,0 до 1492,06 ммоль/л). У 21 (21,46%) цифры снизились до нормы.
Мониторинг наблюдения больных после ЧПНС составил от 1 нед до 6,5 года.
Основными осложнениями были: профузное кровотечение — 15 (15,30%), паранефральная гематома — 2 (2,04%), лихорадка — 11 (11,44%), ренефростомия — 7 (7,14%) случаев. Замену нефростомического стента производили 1 раз в 3–4 мес. Клубочковая фильтрация и суточный диурез напрямую зависят от толщины паренхимы. У 34 больных с ХПН показатели мочевины и креатинина через 5–7 дней нормализовались, что позволило в последующем выполнить хирургические вмешательства у 10 больных, применить лучевую терапию у 12, химиолучевую — у 14 пациентов, в 7 случаях после лечения с удовлетворительным результатом удалось избавиться от нефростомы.
Применение методики ЧПНС показано при ЗООМТ и УГН с эффективностью 92,5%.
Пункционная нефростомия — эффективный, малоинвазивный метод дренирования ВМП с лечебной и диагностической целью выполняется под местным обезболиванием, и даже тяжелые пациенты хорошо переносят эту операцию.
Чрескожное дренирование гидронефротической почки позволяет не только ликвидировать ХПН, улучшая качество жизни пациента, но и предоставляет возможность провести хирургическое лечение либо химиолучевую терапию.
Организация ранней диагностики онкоурологических заболеваний в экспресс-диагностическом урологическом кабинете (ЭДУК)
В.Н. Журавлев, И.В. Баженов, А. Зырянов, А.В. Машковцев, О.В. Журавлев, И.В. Борзунов
Уральская Государственная медицинская академия, Свердловская областная клиническая больница №1, Екатеринбург, Россия
Онкоурологические заболевания являются одной из наиболее актуальных проблем современности из-за неуклонного роста количества больных как во всем мире, так и в нашей стране, в том числе и в Свердловской области. Решение этих проблем — задача не только медицинская, но и государственная, поскольку за ростом онкоурологических заболеваний следует рост инвалидизации и смертности населения.
В Свердловской области для решения проблем по ранней диагностике урологических и онкоурологических заболеваний была разработана программа «Урологическое здоровье мужчины», одобренная Губернатором Свердловской области и утвержденная специальным постановлением Правительства области. Данная программа позволила организовать, разместить и оснастить 11 экспресс-диагностических урологических кабинетов (ЭДУК) в наиболее крупных городах области. Основной целью Губернаторской программы «Урологическое здоровье мужчины» в Свердловской области является обеспечение гарантированного объема и качества медицинской помощи мужчинам в диагностике и лечении урологических заболеваний.
На фельдшерско-акушерском пункте был внедрен скрининг по ранней диагностике урологических заболеваний. Фельдшер проводил анкетирование мужчин в возрасте 50 лет и старше и выявлял группы риска по специально разработанной анкете. В дальнейшем данную группу пациентов направляли в ЭДУК, где выполнялись основные диагностические исследования: пальцевое ректальное исследование, УЗИ почек, мочевого пузыря, биопсия предстательной железы, цистоскопия, в ряде случаев внутривенная урография, компьютерная томография (КТ) органов малого таза. Сцинтиграфия костей скелета и биопсия предстательной железы выполнялись при повышенных цифрах простатспецифического антигена.
Цель исследования — оценить влияние данной программы на раннее выявление онкоурологических заболеваний и результаты лечебно-диагностических мероприятий.
С момента начала работы ЭДУК в г. Первоуральске с 1.04.2006 г. из 36 745 обследованных пациентов у 29 693 (80,8%) выявлены урологические заболевания. Онкоурологические заболевания выявлены у 4287 (14,4%) обследуемых, из них наиболее частыми были рак предстательной железы — у 2576 (8,6%), рак мочевого пузыря — у 916 (3,1%), рак почки — у 795 (2,7%) больных. Выявляемость в ЭДУК онкоурологических заболеваний на ранних стадиях: рак предстательной железы в стадии Т1-Т2 в 1999 г. — 26,8%, а в 2008 г. — 56,3%, рак мочевого пузыря — 33,8 и 54,9%, рак почки — 34,6 и 53,% соответственно.
Следовательно, организация специализированной урологической помощи с созданием ЭДУК обеспечивает доступность обследования по месту жительства и диагностику онкоурологических заболеваний на ранних стадиях развития, что позволяет значительно улучшить результаты лечения и повысить качество жизни больных.
Роль рецепторного аппарата калликреин-кининовой системы в пролиферативных процессах предстательной железы
М.И. Коган1, М.Б. Чибичян1, А.В. Ильяш1, А.Э. Мационис2, П.Э. Повилайтите2
1НИИ урологии «Ростовский государственный медицинский университет, Россия
2РОПАБ, Ростов-на-Дону, Россия
Известно, что компоненты регуляторных систем, в частности калликреин-кининовой системы (ККС), играют важную роль в контроле морфогенеза клеток, неоангиогенеза, злокачественного роста и других патологических состояний, в том числе и в ткани предстательной железы. Основной эффектор ККС — брадикинин — оказывает свое действие через В-кининовые рецепторы 2 типов — В1 и В2. Выяснение особенностей кинин-связанных процессов в ткани предстательной железы при ее раке и доброкачественной гиперплазии представляется перспективным, притом что работ, посвященных роли рецептора В2 в пролиферативных процессах в простате, мало.
Цель работы — изучение роли брадикинина как ключевого эффектора ККС, действующего через рецепторы В1 и В2 в ткани простаты при доброкачественной гиперплазии предстательной железы (ДГПЖ) и раке предстательной железы (РПЖ).
Исследован материал полифокальных пункционных биопсий простаты 15 мужчин с РПЖ (Т2 — у 6 пациентов, Т?3 — 9 пациентов) (средний возраст 69,7±7,52 года), простатспецифический антиген — 7,38±3,1 нг/мл и 15 мужчин с ДГПЖ (средний возраст 66,7±8,53 года). Иммуногистохимические реакции проводили в автоматическом роботизированном аппарате для постановки иммуногистохимических реакций DakoAutostainer Plus по стандартному протоколу. Использовали набор первичных антител: Bradykinin B1 Receptor (BDKRB1), rabbit polyclonal, 1:100 (Abcam), Bradykinin B2 Receptor (BDKRB2), rabbit polyclonal, 1:1000 (Abcam).
При ДГПЖ экспрессия В1 в железистых клетках полностью отсутствовала. Специфическая реакция с анти-В1 антителами в железистом эпителии имеет место только в малигнизированных ацинусах и фокусах ПИН. Локализация рецептора В1 — цитоплазматическая, в апикальной части клеток. Иммуноокрашивание с анти-В2 антителами в группе РПЖ выявляет экспрессию их преимущественно в строме ткани предстательной железы как при ДГПЖ, так и при РПЖ. Не обнаружено изменения экспрессии В2 в строме низкодифференцированных карцином. Окрашивание выявляется во всех случаях РПЖ, его интенсивность одинакова.
Рецепторы В1 доминируют на мембране эпителиоцитов при РПЖ, а В2 обнаруживаются в строме. Это указывает на наличие функционально активной ККС в ткани РПЖ, эффекторное воздействие которой на строму и эпителий осуществляется через разные типы рецепторов. При ДГПЖ в железистом эпителии отсутствует экспрессия В1, тогда как В2 локализован в строме и хорошо выявляется. Данные о характере экспрессии В1 свидетельствуют о возможности использовать его как маркер РПЖ.
ТУР цистоуретрального сегмента как этап радикальной нефруретерэктомии при папиллярных новообразованиях почки
Ф.И. Костев, Д.Ф. Тучин, В.М. Ходос, Р.А. Лунев, А.Н. Зачеславский
Урологическая клиника ГКБ № 10, Одесса, Украина
Оперативное лечение больных папиллярными опухолями лоханки почки включает в себя выполнение хирургического вмешательства, состоящего из двух разрезов для нефрэктомии и резекции мочевого пузыря. Внедрение современных хирургических технологий позволило изменить принципы лечения больных.
Цель исследования — обосновать эффективность трансуретральной резекции (ТУР) цистуретерального сегмента как этапа радикальной нефруретерэктомии, обеспечивающего малотравматичность и сокращение продолжительности операции и анестезии у больных с папиллярными новообразованиями почек.
Под нашим наблюдением находились 9 пациентов в возрасте от 52 до 73 лет с папиллярными опухолями лоханок почек, которым была выполнена нефруретерэктомия (8 пациентам — открытая и 1 — лапароскопическая) в сочетании с эндоскопической ТУР стенки мочевого пузыря, устья и мочеточника. В начале было проведено открытую нефруретерэктомию с мобилизацией нижней части мочеточника. Последний пересекался на уровне подвздошных сосудов, производилась катетеризация дистального отдела и фиксация мочеточника к катетеру. Затем, в положении Тренделенбурга, вводили цистоскоп и извлекали наружу дистальный конец мочеточникового катетера. После чего резектоскопом и крючковидным электродом в радиусе 1,5 см от устья производили круговое сквозное рассечение стенки мочевого пузыря. Подтягивая за катетер, петлевым электродом очищали мочеточник от окружающих тканей и удаляли последний. Мочевой пузырь дренировали катетером Foley. Затем больного укладывали в положение для люмботомии, подводили дренаж к месту перфорации мочевого пузыря и ушивали рану поясничной области.
В одном наблюдении в связи с выполнением лапароскопической нефруретерэктомии операцию начинали с эндоскопического этапа. Крючковидным электродом рассекалась стенка мочевого пузыря в радиусе 1,5 см от устья, мобилизовали мочеточник и последний удаляли лапароскопически единым блоком с почкой. Дренировали мочевой пузырь по уретре на протяжении 6–7 суток.
Эндоскопическая резекция стенки мочевого пузыря, устья и мочеточника сокращает время операции, избавляет от достаточно травматичного дополнительного доступа к терминальному отделу мочеточника. Время эндоскопического этапа составило 25–45 мин. Осложнений, связанных с эндоскопической резекцией мочевого пузыря, в послеоперационный период не отмечали. Мониторинг пациентов в сроки от 3 мес до 4 лет не выявил рецидивов заболевания.
Лечение герминогенных опухолей у мужчин за период 1998–2011 гг.
С.Л. Матвийчук , И.П. Ерко, В.Н. Зотов, Р.К. Цисельский
Областной онкологический диспансер, Чернигов, Украина
Опухоли яичка составляют 0,5–3% всех новообразований у мужчин. Чаще всего они встречаются в возрасте 20–40 лет. Герминогенные опухоли характеризуются быстрым ростом и очень агрессивным течением. Только у 30% больных могут излечиться при помощи хирургического вмешательства.
За период с 1998 по 2011 годы в отделении химиотерапии пролечено 79 больных семиномой и 66 больных несеминомными герминогенными опухолями, которые ранее не получали химиотерапию.
Следует отметить, что 48 пациентов (33,1%) ранее были прооперированы в других лечебных учреждениях области. Оценка прогноза течения заболевания у этой группы больных весьма сомнительна. Так из 48 пациентов 31 (64,5%) госпитализировано в отделение химиотерапии с распространением процесса на протяжении первого года после оперативного вмешательства.
В лечении больных с герминогенными опухолями мы придерживались следующей тактики. На первом этапе с диагностической и лечебной целью выполнялась орхофуникулэктомия. Для определения распространенности процесса все больные подвергались рентгенологическому исследованию органов грудной клетки и сонографии органов брюшной полости, при необходимости эти методы исследования дополнялись компьютерной томографией. До и после хирургического вмешательства проводились исследования сывороточных опухолевых маркеров: альфа-фетопротеин (АФП), хорионический гонадотропин (ХГ) и лактатдегидрогеназа (ЛДГ).
Прогноз протекания заболевания определялся по классификации IGCCCG.
Больным проводилось 4 курса химиотерапии комбинацией PEB.
В ходе исследования нами было установлено, что у большинства больных была тестикулярная локализация опухоли, что составило 94,8%. Обращает на себя внимание тот факт, что значительная часть пациентов с семиномой (93,1%), в отличие от пациентов с несеминомами (44,5%), относятся к группе с хорошим прогнозом, что отображает более благоприятное течение этого заболевания.
Медиана срока наблюдения на конец 2011 года за группой больных семиномой составляет 88,4 мес (6–144 мес), а группа больных несеминомными опухолями составляет 64,2 мес (8–112 мес).
Лечение больных с герминогенными опухолями яичка должно проводиться исключительно в условиях онкологического учреждения, так как это дает возможность оптимально установить прогноз течения болезни, обеспечить комплексный подход к лечению такой категории больных и соответственно улучшить сроки их выживания.
Анализ качества жизни больных после традиционной и лапароскопической эпинефрэктомии
Д.Н. Матюшко, В.А. Земляницына
Областная клиническая больница, Областной онкологический диспансер, Карагандинский государственный медицинский университет, Караганда, Казахстан
Качество жизни — относительно новое социально-медицинское понятие-критерий, включающее в себя не только состояние здоровья человека, но и его ощущения социального, физического и духовного благополучия. До настоящего времени в отечественной и зарубежной литературе не встречалась оценка хирургических способов лечения опухолей надпочечников по данному критерию.
Цель исследования — произвести сравнительный анализ качества жизни пациентов через 1 мес после выполнения им эпинефрэктомии традиционным и лапароскопическим методами.
Материалом исследования явились результаты лечения 30 больных, оперированных по поводу опухолей надпочечников в Областной клинической больнице и Областном онкологическом диспансере г. Караганды с 1998 по 2012 годы. Основная группа — 15 больных, оперированных лапароскопическим методом. Группу сравнения составили 15 больных, оперированных традиционными доступами (люмботомия, верхняя срединная лапаротомия). Группы по возрастному и половому составу, локализации (справа/слева) и морфологической форме опухоли сопоставимы.
Анализ качества жизни проводился через 1 мес после операции путем анкетирования больных с помощью опросника SF-36. Данный опросник содержит ряд вопросов, ответы к которым в совокупности составляют тот или иной критерий качества жизни (ФФ — физическое функционирование, РФФ — ролевое физическое функционирование, Б — интенсивность боли, ОЗ — общее состояние здоровья, Ж — жизненная активность, СФ — социальное функционирование, РЭФ — ролевое эмоциональное функционирование, ПЗ — психическое здоровье). Каждый критерий оценивается по 100-бальной шкале. Чем ближе результат к нулю, тем он хуже; чем выше и ближе к 100, тем качество критерия выше.
Анализ показателей качества жизни у пациентов основной группы, перенесших лапароскопическую эпинефрэктомию, выявил более значительное улучшение качества жизни по всем шкалам (рисунок). При этом статистически достоверные различия (p<0,05) получены по показателям общего и ролевого физического функционирования (увеличение величины показателей в 2,5 и 1,9 раза соответственно), социального функционирования и интенсивности боли (увеличение величины обоих показателей в 2,0 раза).
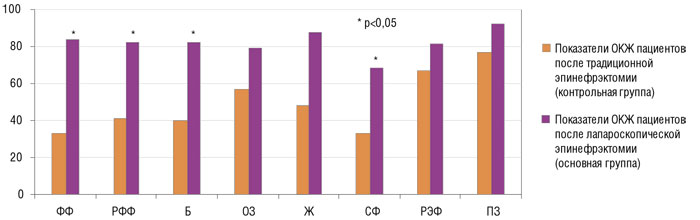
Описанные выраженные различия и значительная позитивная динамика в уровне качества жизни пациентов после лапароскопической эпинефрэктомии свидетельствуют о высокой эффективности данного метода не только по объективным критериям, но и в восприятии самого пациента, улучшение качества жизни которого является одной из самых важных задач в лечении любого заболевания.
Особенности подготовки и лечения больных с опухолями надпочечников
Н.С. Нургалиев, Б.Т. Онгарбаев
КазНИИОиР, отделение онкоурологии, Алматы,
Республика Казахстан
Опухоли надпочечников — относительно редкие заболевания, составляющие не более 0,6% от всех злокачественных новообразований. В большинстве случаев эти новообразования являются исходящими либо из коркового, либо из мозгового слоя опухолями. Иногда эти образования являются метастазами опухолей другой локализации. Известно, что большинство опухолей надпочечников сопровождается артериальной гипертонией, нередко злокачественного характера, исчезающей после удаления опухоли. В этой связи проблема опухоли надпочечников, помимо ее онкологической направленности, приобретает совершенно новое значение, так как гипертония, являясь одним из ранних проявлений опухолевого страдания, должна учитываться для ранней диагностики новообразования.
Основным методом лечения опухолей надпочечников в настоящее время является хирургический. Успех хирургического лечения во многом зависит от предоперационной подготовки, адекватности обезболивания, правильности ведения послеоперационного периода. Предоперационную подготовку следует проводить с учетом степени гормональной активности опухоли, проявлений заболевания, его осложнений и сопутствующей патологии. Обязательным является исследование уровня гормонов надпочечников — минерало-, глюкокортикоидов, кортикостероидов. В предоперационный период с целью коррекции состояния, в процессе ведения больного во время операции и в послеоперационный период необходимо координировать действия эндокринологов-терапевтов, урологов (хирургов) и анестезиологов.
Радикальным методом лечения является удаление опухоли (надпочечника), при необходимости с последующей заместительной терапией глюко-, минералокортикоидами. Во время операции при гормонально-активных опухолях можно столкнуться с различными трудностями. Как правило, на начальном этапе ревизии и выделения надпочечника происходит массивный выброс гормонов, сопровождающийся тахикардией и гипертензией (частота сердечных сокращений повышается до 100–150 ударов в минуту, систолическое АД — до 200–280 мм.рт.ст.), в связи с чем для уменьшения нежелательных последствий необходимо использовать «управляемую гипотонию» — инфузию растворов нитроглицерина, азаметония бромида и др. Необходимо стремиться быстрее перевязать основную вену надпочечника. Наоборот, после удаления железы наблюдается резкое снижение гемодинамики, что требует дополнительного введения гормональных средств (дексаметазон, адреналин), фенилэфрина, декстрана.
В нашей клинике с 2006 года прооперировано 17 больных с опухолями надпочечников, в 5 случаях из которых гистологически выявлена аденома надпочечника, в остальных — рак (в 1 случае — метастазы рака легкого в надпочечник). Исходя из нашего небольшого опыта, можем сделать следующее заключение: 1) обязательными являются осмотр эндокринолога для решения вопроса о необходимости операции на данном этапе и коррекция гормонального статуса предоперационного и послеоперационного периода; 2) необходимы осмотр больного анестезиологом для подготовки к операции, а также предоставление возможности подготовиться самому анестезиологу к вероятным скачкам АД во время операции; 3) нужно стремиться максимально раньше перевязать основную надпочечниковую вену. На наш взгляд, при наличии достаточно квалифицированной службы анестезиологии-реаниматологии подобные операции могут с успехом быть выполнены.
Ошибки в диагностике первично-множественных синхронных злокачественных новообразований мочеполовой системы
Т.Н. Попова
ГБОУ ВПО Саратовский ГМУ им. В.И. Разумовского Минздравсоцразвития РФ, Саратов, Россия
Первично-множественные злокачественные новообразования мочеполовой системы составляют 5,2–13,4% от всех злокачественных новообразований данной локализации. Синхронные опухоли имеют место у 18,2–48,7% больных с полинеоплазиями мочевыделительных органов. На фоне роста заболеваемости солитарными злокачественными новообразованиями растет число больных с полинеоплазиями. Но до настоящего времени не разработана система диагностики первично-множественных синхронных злокачественных новообразований (ПМСЗН), поэтому вторая опухоль выявляется поздно и часто в запущенной стадии.
Цель исследования: повышение эффективности диагностики при ПМСЗН мочеполовой системы.
Проанализированы истории болезни 91 больного с ПМСЗН мочеполовой системы. Мужчин — 72 (79,1±4,3%) — было больше (р<0,01), чем женщин — 19 (20,9±4,3%). Средний возраст мужчин составил 61,0±1,3 года, женщин — 63,7±1,9.
2 опухоли были выявлены у 90 (98,9±1,1%), 3 — у 1 (1,1±1,1%) пациента. Всего 183 новообразования. Из них 116 опухолей локализовались в мочеполовой системе, а 67 — вне ее.
Чаще всего была поражена почка (37,9±4,5%), несколько реже — мочевой пузырь (33,6±4,4%), гораздо реже — предстательная железа (19,8±3,7%).
У большинства больных при локализации одной опухоли в предстательной железе (60,9±10,2%), в мочевом пузыре (53,9±7,6%) и реже в почке (20,9±6,2%) вторая опухоль располагалась в пределах той же системы.
Почти у половины больных (49,3±6,1%) вторые опухоли локализовались в пищеварительной системе: в желудке, прямой и ободочной кишке. Значительно реже — в легком (16,4±4,5%) и на коже (14,9±4,4%).
При диагностике ПМСЗН мочеполовой системы вторая опухоль у большинства больных (71,1±4,8%) была выявлена в процессе обследования по поводу первой опухоли, у 24,5±4,5% пациентов — после лечения первой опухоли и у 4,4±2,2% — во время хирургического вмешательства. То есть почти у каждого третьего больного вторая опухоль при обследовании была пропущена.
Диагностическая ошибка была допущена у 20 (22,2±4,4%) больных ПМСЗН мочеполовой системы. При обследовании не было диагностировано 16 (22,5±5,0%) опухолей, расположенных в мочеполовой системе (мочевом пузыре, почке, предстательной железе, уретре, яичках), и 4 (21,1±9,4%) неоплазии, расположенные вне ее (желудок, полость рта, прямая кишка, яичники). 88,9±7,4% опухолей имели внутреннюю локализацию, а 11,1±7,4% — наружную.
Выводы:
1. При диагностике ПМСЗН мочеполовой системы вторая опухоль пропускается почти у каждого третьего больного.
2. Для своевременной диагностики ПМСЗН мочеполовой системы при обнаружении одной опухоли следует обследовать всю систему, так как у большинства больных вторая опухоль локализуется в этой же системе.
3. Почти у половины больных ПМСЗН мочеполовой системы вторые опухоли обнаружены в желудочно-кишечном тракте, что диктует необходимость исследовать желудок и толстую кишку при наличии опухоли в мочеполовой системе.
Трудности дифференциальной диагностики изолированного туберкулеза и опухолей семенного канатика. Особенности оперативного лечения
И.М. Русинко, Е.А. Квятковский, Н.М. Русинко, М.В. Челпанова
КЗ «Д 12 ТМО» ДОС, ГКБ №9, Днепропетровск, Украина
Туберкулез семенного канатика относится к очень редким заболеваниям. В доступной литературе описаны 27 случаев изолированного туберкулеза семенного канатика (R. Martiniello et al., 1984, S. Vamasaki et al., 1996, M. Tanaka et al., 2002 и др.). Во всех случаях была выполнена орхофуникулэктомия по поводу опухоли. Во всех случаях гистологически был диагностирован туберкулез семенного канатика при неизмененном яичке и его придатке.
Опухоли семенного канатика встречаются крайне редко у мужчин любого возраста и разделяются на доброкачественные и злокачественные. Они развиваются из оболочек семенного канатика, соединительной и жировой тканей, расположенных между его элементами. Существуют и метастатические опухоли семенного канатика. Чаще всего это метастазы предстательной железы. Одним из первых симптомов опухолей семенного канатика является появление безболезненного уплотнения по ходу семенного канатика. По мере роста опухоли появляется ноющая боль, чувство тяжести и дискомфорта в мошонке.
В нашей практике мы наблюдали 2 случая изолированного туберкулеза семенного канатика «симулирующих» опухолевидное образование. Пациент 32 лет обратился за медицинской помощью через 6 мес с момента обнаружения им образования в правом семенном канатике, которое последние 2 нед начало причинять беспокойство. При УЗИ было выявлено анэхогенное образование размерами 23?13?12 мм с положительным симптомом усиления его дистальной стенки, что характерно для кисты. При пальпации в дистальной части правого семенного канатика было обнаружено болезненное образование эллипсоидной формы, плотной консистенции, спаянное с семенным канатиком.
Во время операции после рассечения влагалищной оболочки яичка и семенного канатика у пациента было выявлено опухолевидное образование интимно спаянное с сосудами яичка. После пережатия сосудов яичка дистальнее образования яичко оставалось макроскопически жизнеспособным, что можно объяснить развитием коллатерального кровотока по сосудам оболочек яичка и семявыносящего протока. Последний был не изменен и сохранен во время операции. Яичковые сосуды проксимальнее и дистальнее образования были пересечены, культи их лигированы. Удаленные образования на разрезе серого цвета с однородной структурой. При гистологическом исследовании в образовании выявлен воспалительный процесс туберкулезной этиологии. Других туберкулезных очагов у пациента не обнаружено. Аналогичный случай мы наблюдали у пациента 56 лет с единственным левым яичком. Благодаря сохранению сосудов оболочек яичка и семявыносящего протока, яички остались жизнеспособными, что было подтверждено ультразвуковой цветовой допплерографией интраорганных сосудов яичек через 6 мес, 1 год, 2 и 3 года после операции.
Литературные и наши данные должны нацелить урологов и сонологов на диагностику данной патологии, что будет способствовать выявлению туберкулеза семенного канатика и его лечению путем выполнения органосохраняющих операций с дальнейшим лечением у фтизиоуролога. Применение цветовой допплерографии интраорганных сосудов яичка в пред- и послеоперационный период способствует выработке правильной тактики оперативного лечения и объективизации при динамическом наблюдении за пациентом после операции.
Частое выявление тератомы в резидуальной опухоли у больных метастатическими несеминомными опухолями яичка с полной ремиссией после химиотерапии
А.В. Сакало, В.В. Мрачковский, В.В., Кондратенко, Ю.Ю. Куранов, О.А.Черниченко, П.М. Салий, Я.В. Левчишин, Ю.В. Жилюк
ДУ «Институт урологии НАМН Украины», Киевский городской клинический онкологический центр, Киев, Украина
После химиотерапевтического лечения метастатических несеминомных опухолей яичка (НСОЯ) в случае отсутствия резидуальной опухоли на КТ рекомендуется тактика только наблюдения.
Целью исследования было изучить гистологическое строение и отдаленные результаты забрюшинной лимфаденэктомии (ЗЛАЭ) у больных с НСОЯ с полной клинической ремиссией после химиотерапии (ХТ).
С 1990 по 2010 гг. выполнена трансабдоминальная ЗЛАЭ у 82 больных НСОЯ с регионарными метастазами. Согласно IGCCCG-классификации благоприятный прогноз был у 69 (85%) и промежуточный/плохой у 13 (15%) больных. Размеры регионарных метастазов до ХТ были: <2 см — у 32 (40%), 2–5 см — у 37 (34%) и >5 см — у 13 (15%) пациентов соответственно. Проводили от 2 до 5 курсов индуционной ХТ на основе платины (ВЕР или ЕР).
Средний размер забрюшинных метастазов после лечения составил 0,5 см (колебания от 0 до 0,8 см). Жизнеспособная опухоль в резидуальной ткани после ХТ выявлена у 5 (6%) и тератома у 34 (47%) больных. Средний безрецидивный период наблюдения составил 96%.
Результаты наблюдения свидетельствуют, что у значительного процента больных в резидуальной ткани в забрюшинной области сохраняется жизнеспособная опухоль или тератома, несмотря на отсутствие патологических находок на КТ после индукционной ХТ.
Наличие жизнеспособной опухоли или тератомы и высокий процент (96%) безрецидивной выживаемости подтверждают необходимость выполнения постхимиотерапевтической ЗЛАЭ как интегральной части мультидисциплинарного ведения таких больных.
Выбор метода дренирования при инфраренальной обструкции опухолевой этиологии
С.В. Шкодкин, Ю.Б. Идашкин
Белгородская областная клиническая больница Святителя Иоасафа, Белгород, Россия
Частота выявления местно-распространенного генитального, колоректального рака, опухолей мочевого пузыря и предстательной железы, сопровождающихся инфраренальной обструкцией с развитием уретерогидронефроза не имеет тенденции к снижению (Б.П. Матвеев, 2011). Малоинвазивные технологии в последнее время занимают основное место в лечении данной категории пациентов (О.В. Теодорович, 2007).
За период 2005–2012 гг. нами наблюдались 13 пациентов с уретерогидронефрозом опухолевой этиологии. Показаниями к дренированию были острая почечная недостаточность и острый обструктивный пиелонефрит. Всего дренирование проведено на 21 почке.
У 7 пациентов этой группы предпринята попытка установки внутреннего дренажа (всего 11 почек). В 5 случаях (45,5%) установить стент технически не удалось, еще в 2 случаях (18,1%) отмечена неудовлетворительная функция стента (сохранялась клиника острого обструктивного пиелонефрита), что потребовало выполнения наружного дренирования. Чрескожная пункционная нефростомия (ЧПНС) под комбинированным УЗИ и рентген-контролем выполнена первично у 6 пациентов, дренировано 10 почек и после неудачи при постановки внутреннего стента —7 почек. Технических проблем при установке нефростомического дренажа отмечено не было. На фоне наружного дренирования зарегистрирован быстрый регресс воспалительных изменений и азотемии. Лихорадочный период составил 2,8±1,2 сут, умеренная гематурия без сгустков отмечена на протяжении 1,6±0,21 сут. У одного пациента (5,9%) наблюдалась миграция нефростомического дренажа на 2-е сутки, выполнена повторная ЧПНС. У всех пациетов с внутренними мочеточниковыми стентами сохранялась гематурия различной интенсивности на протяжении всего периода госпитализации.
Таким образом, ЧПНС является безопасным и эффективным способом дренирования почки при обструкции опухолевой этиологии.
Необходимо дополнительное исследование качества жизни и состояние почечной функции у данной категории пациентов в зависимости от способов дренирования в отдаленные сроки наблюдения.
Видеофиксация как фактор совершенствования лапароскопической техники в онкоурологии
П.Г. Яковлев1, В.В. Мрачковский1, В.С. Сакало2, А.В. Кондратенко1, Ю.Ю. Куранов1, П.Н. Салий1,
Я.В. Левчишин1, А.В. Сакало2
1Киевский городской клинический онкологический центр, Украина
2ГУ «Институт урологии НАМНУ», Киев, Украина
Лапароскопическая техника оперирования имеет важную отличительную особенность по сравнению с конвенциальной хирургией — возможность трансляции изображения операционного поля на экран монитора лапароскопической стойки. Это позволяет выполнять видеофиксацию хода операции, чтобы послеоперационно проанализировать ее с точки зрения эффективности хирургических маневров на этапе совершенствования хирургической техники, увидеть тактические ошибки, повторяющиеся движения как пример неэффективного использования времени операции. Такой анализ позволяет проводить последующие операции более рационально, что будет отражаться на сокращении времени операции.
Цель исследования — оценить эффект от использования видеофиксации хода операции для оптимизации лапароскопического оперирования, продемонстрировать допущенные ошибки, которые были выявлены с помощью видеофиксации.
С ноября 2009 по февраль 2012 гг. в отделении урологии Киевского городского клинического онкологического центра было проведено 22 лапароскопические нефруретерэктомии при раке почки или верхних мочевыводящих путей. Операции проводились с использованием видео- и электрохирургической аппаратуры фирмы «Olympus», видеозахват цифрового видеосигнала осуществлялся с помощью системы Pinnacle Video Transfer. Конверсия в открытый доступ была применена в одном случае кровотечения при травме селезенки.
Среди оперированных было 13 мужчин и 9 женщин, средний возраст которых составлял 55,3 года (49–78 лет). Индекс массы тела (ИМТ) составил в среднем 26,3±4,9 кг/м2 (20,7–39,1 кг/м2). Длительность операции составляла в среднем 305 мин (201–360 мин) и была больше у пациентов с более высоким ИМТ. При просмотре записи операций были выявлены следующие недостатки хирургической техники: неадекватный конституции пациента выбор мест для установки портов, что не обеспечивало эргономичность работы хирурга, недостаточно прецизионная диссекция сосудов ворот почки, надпочечника и верхнего полюса левой почки.
Ретроспективный анализ хода проведенной операции способствует фиксации технических неточностей и ошибок, допускаемых хирургом во время операции, что позволит исключить их при следующей операции. Главными аспектами, на которые надо обращать внимание при проведении лапароскопической нефрэктомии, являются: 1) тщательный отбор пациентов для операции с учетом стадии и распространенности опухолевого процесса; 2) установка портов в соответствии с конституцией больного и количеством подкожного и внутреннего жира для обеспечения эргономичности движений рук хирурга; 3) проведение прецизионной диссекции тканей в воротах почки, надпочечника и капсулы селезенки, что обеспечит работу в сухом поле и предотвратит кровотечения, ликвидация которых значительно удлиняет время операции.
Видеофиксация хода операции является ценным инструментом совершенствования навыков лапароскопического хирурга; позволяет ретроспективно проанализировать ход вмешательства и допущенные технические ошибки, что сокращает длительность последующих операций.
Microsatellite instability and allelic imbalance in papillary renal cell carcinoma as potential molecular genetic markers
D.S. Mikhaylenko1,2,3, L.V. Moskvina4, Y.Y. Andreeva4, А.Е. Mikhalchenko5, D.V. Zaletayev1,2,3
1Research Centre for Medical Genetics RAMS, Moscow, Russia
2Institute of Molecular Medicine of the Sechenov First Moscow Medical University, Moscow, Russia
3Medical-Biological Faculty of the Pirogov Russian Research Medical University, Moscow, Russia
4Hertzen Moscow Research Oncological Institute, Moscow, Russia
5Faculty of Bioengineering and Bioinformatics of the Lomonosov Moscow State University, Moscow, Russia
Renal cancer is one of 10 most common adult malignancies, however, the panels of protein and DNA-markers for laboratory diagnostics and prognosis are still to be developed. Data about cytogenetic and molecular genetic alterations mainly refer to the most frequent form of renal cancer — clear cell carcinoma that includes 80% of cases. Papillary carcinoma (second major type: 15% of cases) is less studied than clear cell tumors, therefore search of genetic abnormalities with diagnostic and prognostic characteristics in papillary carcinoma is particularly actual. For instance, there is lack of data about the frequency of microsatellite instability (MSI) in papillary renal cancer (PRC), where as this alteration is frequent in some other malignant tumor types and is associated with poor prognosis. At the same time, it was shown by other authors that duplication of 1q32 is associated with short survival time in PRC patients. The purpose of our work was to analyze allelic imbalance in locus 1q32 and MSI by using STR-markers in different groups of PRC patients to assess the prognostic relevance of these alterations. We have studied 39 PRC paired samples (fragments of tumor and adjacent morphologically intact tissue) using D1S2142 и D1S3465 polymorphic repeats (locus 1q32) by PCR with fluorescently labeled primers and fragment analysis in ABI3100 sequencer (“Applied Biosystems”). Allelic imbalance was observed in 36.8% of informative cases, MSI — in 48.7% of tumor samples. We have not witnessed any associations of allelic imbalance or MSI with disease stage, tumor grade and metastases at the diagnosis. Still, the correlation trend was demonstrated for MSI frequency and tumor grade that might indicate the association of MSI with primary tumor progression; however, this suggestion requires confirmation by investigation of a larger sampling. Additionally, genetic heterogeneity of different primary tumors was revealed in multifocal PRC, as well as involvement of adjacent normal kidney parenchyma in carcinogenesis, which is concordant with conception of field cancerization in primary-multiple PRC. As a whole, it was demonstrated for the first time that 1q32 allelic imbalance and MSI are frequent events in the papillary renal cell carcinomas, could be observed at any disease stage, even in the morphologically normal tissue of kidney with multifocal PRC. Investigation of prognostic utility of MSI is rational by testing a large patient cohort.
Testicular tumor: influence of diagnostic delay on disease stage and prognosis
A.K. Nosov, S.B. Petrov, E.M. Mamizhev, I.V. Karnaukhov
Department of oncourology N.N. Petrov Research Institute of Oncology, Saint-Petersburg, Russia
Testicular cancer — the most common solid malignancy in men at a young age, ranked second in frequency among malignant tumors in men 35 to 39 years. One of the reasons for the unsatisfactory results of treatment for this pathology could be late diagnosis.
The aim of study was to analyse the actual time from appearing of the first symptoms till the final staging and evaluation of its effect on the stage of disease at the beginning of treatment.
A retrospective analysis based on data from case histories of 294 patients treated between 1998 and 2011 years, as well as a results of their survey the last time of visiting doctor.
The median time from appearing of the first symptoms to final diagnosis was 14 weeks in the general population, in patients with seminoma 17 weeks and with testicular non-seminoma tumor 13 weeks. To analyse the effect of the delay in the diagnosis of the patients and the role of general practitioner time period was divided into 3 periods. The median period from onset of symptoms and/or suspicion of testicular tumor before patient first visited doctor in the general population was 9.5 weeks, from first contact to orchifuniculectomy was 3 weeks, from the surgery till the final diagnosis was 2 weeks. For seminoma tumor, these intervals were 11; 4 and 2 weeks accordingly. For non-seminoma tumor 9; 3 and 2 weeks respectively.
The allocation of these groups of patients by stage of the disease: the median time from first symptoms and/or suspicion of testicular tumor before the final diagnosis in the general population was Stage I — 13 weeks; Stage II — 23 weeks and Stage III — 21 weeks. With seminoma: I stage — 14 weeks; Stage II — 25 weeks and Stage III — 28 weeks. For non-seminoma tumor: Stage I — 10 weeks, Stage II — 21 weeks and Stage III — 21 weeks.
The statistical analysis showed a significant dependence of the stage of disease on the time of the diagnostic delay, as for group in the general population (p<0.001) and among patients with seminoma (p=0.001) and for non-seminoma tumor (p<0.001).
In our group of patients with germ cell testis tumors stage of the disease was significantly depended on the delay of time diagnosis. Reducing of this time period should lead to the early stage diagnostics and decrease the amount of required treatment measures.














Leave a comment