Профилактическая мастэктомия: взгляд на проблему
Смоланка И.И., Скляр С.Ю., Лобода А.Д.
Резюме. Рассмотрены вопросы выполнения профилактической двухсторонней мастэктомии у лиц — носителей мутации гена BRCA1/2. Представлены данные клинических рекомендаций NCCN и ESMO, мнения специалистов и личный опыт пациентки.
В настоящее время большинство исследователей рассматривают рак грудной железы (РГЖ) как ряд генетически разнородных опухолевых процессов, развивающихся в одном органе-мишени и имеющих различное течение и прогноз. Особую важность имеют исследования, посвященные определению молекулярно-генетических особенностей злокачественных новообразований, изучению корреляций молекулярных субтипов с клинико-биологическими характеристиками и ответами на те или иные схемы лечения. При прогнозировании возникновения и течения РГЖ особое значение уделяют фактору наследственности, связанному с мутацией гена BRCA 1/2 [1–6]. В руководстве по профилактике и лечению РГЖ (NCCN — National Comprehensive Cancer Network, 2013) отмечено, что риск развития РГЖ у женщин — носителей мутации BRCA1/2 оценивается в 56–84%. Ретроспективные анализы рандомизированных исследований с медианой наблюдения более 13 лет показали, что у женщин с высоким риском развития РГЖ и доказанной мутацией гена BRCA1/2 двухсторонняя профилактическая мастэктомия снижает риск развития опухоли в грудной железе в среднем на 90% [3–6, 7, 9]. В связи с этим NCCN поддерживает желание женщин с высоким риском развития РГЖ выполнить профилактическую двухстороннюю мастэктомию.
В клинических рекомендациях ESMO (European Society for Medical Oncology) по диагностике, лечению и наблюдению больных РГЖ фактору наследственной предрасположенности к РГЖ отведен целый раздел. Частота наследственной предрасположенности к РГЖ составляет около 25% всех случаев заболевших. Приблизительно 5–10% случаев РГЖ и рака яичника вызваны мутациями генов BRCA1, BRCA2, CHEK2, TP53 и PTEN. Специфичность и чувствительность определения мутации генов BRCA1 и BRCA2 высока при РГЖ, в то время как мутации в CHEK2, ATM, BRIP1 и PALB2 сегодня малоинформативны, более 70% случаев генетической предрасположенности к РГЖ остаются необъяснимыми.
Распространенность носителей мутации гена BRCA в общем в популяции составляет от 1/800 до 1/1000. Это обусловливает повышение риска развития РГЖ на 15–20%. Распространенность мутаций генов BRCA1 или BRCA2 значительно различается у этнических групп в разных географических регионах. Специфические мутации генов в зависимости от популяции описаны в Исландии, Нидерландах, Швеции, Норвегии, Германии, Франции, Испании, Канаде, странах Центральной и Восточной Европы, а также среди потомков евреев, выходцев из Германии.
Частота мутаций BRCA1 и BRCA2 (рис. 1 а, б) у больных РГЖ и раком яичника, изначально не дифференцированных по признаку наследственности либо возраста, в общей массе незначительна: <1-7% приходится на BRCA1 и 1–3% — BRCA2.
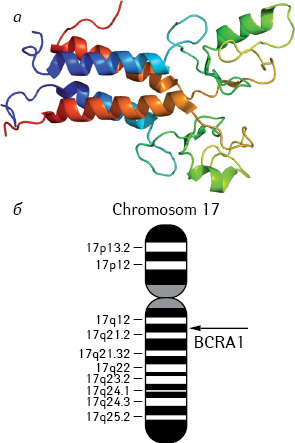
По данным, основанным на объединенных случаях, не дифференцированных по признаку наследственности, предполагают, что средний кумулятивный риск развития РГЖ у носителей BRCA1-мутации составил 65% (доверительный интервал — ДИ — 44–78%) для РГЖ и 39% (ДИ 18–54%) для рака яичника. Аналогичные показатели оценки для BRCA2 составили 45% (31–56%) и 11% (2,4–19%) соответственно [4–6, 8].
Повышенный риск развития РГЖ также отмечен у мужчин при мутациях обоих генов, главным образом BRCA2 (6%). Другими локализациями рака, имеющими повышенный риск развития при мутации BRCA1/2, являются рак поджелудочной железы (до 2%), рак желудка и рак головы и шеи, особенно у мужчин в возрасте младше 65 лет. При наличии в семье лица, перенесшего онкологическое заболевание, во многих развитых странах проводят генетическое тестирование, в частности тестирование на наличие мутации гена BRCA. В разных странах критерии генетического тестирования могут варьировать в зависимости от распространенности мутаций. Широко применяемые в США критерии для направления на генетическое исследование включают в себя: 1) три или более случая РГЖ и/или рака яичника среди близких родственников, при этом по крайней мере у одного из них в возрасте <50 лет; 2) два случая РГЖ у родственников в возрасте <40 лет; 3) РГЖ у мужчин и женщин, изначально диагностированный в молодом возрасте; 4) РГЖ у потомков евреев, выходцев из Германии, в возрасте <60 лет, возникновение билатерального РГЖ в молодом возрасте, РГЖ и рака яичника у одного лица.
Решение Анджелины Джоли (Angelina Jolie) (рис. 2) провести двустороннюю ампутацию грудных желез (мастэктомию), а затем и овариоэктомию всколыхнуло весь мир.

Анджелина Джоли — известная и многими любимая кинозвезда — перенесла операцию по удалению обеих грудных желез, чтобы предотвратить развитие рака этой локализации. Чтобы помочь другим женщинам, оказавшимся в подобной ситуации, актриса решила поделиться опытом.
«Моя мать сражалась с раком почти 10 лет и умерла в возрасте 56 лет. Она продержалась достаточно долго, чтобы дождаться первых внуков и подержать их у себя на руках. Но остальные мои дети навсегда лишены возможности узнать бабушку и то, насколько любящим и добрым человеком она была. Мы часто говорим о моей матери, и я пытаюсь рассказать детям о той болезни, которая отняла ее у нас. Они спрашивают, может ли то же самое случиться со мной. Я всегда говорю, что им не о чем беспокоиться, однако правда заключается в том, что я несу в себе «бракованный» ген BRCA, который существенно повышает риск возникновения у меня РГЖ и рака яичника. Когда я узнала, что меня ожидает, я решила действовать в упреждающем порядке, дабы по мере возможности свести риск развития РГЖ до минимума. Я приняла решение об операции — двусторонней мастэктомии. Я начала именно с грудной железы, поскольку риск возникновения РГЖ у меня гораздо выше, чем рака яичника, и потому что эта операция с последующей пластикой органа более сложная. 27 апреля 2013 г. я закончила 3-месячный курс медицинских процедур, необходимых для подготовки к операции. Все время мне удавалось держать мое решение в тайне, и я продолжала работать. Но я решила написать об этом в надежде на то, что мой опыт пойдет на пользу другим женщинам, которые попали в затруднительное положение. Рак — это до сих пор то слово, которое вселяет страх в сердца людей и порождает глубокое чувство бессилия. Но сегодня путем проведения анализов крови и генетических исследований вполне можно узнать, насколько вы подвержены опасности развития РГЖ и рака яичника, и затем принять решение и соответствующие меры. Свои процедуры я начала 2 февраля 2013 г. с терапии, позволяющей исключить возникновение болезни в протоках грудных желез в области сосков и увеличить приток крови в эту зону. Это немного болезненно, появляются гематомы, но такая процедура дает возможность спасти сосок. Спустя 2 нед мне сделали основную операцию, удалив ткани грудных желез и установив временные наполнители. Операция длилась около 8 ч. Когда я пришла в себя, в груди были дренажные трубки и расширители. Похоже на сцену из научно-фантастического фильма. Но спустя несколько дней после операции я возвратилась к нормальной жизни. Через 9 нед после этого была проведена завершающая восстановительная операция с установлением имплантов. За последние несколько лет такие операции были существенно усовершенствованы, и результаты оказались просто чудесными. Я решила написать об этом и рассказать другим женщинам, что принять решение о проведении мастэктомии мне было непросто. Но я счастлива, что согласилась на эту операцию. Шансы на возникновение у меня РГЖ снизились с 87 до 5%. Теперь я скажу своим детям, что они могут не бояться потерять меня из-за этой тяжелой болезни».
Узнав все это и проанализировав ситуацию, мы не можем отрицать долю пиара и широкомасштабной рекламы лабораторной диагностики, пластической хирургии и имплантов грудной железы, но оставаться в стороне от этого важного и волнующего женщин — носителей мутации гена BRCA1/2, получивших большой объем такой информации, вопроса тоже не можем. На сегодня проведение профилактической двухсторонней мастэктомии может рассматриваться при наличии факторов: наследственной предрасположенности в сочетании с доказанной мутацией гена BRCA1/2 и настойчивого желания пациентки, уверенной в том, что это наиболее приемлемое решение проблемы.
Таким образом, женщины, обращающиеся в медицинские учреждения для проведения двухсторонней профилактической мастэктомии, должны получить многопрофильную консультацию специалистов, пройти клиническое обследование грудных желез и обзорную маммографию, если ее не выполняли в течение последних 6 мес. Если результаты обследований не выявляют каких-либо противопоказаний к общему наркозу и оперативному вмешательству, женщины, которые выбирают профилактическую двухстороннюю мастэктомию, могут быть прооперированы с или без одномоментной реконструкции грудных желез. Двухсторонняя мастэктомия, выполняемая для снижения риска развития РГЖ, должна включать полное подкожное удаление всех тканей грудной железы (то есть подкожную ампутацию органа). Данная операция не требует подмышечной лимфодиссекции, за исключением случаев, когда при окончательном патологистологическом заключении удаленной ткани выявляют РГЖ. После выполнения операции и проведения реабилитационных мероприятий (рис. 3) женщины, имеющие мутации BRCA1/2, подлежат постоянному наблюдению в соответствии со стандартами диагностики и лечения, утвержденными МОЗ Украины, так как еще существует риск развития рака репродуктивных органов. Пациентки, у которых после оперативного вмешательства диагностирован РГЖ (LCIS или DCIS), должны проходить специальное противоопухолевое лечение также в соответствии со стандартами диагностики и лечения, утвержденными МОЗ Украины. Большинство рекомендаций по поддержанию здоровья общеприняты и не связаны с проводимой операцией на грудной железе.
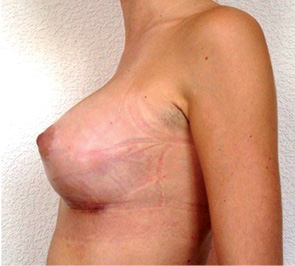
Профилактическая двухсторонняя мастэктомия — наиболее эффективная из известных на сегодня стратегий по снижению риска развития РГЖ у носителей мутации гена BRCA [7], хотя многие женщины не считают ее приемлемой по косметическим соображениям. Контралатеральная профилактическая мастэктомия — вариант к рассмотрению для носителей мутации BRCA, перенесших лечение по поводу РГЖ в молодом возрасте.
Типы профилактической мастэктомии могут быть от подкожной ампутации грудной железы с сохранением сосковоареолярного комплекса до тотальной мастэктомии. Различные варианты реконструкции грудной железы должны быть обсуждены и согласованы с пациенткой с учетом ее особенностей, индивидуальных преимуществ и рисков проведения данного вмешательства.
Список использованной литературы
1. Fackental J.D., Olopade O.I. (2007) Breast cancer risk associated with BRCA1 and BRCA2 in diverse populations. Nat. Rev. Cancer, 7: 937–948.
2. Ford D., Easton D.F., Stratton M. et al. (1998) Genetic heterogeneity and penetrance analysis of the BRCA1 and BRCA2 genes in breast cancer families. The Breast Cancer Linkage Consortium. Am. J. Hum. Genet., 62: 676–689.
3. Pharoah P.D., Antoniou A., Easton D., Ponder B. (2008) Polygenes, risk prediction, and targeted prevention of breast cancer. N. Engl. J. Med., 358: 2796–2803.
4. Antoniou A., Pharoah P.D., Narod S. et al. (2003) Average risks of breast and ovarian cancer associated with BRCA1 or BRCA2 mutations detected in case series unselected for family history: a combined analysis of 22 studies. Am. J. Hum. Genet., 72: 1117–30.
5. Walsh T., Casadei S., Coats K.H. et al. (2006) Spectrum of mutations in BRCA1, BRCA2, CHEK2, and TP53 in families at high risk of breast cancer. JAMA, 295: 1379–88.
6. Meijers-Heijboer H., van Geel B., van Putten W.L. et al. (2001) Breast cancer after prophylactic bilateral mastectomy in women with a BRCA1 or BRCA2 mutation. N. Engl. J. Med., 345: 159–164.
7. Gerber B., Krause A., Dieterich M. et al. (2009) The oncologic safety of skin sparing mastectomy with conservation of the nipple-areola complex and autologous reconstruction: an extended follow-up study. Ann. Surg., 249: 461–468.
8. Andrieu N., Goldgar D., Easton D. et al. (2006) Pregnancies, breast-feeding, and breast cancer risk in the International BRCA1/2 Carrier Cohort Study (IBCCS). J. Natl. Cancer Inst., 98: 535–44.
9. Rottenberg S., Jaspers J.E., Kersbergen A. et al. (2008) High sensitivity of BRCA1-deficient mammary tumors to the PARP inhibitor AZD2281 alone and in combination with platinum drugs. Proc. Natl. Acad. Sci. USA, 105: 17079–84.
Профілактична мастектомія: погляд на проблему
Резюме. Розглянуто питання виконання профілактичної двобічної мастектомії у пацієнток, які є носіями мутації гена BRCA1/2. Авторами наведено дані клінічних рекомендацій NCCN и ESMO, думки фахівців й особистий досвід пацієнтки.
Ключевые слова: рак грудної залози, мутації гена BRCA1/2, профілактична мастектомія.
Prophylactic mastectomy: opinionI.
Summary. The question of the bilateral prophylactic mastectomy in patients, carriers of the mutation of the gene BRCA 1/2 have been considered. The NCCN and ESMO clinical guidelines, the opinions of experts and personal experience of the patient were presented.
Key words: breast cancer, mutations in the BRCA1/2gene, prophylactic mastectomy.














Leave a comment