Експресія CD44 в аденокарциномах товстої кишки
Грабовой А.Н., Савчин Т.М., Антонюк С.А., Тарасова Т.А.
Резюме. Аденокарциноми товстої кишки проявляють виражену гетерогенність за експресією CD44. Інтенсивність експресії CD44+ не залежить від грейда пухлини, але залежить від плоїдності, а частка клітин у пухлині, що експресують CD44%, залежить від грейда і не залежить від кількості ДНК в їх ядрах. Похідне двох згаданих показників (CD44%+) зворотно корелює з накопиченням ДНК в ядрах пухлинних клітин. Отримані значення залежностей є слабкими, що не дозволяє використовувати показники експресії CD44 як самостійні критерії для уточнення грейда аденокарциноми або прогнозу. Найбільш виражена експресія CD44 у клітинах аденокарцином із вмістом ДНК від 2с до 4с дає можливість розглядати їх як пул, який є найбільш насичений стовбуровими клітинами та визначає розвиток пухлини.
Резюме. Аденокарциномы толстой кишки проявляют выраженную гетерогенность по экспрессии CD44. Интенсивность экспрессии CD44+ не зависит от грейда опухоли, но зависит от плоидности, а доля клеток в опухоли, экспрессирующих CD44%, зависит от грейда и не зависит от количества ДНК в их ядрах. Производное двух упомянутых показателей (CD44%+) обратно коррелирует с накоплением ДНК в ядрах опухолевых клеток. Полученные значения зависимостей являются слабыми, что не позволяет использовать показатели экспрессии CD44 в качестве самостоятельных критериев для уточнения грейда аденокарциномы или прогноза. Наиболее выраженная экспрессия CD44 в клетках аденокарцином с содержанием ДНК от 2с до 4с дает возможность рассматривать их как пул, наиболее насыщенный стволовыми клетками и определяющий развитие опухоли.

Введение
CD44 является одной из широко распространенных молекул клеточной адгезии и опосредует сцепление клеток с внеклеточным матриксом [24]. Этот гликопротеин участвует во многих клеточных процессах, в том числе росте, выживании, дифференцировке и подвижности [9, 20, 23]. В эпителии толстой кишки CD44 экспрессируется преимущественно в глубине крипт [15]. CD44 супрессирует апоптоз, что может играть критичную роль в развитии опухоли толстой кишки и переходе аденома-рак [24], ассоциируется с агрессивным поведением опухоли [6, 24], связан с опухолевой прогрессией и стадией Dukes’ [15]. CD44, как и некоторые другие молекулы адгезии, могут выступать в качестве супрессоров миграции опухолевых клеток [14]. В то же время сплайс-варианты CD44 или CD44 вместе с другими молекулами адгезии, такими как CD26, могут привести к формированию метастатических фенотипов опухолевых клеток [7, 17, 18, 21].
Белок CD44 обратил на себя особое внимание как важнейший маркер стволовых клеток колоректального рака (КРР) [11, 13, 16]. CD44-клетки опухоли способны образовывать колонии in vivo и генерировать опухоли при ксенотрансплантации. При этом нокдаун CD44, но не CD133, сильно препятствовал развитию опухоли. Только лишь 100 CD44 клеток КРР, выделенных из опухоли, смогли дать начало очагу опухолевого роста [11]. Была также показана гетерогенность и самих CD44 клеток: CD44/PrPc клетки КРР, в отличие от CD44/PrPc, имеют высокий потенциал по образованию метастатических очагов в печени [12].
Цель роботы — определить особенности экспрессии CD44 среди клеток аденокарцином (АК) толстой кишки разных грейдов и с разным содержанием ДНК в ядрах.
Объект и методы исследования
Исследования проведены на материале 92 опухолей толстой кишки: полипы и аденомы (В) — 14; АК G1 (G1) — 23; АК G2 (G2) — 46; АК G3 (G3) — 9. Обработка материала была четко стандартизована. Тканевые образцы фиксировали в забуференном 10% формалине (pH 7,4; 24 ч) и заливали в парапласт с использованием гистиопроцессора Histos-5 (Milestone, Италия). Из блоков изготавливали срезы толщиной 5 мкм на микротоме Microm НМ325 (Thermo Scientific, Германия). Срезы окрашивали гематоксилином и эозином, галлоцианин-хромовыми квасцами по Эйнарсону (pH 1,62; 37 °С; 24 ч) для выявления содержания нуклеиновых кислот [4, 5]. Для каждого случая часть срезов обрабатывали РНКазой (MACHEREY-NAGEL GmbH&Co. KG, Германия) для экстракции РНК [4]. Иммуногистохимические реакции проводили с моноклональным мышиным антителом против CD44 человека (HCAM Clone 156-3C11, DBS, США) в соответствии с протоколом производителя с использованием системы детекции EnVision FLEX (Dako, Дания). Срезы докрашивали гематоксилином Gill.
Препараты изучали и фотографировали при помощи микроскопа Nikon Eclipse 80i с камерой DS-5SMc/L2 при стандартизованных условиях, а изображения (×400, 1280×960 пикселей RGB) обрабатывали с использованием системы анализа ImageJ 1,46. На изображениях препаратов, окрашенных галлоцианин-хромовыми квасцами, в 30 клетках каждой опухоли определяли площадь сечения ядра, интегральную оптическую плотность ядра и рассчитывали содержание в нем ДНК (nuclear DNA — NDNA). При определении последнего в качестве единицы использовали содержание ДНК в ядрах лимфоцитов (2с) стромы опухоли [1]. По среднему NDNA клеток опухоли были разделены на три ранга: D — <1,2, D+ — 1,2–2,5 и Т+ — >2,5. Клетки опухоли разделяли на морфофункциональные ранги с условно нормальными ядрами (Nn) и на такие, ядра которых находились в состоянии пикноза (Np) или лизиса хроматина (Nl). Оценку проводили по критерию средней оптической плотности, площади сечения ядра и содержанию в нем ДНК по оригинальной методике [3].
Экспрессию CD44 оценивали на 5 цифровых изображениях каждой опухоли. Определяли процент меченых опухолевых клеток (CD44%), а также интенсивность экспрессии (CD44+): мембранная частичная — 1+, мембранная полная — 2+, мембранная полная и цитоплазматическая — 3+. Рассчитывали средние значения для каждой опухоли и вычисляли интегральный коэффициент экспрессии (CD44%+) как произведение значений CD44%•CD44+.
Статистический анализ проводили в среде IBM SPSS Statistics 22. Коэффициент корреляции Пирсона использовали для анализа взаимосвязей. Для сравнения групп применяли H-критерий Краскела — Уоллиса, U-критерий Манна — Уитни для случайных величин с распределением, отличным от нормального, а также t-критерий Стьюдента для величин с нормальным распределением. Для исследования связи между порядковыми переменными использовались таблицы сопряженности c критерием согласованности Пирсона (χ).
Таблица. Результаты корреляционного анализа оценки связей между экспрессией CD44 и содержанием ДНК, относительным содержанием морфофункциональных типов клеток в опухоли
| CD44% | CD44%+ | Nn% | Nl% | Np% | |
| NDNA (у.е.) | −0,151 | −0,200 (−0,214)* | −0,050 | −0,173 | 0,170 |
| CD44% | − | − | 0,171 | −0,104 | −0,104 |
| CD44%+ | − | − | 0,174 | −0,046 | −0,147 |
*Результаты, полученные на основе статистического бутстрепа (p<0,05).
NDNA — содержание ДНК в ядрах опухолевых клеток; CD44% — процент меченых клеток; CD44%+ — интегральный коэффициент экспрессии; Nn%, Nl%, Np% — процент опухолевых клеток с условно нормальными ядрами, ядрами в состоянии пикноза или лизиса хроматина соответственно.
При статистическом анализе показателей экспрессии CD44 в АК оказалось, что два случая имеют аномальные значения для своих групп, что приводит к «выбросу данных». Значения их показателей выходили за пределы распределения данной величины для заданной исследуемой группы. Эти случаи (B и АК G3) были исключены из анализа для повышения однородности исследуемой выборки. Таким образом, последующий анализ проведен на 90 образцах опухолей.
Результаты и их обсуждение
Проведенные исследования показали, что экспрессия CD44 в АК и аденомах толстой кишки варьировала в значительных пределах. Так, исследуемые опухоли характеризовались широким диапазоном CD44%, составлявшим от 2 до 100% со средним значением 46,6±2,8%. CD44+ при этом являлась исключительно положительной: для 20% опухолей она составила 1+, для 46% — 2+ и, соответственно, 3+ — для 34% оставшихся.
Оценка средних значений экспрессии CD44 показала (рис. 1), что относительное количество меченых клеток (CD44%) возрастало в диапазоне от аденом до G2, после чего несколько уменьшалось в G3. Средняя интенсивность экспрессии (CD44+) достоверно повышалась при переходе от аденом к АК и не имела статистически значимых отличий между АК разных грейдов. Интегральный показатель экспрессии CD44%+ возрастал в диапазоне аденома — G2. Это происходило на фоне некоторого снижения содержания ДНК в клетках АК [1] и увеличения относительного количества опухолевых клеток с условно нормальными ядрами [3].
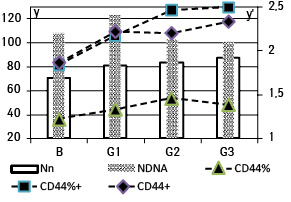
Среднее NDNA опухолей варьировало в пределах от 0,8 до 5,2 у.е., а его среднее значение для всей выборки составило 2,1±0,1 у.е. Последнее свидетельствует о том, что для большинства опухолей нашей выборки присуща хромосомная нестабильность, являющаяся наиболее распространенным механизмом развития АК [8, 10]. При разделении опухолей на ранги по содержанию ДНК наиболее многочисленной оказалась D+, 50 (56%), T+ включила 26 (29%) случаев, и только 14 (15%) изученных АК можно было отнести в ранг с содержанием ДНК, приближенным к диплоидному (ранг D). Это дает основание рассматривать последние АК как развивающиеся за счет микросателлитной нестабильности [10].
Аппроксимация зависимости NDNA и экспрессии CD44 в целом для всей выборки опухолей (рис. 2) показала полиноминальную зависимость между этими показателями, однако с крайне низкой ее значимостью (для: CD44% R=0,15; CD44+ R=0,15; CD44%+ R=0,17). Применительно к опухолям разной степени дифференцировки (G) величина достоверности аппроксимации оказалась значительно выше (NDNA/CD44%+; максимальные значения для: B R=0,73, G1 R=0,46, G2 R=0,18, G3 R=0,7). Это дает основание утверждать, что между NDNA и экспрессией CD44 отсутствует прямая зависимость. Введение же в систему анализа грейда указывает на тенденцию и возможную связь экспрессии CD44 с уровнем анаплазии. Примечательно, что максимальные значения кривой тренда как для аппроксимации NDNA/CD44%+ в целом для выборки, так и для отдельных грейдов находится в диапазоне значения NDNA 1,5–2,0 (см. рис. 2).
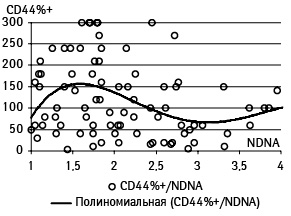
Проведенный корреляционный анализ для общей оценки связей между экспрессией CD44 и NDNA в целом также показал отсутствие значимых результатов (таблица). Однако для CD44%+ и NDNA отмечена корреляция с коэффициентом r=−0,2, приближающаяся к статистически значимой (p=0,059). Дополнительно использованный в этом случае метод статистического бутстрепа позволил получить значимый результат, демонстрирующий наличие обратной связи между CD44%+ и NDNA (r=−0,214, p=0,044). Данный факт подтверждается результатами, полученными при исследовании связи между интенсивностью экспрессии (СD44+) и рангом опухоли по содержанию ДНК. Так, при росте последнего интенсивность экспрессии снижается (χ=10,72; p=0,0299), причем нелинейно, с наибольшими значениями интенсивности для ранга D+ (рис. 3).
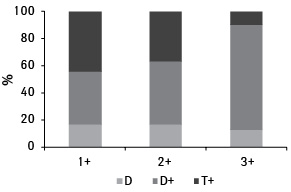
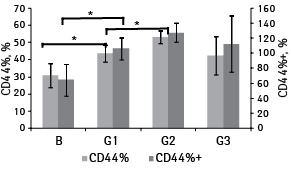
Оценка NDNA в группах опухолей с различной интенсивностью экспрессии CD44+ показала, что его наименьшее значение характерно для ранга 3+ по сравнению с 1+ (p=0,034) и 2+ (p=0,035) и составляет 1,84±0,09 у.е. (рис. 4). При попарном сравнении рангов по CD44% и CD44%+ прослеживалось отличие опухолей T+ от D+ по уровню экспрессии CD44% (p=0,026), а также по CD44%+ (p=0,006) (рис. 5). Для опухолей D и D+ схожих различий не отмечено (p=0,135 и p=0,102 соответственно).
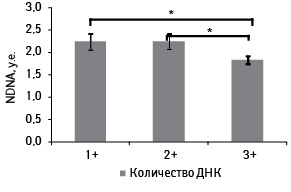
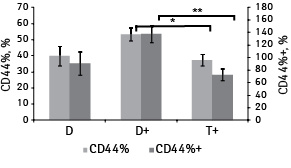
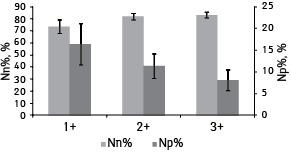
Итак, наибольшие частота мечения и интенсивность экспрессии CD44+ характерны для опухолей ранга D+, самые низкие — для ранга T+. Повышение содержания ДНК сопровождается уменьшением экспрессии CD44. Необходимо отметить, что в последнем ранге показатель процента клеток с пикнотическими ядрами является самым высоким (16,8±4,7%) [3], такой же показатель (16,4±4,8%) характерен для опухолей CD441+, также является самым высоким показателем по сравнению с другими группами (рис. 6).
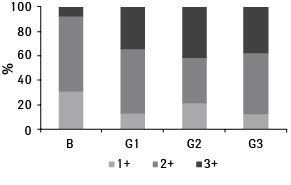
Проведенный анализ не выявил статистически значимых отличий интенсивности экспрессии CD44+ между аденомами и АК разных грейдов (χ=6,69; p=0,35). Однако обнаружилась некоторая тенденция к повышению уровня CD44+ по мере нарастания анаплазии в опухолях (рис. 7). Сравнение групп с использованием H-критерия Краскела — Уоллиса показало повышение CD44% по мере снижения уровня дифференцировки новообразования от B до G3 (p=0,024). Причем в диапазоне B–G1–G2 его значимость была определена на уровне p=0,01 (рис. 8). Группа G3, будучи наименее многочисленной, не продемонстрировала статистически значимых результатов.
Таким образом, проведенные исследования показали, что АК являются весьма гетерогенными по экспрессии CD44. Вместе с тем выявлено, что интенсивность экспрессии CD44+ не зависит от грейда опухоли, но зависит от плоидности. И наоборот, доля клеток, экспрессирующих CD44%, в опухоли зависит от грейда и не зависит от количества ДНК в их ядрах. Производное двух упомянутых показателей (CD44%+) обратно коррелирует с накоплением ДНК. Полученные значения зависимостей являются слабыми, что не позволяет использовать показатели экспрессии CD44 в качестве самостоятельных критериев для уточнения грейда АК или прогноза.
Выявленные зависимости между экспрессией CD44 и грейдом опухоли или содержанием ДНК в ядрах ее клеток, прежде всего, могут отражать процессы клональной эволюции [19, 22] в АК, характер которой зависит от патогенетического механизма развития опухоли [8, 10]. Так, нарастание в опухолях части клеток, экспрессирующих CD44, по мере снижения их дифференцировки совпадает с сужением их клеточного спектра по содержанию ДНК в ядрах [1]. Это можно рассматривать как результат элиминации из АК нежизнеспособных клеточных элементов и постепенного увеличения в их составе пула клеток с сохраненными системами жизнеобеспечения. Последнее утверждение основывается на данных об увеличении в АК типов клеток с ядрами, активными по морфофункциональным признакам [3].
Следует также отметить, что наибольшая экспрессия CD44 зафиксирована среди клеток АК, содержание ДНК в ядрах которых приближается к 4с. Последнее можно расценивать преимущественно как синтезирующие ДНК во время митотического цикла, что совпадает с данными о наибольшей митотической активности в этом сегменте спектра клеток АК [2]. Все это позволяет полагать, что к пулу клеток с содержанием ДНК от 2с до 4с и экспрессирующих CD44 принадлежат клетки, определяющие основной потенциал развития АК и рассматриваемые как стволовые [16].
Выводы
АК толстой кишки проявляют выраженную гетерогенность по экспрессии CD44. Интенсивность экспрессии CD44+ не зависит от грейда опухоли, но зависит от плоидности, а доля клеток в опухоли, экспрессирующих CD44%, зависит от грейда и не зависит от количества ДНК в их ядрах. Производное двух упомянутых показателей (CD44%+) обратно коррелирует с накоплением ДНК в ядрах опухолевых клеток. Полученные значения зависимостей являются слабыми, что не позволяет использовать показатели экспрессии CD44 в качестве самостоятельных критериев для уточнения грейда АК или прогноза.
Наиболее выраженная экспрессия CD44 в клетках АК с содержанием ДНК от 2с до 4с дает возможность рассматривать их как пул, наиболее насыщенный стволовыми клетками и определяющий развитие опухоли.
Список использованной литературы
1. Грабовий О.М., Антонюк С.А., Воробєй Є.А. (2013) Вміст нуклеїнових кислот у ядрах клітин епітеліальних пухлин товстої кишки. Український морфологічний альманах, 11(1): 73–76.
2. Грабовий О.М., Антонюк С.А., Воробєй Є.А. (2013) Мітотична активність та вміст нуклеїнових кислот у ядрах клітин епітеліальних пухлин товстої кишки. Патологія, 2(28): 13–16.
3. Грабовий О.М., Антонюк С.А., Сільченко В.П. та ін. (2015) Питомий вміст ДНК у ядрах клітин та клітинна гетерогенність аденокарцином товстої кишки. Патологія, 1(33): 44–47.
4. Лупа Х. (1980) Основы гистохимии (Пер. с немец.). Мир, Москва, 344 с.
5. Ташке К. (1980) Введение в количественную цито-гистологическую морфологию. (Пер. с рум.). Из. Акад. Соц. Респ. Румынии, 192 с.
6. Aruffo A., Stamenkovic I., Melnick M. et al. (1990) CD44 is the principal cell surface receptor for hyaluronate. Cell., 61: 1303–1313.
7. Bankfalvi A., Krassort M., Buchwalow I. et al. (2002) Gains and losses of adhesion molecules (CD44, E-cadherin, and betacatenin) during oral carcinogenesis and tumour progression. J. Pathol., 198: 343–351.
8. Bardhan K., Liu K. (2013) Epigenetics and colorectal cancer pathogenesis. Cancers, 5(2): 676–713.
9. Cheng C., Sharp P. (2006) Regulation of CD44 alternative splicing by SRm160 and its potential role in tumor cell invasion. Mol. Cell. Biol., 26: 362–370.
10. Coppedè F., Lopomo A., Spisni R. et al. (2014) Genetic and epigenetic biomarkers for diagnosis, prognosis and treatment of colorectal cancer. World J. Gastroenterol., 20: 943–956.
11. Dalerba P., Dylla S., Park I. et al. (2007) Phenotypic characterization of human colorectal cancer stem cells. Proc. Nat. Acad. Sci., 104: 10158–10163.
12. Du L., Rao G., Wang H. et al. (2013) CD44-positive cancer stem cells expressing cellular prion protein contribute to metastatic capacity in colorectal cancer. Cancer Res., 73(8): 2682–94.
13. Du L., Wang H., He L. et al. (2008) CD44 is of functional importance for colorectal cancer stem cells. Clin. Cancer Res., 14: 6751–6760.
14. Gao A., Lou W., Dong J. et al. (1997) CD44 is a metastasis suppressor gene for prostatic cancer located on human chromosome 11p13. Cancer Res., 57: 846–849.
15. Gotley D., Fawcett J., Walsh M. et al. (1996) Alternatively spliced variants of the cell adhesion molecule CD44 and tumour progression in colorectal cancer. Brit. J. Cancer, 74: 342–351.
16. Hong I., Hong S.W., Chang Y.G. et al. (2015) Expression of the cancer stem cell markers CD44 and CD133 in colorectal cancer: an immunohistochemical staining analysis. Ann. Сoloproctol., 31(3): 84–91.
17. Jothy S. (2003) CD44 and its partners in metastasis. Clin. Exp. Metastasis, 20: 195–201.
18. Martin T., Harrison G., Mansel R. et al. (2003) The role of the CD44/ezrin complex in cancer metastasis. Crit. Rev. Oncol. Hem., 46: 165–86.
19. Murugaesu N., Chew S.K., Swanton C. (2013) Adapting clinical paradigms to the challenges of cancer clonal evolution. Am. J. Pathol., 182(6): 1962–71.
20. Nagano O., Saya H. (2004) Mechanismand biological significance of CD44 cleavage. Cancer Sci., 95: 930–5.
21. Pang R., Law W., Chu A. et al. (2010) A subpopulation of CD26+ cancer stem cells with metastatic capacity in human colorectal cancer. Cell. Stem. Cell., 6: 603–15.
22. Swanton C. (2012) Intratumor heterogeneity: evolution through space and time. Cancer Res., 72(19): 4875–4882.
23. Vigetti D., Viola M., Karousou E. et al. (2008) Hyaluronan-CD44-1/2 regulate human aortic smooth muscle cell motility during aging. J. Biol. Chem., 283: 4448–4458.
24. Wielenga V., Van der Neut R., Offerhaus G. et al. (2000) CD44 glycoproteins in colorectal cancer: expression, function, and prognostic value. Adv. Cancer Res., 77: 169–87.














Leave a comment