Молекулярно-генетичні особливості раку шлунка: погляд клінічного онколога
Дубинина В.Г.1, Лурин А.Г. 2, Машуков А.А. 2, Захарцева Л.М.3, Орел Н.А. 2, Биленко А.А. 1, Згура А.Н. 2, Рациборский Д.В. 2, Максимовский В.Е. 1, Мерлич С.В. 2, Шилин И.В.2, Ли С.Н.2
- 1Одеський національний медичний університет
- 2Одеський обласний онкологічний диспансер
- 3Киевский городской клинический онкологический центр
Резюме. Проведено дослідження, присвячене експресії онкобілків при раку шлунка. Робота відзначається великою кількість цифр і складністю їх інтерпретації в низці випадків. Усього в дослідження, проведене на базі абдомінального онкохірургічного відділення КУ «Одеський обласний онкологічний диспансер», включено 188 хворих, оперованих з приводу раку шлунка в період 2007–2011 рр. У всіх випадках виконано лімфодисекції з принципових міркувань — великі профілактичні біопсії візуально незмінених лімфовузлів. Проведено багатофакторний аналіз залежності експресії онкобілків p53, VEGFR-3, erbB2 і проліферативної пухлинної активності Ki-67 від залученості пухлинного мікроциркуляторного русла (ly, V), місцевого росту (Т), наявності резидуальної пухлинної тканини (R), ступеня диференціювання пухлини (G), ступеня залученості регіонарних лімфовузлів (N), виду мікроінфільтрації (Inf α, β, Inf γ).
Резюме. Проведено исследование, посвященное экспрессии онкобелков при раке желудка. Работа отличается обилием цифр и сложностью их интерпретации в ряде случаев. Всего в исследование, проведенное на базе абдоминального онкохирургического отделения КУ «Одесский областной онкологический диспансер», включено 188 больных, оперированных по поводу рака желудка в период 2007–2011 гг. Во всех случаях выполнены лимфодиссекции по принципиальным соображениям — обширные профилактические биопсии визуально неизмененных лимфоузлов. Проведен многофакторный анализ зависимости экспрессии онкобелков p53, VEGFR-3, erbB2 и пролиферативной опухолевой активности Ki-67 от вовлеченности опухолевого микроциркуляторного русла (ly, V), местного роста (Т), наличия резидуальной опухолевой ткани (R), степени дифференцировки опухоли (G), степени вовлеченности регионарных лимфоузлов (N), вида микроинфильтрации (Inf α, β, Inf γ).
 Исследование взаимосвязи выраженности тех или иных гистологических и иммуногистохимических (ИГХ) маркеров до сих пор носит в значительной степени умозрительный, теоретизированный характер, оставаясь «кабинетной наукой». Его клиническое значение раскрывается в основном при прогнозировании результатов химиотерапии или скрининга. Например, значимая экспрессия Her2/new — назначение трастузумаба, лапатиниба [1]; мутированный ген EGFR — эрлотиниба, гефитиниба, афатиниба; транслокации EML4-ALK — кризотиниба; транслокации BCR-ABL — иматиниба; «дикий» тип генов тирозиновых киназ K-RAS и N-RAS — предикторы эффективности терапии цетуксимабом и панитумумабом [2], серин-треониновой киназы B-RAFwt — лечения вемурафенибом; наличие мутации генов CDH-1, BRCA-1, MLH1 [3], MLH3, MSH-2, MSH-6, PMS-1 — аутосомно-доминантное наследование предрасположенности к раннему раку желудка (РЖ) и т.д. В процессе разработки выявляют новые терапевтические «мишени»: ингибиторы ЦОГ-2 (есть сообщения об эффективности ацетилсалициловой кислоты при мутированном PIK3CA [4]), металлопротеиназы [5], теломераза, фарнезилтрансфераза [6].
Исследование взаимосвязи выраженности тех или иных гистологических и иммуногистохимических (ИГХ) маркеров до сих пор носит в значительной степени умозрительный, теоретизированный характер, оставаясь «кабинетной наукой». Его клиническое значение раскрывается в основном при прогнозировании результатов химиотерапии или скрининга. Например, значимая экспрессия Her2/new — назначение трастузумаба, лапатиниба [1]; мутированный ген EGFR — эрлотиниба, гефитиниба, афатиниба; транслокации EML4-ALK — кризотиниба; транслокации BCR-ABL — иматиниба; «дикий» тип генов тирозиновых киназ K-RAS и N-RAS — предикторы эффективности терапии цетуксимабом и панитумумабом [2], серин-треониновой киназы B-RAFwt — лечения вемурафенибом; наличие мутации генов CDH-1, BRCA-1, MLH1 [3], MLH3, MSH-2, MSH-6, PMS-1 — аутосомно-доминантное наследование предрасположенности к раннему раку желудка (РЖ) и т.д. В процессе разработки выявляют новые терапевтические «мишени»: ингибиторы ЦОГ-2 (есть сообщения об эффективности ацетилсалициловой кислоты при мутированном PIK3CA [4]), металлопротеиназы [5], теломераза, фарнезилтрансфераза [6].
ЦОГ-2 (СОХ-2), наряду с рецептором к фактору роста эндотелия сосудов (vascular endothelial growth factor receptor — VEGFR)-3 (VEGF-C), считается фактором прогноза при РЖ [7]. Имеется целый ряд сообщений о прогностической роли маркера Her2 при РЖ [8–11]. Экспрессия ERCC1 упоминается как предиктор чувствительности к оксалиплатину [12] при РЖ.
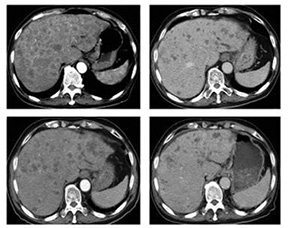
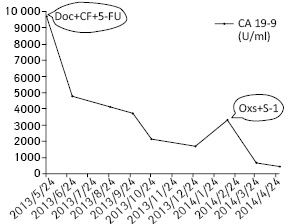
Уровень информационной РНК (mRNA — messenger RNA) гена BRCA-1 при РЖ в клинических исследованиях имел негативную корреляцию по отношению к чувствительности РЖ к цисплатину и положительную — к таксанам. В литературе описан случай успешного излечения доцетакселом BRCA-1+ метастатического РЖ с поражением печени [13] (рис. 1).
J.G. Kim [14] описывает следующие молекулы-мишени, актуальные при распространенном РЖ (2013 г.):
1. Моноклональные антитела к EGFR (цетуксимаб/панитумумаб).
2. Ингибиторы тирозиновой киназы EGFR (эрлотиниб/гефитиниб).
3. Моноклональные антитела к рецептору Anti-Her2 mAbs (трастузумаб).
4. Ингибиторы тирозиновой киназы Her2 TKI (лапатиниб).
5. Моноклональные антитела к фактору роста Anti-VEGF (бевацизумаб).
6. Моноклональные антитела к рецептору Anti-VEGFR (рамуцирумаб).
7. Ингибиторы тирозиновой киназы VEGFR (сунитиниб/сорафениб/седираниб/апатиниб).
8. Эверолимус — ингибитор mTOR (mammalian target of rapamycin), Akt pathway.
9. Онартузумаб — моноклональные антитела к рецептору фактора роста гепатоцитов (hepatocyte growth factor receptor — HGFR), кодируемому онкогеном c-Met. И некоторые другие молекулы, еще находящиеся на этапе клинических испытаний.
Продолжается мультицентровое исследование KEYNOTE-012 (1b фаза), посвященное перспективности иммунотерапии пембролизумабом у больных распространенным PD-L1+ РЖ [15].
Генетическое тестирование для индивидуализации программы скрининга здоровых людей (достаточно дорогостоящая процедура) делается всего один раз за весь период жизни (полноэкзомное секвенирование). Популяция опухолевых клеток неоднородна, имеются субпопуляции клеток в различных стадиях клеточного цикла, с различной чувствительностью к химиотерапевтическим режимам [16]. Различия между хемонаивными и предлеченными видами рака (формирование лекарственной устойчивости) мотивируют к получению повторных биопсий и стимулируют постепенное внедрение ИГХ исследования не только удаленных операционных препаратов, но и биоптатов опухолей [17], в том числе при РЖ.
Введение в клиническую практику молекулярной классификации РЖ [18], наподобие той, которая ныне широко используется при раке грудной железы, делает это направление поиска актуальным.
Невозможно в рамках одного исследования рассмотреть все белковые молекулы, экспрессируемые при РЖ [19, 20]. С учетом новой генетической классификации избраны четыре наиболее известных онкобелка, анализ которых максимально доступен.
Генетическая классификация РЖ включает четыре разновидности опухолей [21, 22]:
- генетически стабильный РЖ;
- РЖ с микросателлитной нестабильностью (microsatellite instability — MSI);
- хромосомно нестабильный (chromosome instable — CIN) РЖ;
- вирус Эпштейна — Барр (EBV)-ассоциированный РЖ.
Например, при так называемом CIN РЖ отмечают амплификацию гена TP53 (короткое плечо 17-й хромосомы) и онкогена Her2/new (длинное плечо 17-й хромосомы) — соответственно, при ИГХ исследовании будут экспрессированы белки p53 и erbB2 (CD340) (рис. 2 и 3). CIN РЖ составляет примерно 50% всех злокачественных эпителиальных опухолей желудка, поэтому исследование этих двух маркеров представлялось эффективным.
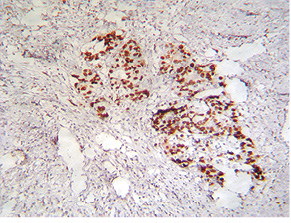
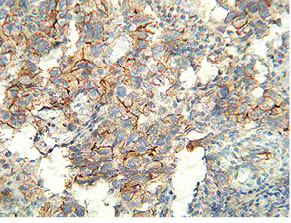
Три другие генетические формы РЖ представлены опухолями с MSI [3, 23, 24]; генетически стабильным раком («рак Наполеона» [25] — CDH-1-индуцированный, белковый продукт E-кадгерин), или, как его еще называют, кадгериновым РЖ; и EBV-индуцированным РЖ [22, 24, 26, 27], в котором выявляют экспрессию гена из другого сигнального каскада эпидермального рецептора EGFR — PI3K или PIK3CA — фосфоинозитол-3-киназы.
Наиболее часто отмечаемой мутацией при РЖ с MSI является так называемое умолкание (silencing) главного гена репарации ДНК — MLH1. Выключение других генов репарации — MLH3, MSH2, MSH3, MSH6, PMS1, PMS2 (хотя все гены-супрессоры считаются генами репарации, например BRCA) — фиксируют реже.
При CIN чаще развивается интестинальная форма РЖ по классификации Лорена, при генетически стабильном кадгериновом варианте — диффузный тип РЖ. Считается, что именно из-за дефицита или дефектности «межклеточного цемента» Е-кадгерина при диффузном РЖ раньше наступает гематогенная диссеминация. РЖ с MSI связан с гиперметилированием [24, 28] наиболее активных участков ДНК — CpG-островков (участков, где цитозин предшествует гуанину). Имеются отдельные сообщения о большей чувствительности этой генетической категории к химиотерапии иринотеканом. EBV-ассоциированный рак наиболее часто поражает антральный отдел желудка.
Генетический анализ MSI РЖ является единственным, который, как представляется, может быть использован в качестве хирургического фактора прогноза, так как классическая химиотерапия, особенно у пациентов пожилого возраста, в случае MSI не перспективна [29]. Данный вид опухолей проявляет выраженную локальную иммуносупрессивную активность [30, 31]. Поэтому, как и при EBV-ассоциированном РЖ, в лечении пациентов с РЖ с MSI считается оправданным назначение новых иммунологических препаратов (PD-L1/PD-L2: ипилимумаб, ниволумаб, пембролизумаб) [32].
Уже доступны моноклональные антитела для более широкого исследования MSI при РЖ [33]:
- Mismatch Repair Protein (MLH1) — антитела ES05;
- Mismatch Repair Protein (MSH2) — антитела 25D12;
- Mismatch Repair Protein (MSH6) — антитела PU29;
- Mismatch Repair Protein (PMS2) — антитела M0R4G.
В частности, E.N. Imyanitov [29] следующим образом комментирует важность анализа MSI для химиотерапии и его особенную значимость для хирургической онкологии:
1. Большинство карцином с MSI (колоректальный рак [КРР] с MSI-H [H — high — высокий уровень нестабильности], РЖ, рак эндометрия входят в синдром Линча) являются спорадическими [34, 35].
2. Наследственный КРР поражает относительно молодых субъектов, спорадические же случаи MSI-H накапливаются у пациентов пожилого возраста. Наследственный рак возникает из-за мутационной инактивации MLH1, MSH2, PMS2 или MSH6; спорадические опухоли с MSI-H обычно возникают в результате метилирования промотора гена MLH1, который может быть следствием широко распространенных нарушений эпигенетической регуляции («methylator-фенотипа»). По неизвестной причине, BRAF мутации происходят только в спорадических, но не в наследственных опухолях с MSI-H [35, 36].
3. Хотя опухоли с MSI-H низкодифференцированы, они, как правило, характеризуются благоприятным течением. В частности, демонстрируют относительно низкую частоту рецидивов после хирургического вмешательства [37, 38]; в соответствии с этим, только 4% местно-распространенного КРР имеют MSI-H фенотип [39, 40]. В результате, случаи MSI-H исключительно редки в исследованиях, связанных с метастатическим раком, поэтому прямая клиническая оценка их химиочувствительности является весьма сложной. Большинство ответов на лечение для случаев MSI-H являются производными от адъювантной терапии, где надежная дифференцировка между прогнозируемой и прогностической значимостью данного параметра не всегда возможна.
4. Чувствительность MMR-дефицитных клеток к различным противоопухолевым препаратам является предметом многочисленных лабораторных исследований. Важно иметь в виду, что естественные раковые клетки с MSI-H имеют исключительно высокую частоту мутаций и, следовательно, накапливается значительное количество «вторичных» генетических поражений; в зависимости от спектра генов-мишеней эти вторичные повреждения могут существенно изменить ответ на терапию [39, 41]. Кроме того, инактивация разных MMR генов, например MSH2 и MLH1, может привести к различным моделям химиочувствительности [42].
5. Большинство доклинических исследований указывает на резистентность MSI-H-клеток к 5-флуороурацилу (5-FU) [39, 43]. MSI-Н-статус также ассоциируется с низкой чувствительностью к цисплатину, карбоплатину, 6-тиогуанину, однако эти соединения в любом случае не применяют для лечения КРР [39, 42–44]. В то время как MMR-дефицитность связана с нечувствительностью к цисплатину [45–47] и карбоплатину, а также препарату третьего поколения оксалиплатину. Результаты нескольких исследований показали специфическую чувствительность MSI-H клеток к иринотекану; продемонстрировано, что ответ на топоизомеразу I может быть опосредован наличием вторичных мутаций в генах MRE11 и Rad50 [44]. Метотрексат является селективным ингибитором MSH2-дефицитных клеток; MLH1-дефектные клетки не показали специфической чувствительности к этому соединению [42, 48].
6. Существует консенсус в литературе, что у пациентов с MSI-H не применяют 5-флуороурацил в основе адъювантной терапии [49]. В некоторых сообщениях предполагают даже худший результат по сравнению с пролеченными пациентами; полихимиотерапия может поставить под угрозу естественный иммунный ответ на MSI-H клеток [39, 50, 51]. Адъювантная химиотерапия пациентов с наследственным КРР также продемонстрировала отсутствие пользы от 5-флуороурацила [52]. С учетом улучшенного прогноза течения опухолей с MSI-H, по общему мнению, адъювантная терапия должна быть опущена при КРР с MSI-H [39, 53, 54]. Комбинация 5-флуороурацила с оксалиплатином была недавно включена в руководящие принципы для адъювантной терапии III стадии КРР; поскольку только несколько пациентов с MSI-H в настоящее время доступны, то пока невозможно сделать выводы из существующей базы данных [55, 56]. Опыты с иринотеканом не квалифицировали этот препарат для использования в адъювантной терапии; однако анализ подгруппы пациентов с MSI-H показал, что эта специфическая категория больных может получить выгоду от добавления иринотекана к флуороурацилу и лейковорину [57].
7. Данные о применении химиотерапии при распространенном MSI-H раке ограничены несколькими небольшими исследованиями. J.T. Liang и соавторы [58] и W.M. Brueckl и соавторы [59] сообщили об улучшении ответа MSI-КРР на 5-флуороурацил. Существует противоречивая информация относительно роли статуса MSI в определении ответа на комбинацию терапии 5-флуороурацилом и оксалиплатином [60–62]. Несколько докладов продемонстрировали большую частоту ответа MSI-H для иринотекана [63–65], хотя это утверждение было оспорено в недавнем исследованием J.E. Kim и соавторов [66].
Так, рак с MSI-H соответствует достаточно частой клинической ситуации, когда при значительных размерах опухоли нет отдаленных метастазов (в противоположность тому, когда метастазы множественные, а первичной опухоли не удается найти вообще). При этом гистологически такой рак имеет наихудшие показатели агрессивности. Такие опухоли низкодифференцированные, характеризуются микроскопической опухолевой инфильтрацией (Inf γ), прорастают в окружающие структуры и могут иметь множественные метастазы в регионарных лимфоузлах. Однако после их удаления, как уже неоднократно сказано, процент рецидива достаточно низкий.
Еще одной, выявленной недавно, генетической особенностью РЖ является принадлежность части случаев (не более 5%) к так называемому синдрому Анжелины Джоли [67]: наличие наследственно передаваемой мутации одного из аллелей гена BRCA-1. Другими заболеваниями, относящимися к этому синдрому, являются рак грудной железы и рак яичника. Делеция оставшегося здорового аллеля (LOH — loss of heterosigosity — потеря гетерозиготности) ведет ко второму виду наследственного РЖ (первый — CDH1-ассоциированный). Так как все наследственные виды рака принадлежат к доминантно наследуемым, данная мутация проявляется в относительно раннем возрасте (до 50 лет).
Также, как и для BRCA-ассоциированного рака грудной железы, наличие амплификации этого гена при РЖ означает резистентность к химиотерапевтическим режимам на основе таксанов [68] и антрациклинов и чувствительность к митомицину С [69], цисплатину и PARP-ингибиторам (ингибиторы поли-АДФ-рибоза-полимеразы — парибы [70]), перспективность иммунотерапии [71]. Her2/neu позиционируется не только как фактор чувствительности к терапии трастузумабом, но и эпирубицином, доксорубицином [72], липосомальным доксорубицином.
Все вышесказанное свидетельствует о перспективности этого направления для анализа даже не в лабораторных, а полевых, клинических условиях.
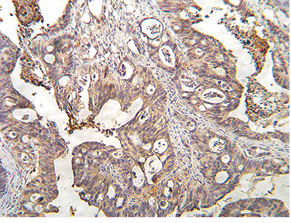
ИГХ исследования выполняли для оценки степени экспрессии белковых продуктов p53, VEGFR-3, Ki-67 [73], Her2/new (рис. 4 и 5). Одним из самых важных фактов об экспрессии Her2/new при РЖ является более мягкий подход для признания маркера положительным по сравнению с раком грудной железы [74]. В нашем исследовании маркер «++» считался положительным. В то время как для рака грудной железы необходимым является критерий «+++».
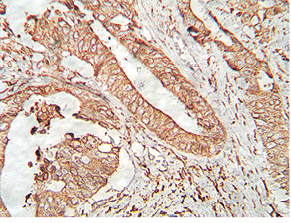
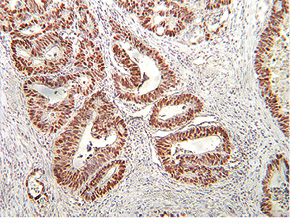
Ki-67 — ядерный антиген, окраска антителами к которому характерна в случае наличия клеток, находящихся в пролиферативной фазе клеточного цикла (G1, S, G2, M). Он также считается митотическим индексом. F. Penault-Llorca и соавторы установили [75], что больные, опухоли которых экспрессируют Ki-67 у >50% клеток, имеют значительный риск развития рецидива заболевания (не местного, а именно клинического рецидива). Экспрессию Ki-67 в исследовании связывали с чувствительностью к химиотерапии доцетакселом [75]. В нашей работе положительной считалась экспрессия у >30% клеток. Использованный реактив — моноклональные антитела MIB-1.
VEGFR-3 и его ростковый фактор VEGF-С ассоциированы с очень плохим прогнозом при РЖ [76]. Наконец, VEGFR-3 не является обычным маркером того дефектного неоангиогенеза, который происходит в опухоли (образование сосудов без перицитов, только эндотелиоциты). VEGFR, так же, как и Ki-67, не может быть использован в качестве фактора прогноза терапии: назначение бевацизумаба не требует выполнения данного анализа [77]. VEGFR-3 (VEGF-C) является фактором, который может быть использован для анализа процесса образования новых лимфатических сосудов в самой опухоли и вокруг нее — так называемого лимфангиогенеза [78, 79]. В нормальной ситуации VEGFR3 экспрессируется эндотелием ранних эмбрионов.
Все микроскопические сосуды в опухоли можно разделить на две группы: щелевидные образования с очень тонкой стенкой и классические микроскопические сосуды. Первые являются микроскопическими лимфатическими капиллярами и содержат лимфу, вторые — кровеносными капиллярами (рис. 6 и 7). Маркер VEGFR3 (рис. 8) имеет отношение к первым. Экспрессия данного маркера в опухоли обратно пропорциональна степени диссеминации по кровеносным капиллярам. Существует как бы компенсаторный механизм: если у опухоли «получалось» создавать новые лимфатические капилляры, диссеминация шла по ним; если нет — начиналась гематогенная диссеминация по кровеносным капиллярам. Наличие циркулирующих раковых клеток в кровеносном русле не означает напрямую наличие гематогенных метастазов, но является фактором плохого прогноза [80, 81]. Свойства микрососудов опухоли может определять эффективность того или иного вида химиотерапии [82].
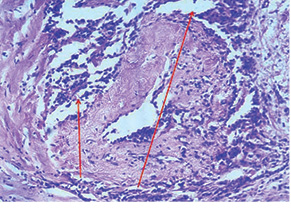
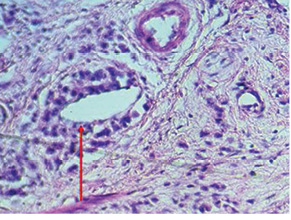
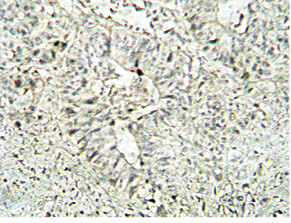
Перспективным, но не включенным в наше исследование маркером является Her1 или, как его называют сегодня, EGFR. Мы имеем одно наблюдение РЖ с мутацией данного гена и экспрессией соответствующего белкового продукта (рис. 9).
Объект и методы исследования
При анализе данных через поисковую систему PubMed и Google Scholar получено следующее количество поисковых запросов (табл. 1):
gastric cancer Her2/new — 165 (189)*;
gastric cancer p53 — 2102 (210 000);
gastric cancer VEGFR — 263 (19 800);
gastric cancer VEGF-C — 137 (9960);
gastric cancer Ki-67 — 733 (31 300);
gastric cancer p53 Ki-67 VEGF — 1 (6730);
gastric cancer p53 Her2 VEGF — 2 (43700);
gastric cancer p53 Her2 Ki-67 — 2 (4620);
gastric cancer Her2 Ki-67 VEGF — 0 (2200);
gastric cancer Her2 p53 Ki-67 VEGF — 0 (1740);
gastric cancer Her2/new p53 Ki-67 VEGF-C — 0 (0).
*В скобках указано количество ссылок на предмет по системе Google Scholar.
Таблица 1. Сочетание 2 и более факторов поиска по PubMed
| РЖ | Her2/new | p53 | VEGF | Ki-67 |
| Her2/new | − | 23 | 38 | 10 |
| p53 | 23 | − | 60 | 206 |
| VEGF | 38 | 60 | − | 33 |
| Ki-67 | 10 | 206 | 33 | − |
Таким образом, выбранное сочетание ИГХ маркеров в изучаемой теме «РЖ» представлялось оригинальным и в то же время актуальным. Нет исследования, обозначенного в системах поиска PubMed и Google Scholar, включающего все 4 указанных гистохимических критерия при РЖ (см. табл. 1).
Для ИГХ окраски VEGF-C (реактив KLT 9) были использованы парафиновые блоки. Готовили тонкие срезы, которые обрабатывали раствором 0,3% перекиси водорода в течение 10 мин при комнатной температуре. Для выявления антигена срезы обрабатывали раствором цитрата натрия pH 6,0 и помещали в микроволновую печь. В течение 12 ч при температуре 4 °C во влажной среде обрабатывали первичными антителами (козьи поликлональные VEGF-C антитела; 1:100, «Биотехнология», Санта-Круз, США). Затем срезы промывали трижды в буферном фосфатном растворе в течение 2 мин, на 30 мин при комнатной температуре помещали в раствор хреносодержащей пероксидазы (Envision, DAKO), меченной козьими антителами. Добавляли 3,3-диаминобензидин. Нормальные козьи IGG служили негативным контролем для выявления VEGF-C. Степень интенсивности прокрашивания классифицировалась по четырем категориям: нет (0), слабое (1), умеренное (2) и сильное (3).
Процедура ИГХ окрашивания для изучения других маркеров отличается практически только видом используемых антител: для p53 — это Do-7, m7001, DAKO, Glostrup, Дания, для Her2/new — это с-erB-2 Oncoprotein, Ki-67 — реактив MIB-1.
И хотя для того, чтобы полностью генетически классифицировать данную группу больных (188 радикально оперированных пациентов), пока не хватает данных, значительный интерес представляет взаимоотношение гистологии и иммуногистохимии РЖ.
При анализе по методике χ изучали следующие характеристики взаимоотношений, возникающих в паре гистологическая/ИГХ структура РЖ. Целью исследования являлось отслеживание тенденций, возможность прогнозирования величины одного теста по показателям другого, а также математическое моделирование возможности использовать новый маркер для клинических потребностей.
Для оценки полученных результатов использовали стандартные описательные статистические маркеры оценки диагностических тестов:
- OR;
- чувствительность;
- специфичность;
- PPV;
- NPV;
- PLR;
- NLR.
OR — odds ratio (отношение шансов) — служит для количественного описания того, насколько наличие либо отсутствие признака Х взаимосвязано с наличием или отсутствием свойства Z в некоторой группе. Самое главное, что если OR >1, то данная взаимосвязь считается положительной. В биологических исследованиях OR редко превышает 10. Как будет показано далее, в нашем исследовании ряд OR превосходил 10 в несколько раз. Например, когда речь шла о ценности диагностической взаимосвязи между белком VEGFR-3 и инвазией опухоли в микроскопические сосуды, OR превысил 10 в сотни раз.
Чувствительность — это доля позитивного предиктора в среде тех, где он действительно является позитивным. Например, в случае чувствительности какого-то диагностического маркера 90%, у 9/10 больных он будет изменен (повышен).
Специфичность — это доля нормального значения маркера в среде тех, где он действительно нормален. Например, в случае 80% специфичности, у 8/10 здоровых больных маркер (диагностический тест) будет нормальным. Оба маркера считаются представляющими диагностическую ценность в случае, если они >75%.
Использование нижеследующих маркеров является нововведением в медицинских исследованиях. В научных работах 10–20-летней давности данные маркеры обычно не упоминаются.
PPV — positive predictive value (положительное прогностическое значение) — положительная прогностическая роль или способность правильно прогнозировать положительный результат теста. Это доля больных с положительными результатами теста, у которых установлен верный диагноз с помощью тестируемой диагностической системы.
NPV — negative predictive value (негативное прогностическое значение) — негативная прогностическая роль, способность правильно прогнозировать отрицательный результат теста. Это доля больных с отрицательными результатами теста, у которых с помощью исследуемой диагностической системы правильно установлен отрицательный результат.
Как же истолковывать значения, полученные при исследованиях этих параметров? Четкого ответа в литературе найти не удается. Тем не менее интерпретация другого подобного критерия — знаменитого коэффициента корреляции Пирсона [32] — является таковой:
- <0,2 — очень слабая корреляция;
- 0,2–0,5 — слабая корреляция;
- 0,5–0,7 — средняя корреляция;
- 0,7–0,9 — высокая корреляция;
- >0,9 — очень высокая корреляция.
Однако все гораздо сложнее для следующей группы оценочных критериев.
PLR — positive likelihood ratio (отношение правдоподобия положительного результата теста). Считается, что если результаты отношения правдоподобия >1, то данный положительный результат теста ассоциирован с данным заболеванием. Если же отношение правдоподобия <1, положительный результат ассоциирован с отсутствием заболевания. Таким образом, PLR — это прогнозируемая математически диагностическая ценность вновь открытого маркера для клинических потребностей (табл. 2).
Таблица 2. Математическое толкование прироста PLR
| Отношение правдоподобия | Примерное изменение [83] вероятности, % |
|---|---|
| Значения между 0 и 1 уменьшают вероятность наличия заболевания | |
| 0,1 | −45 |
| 0,2 | −30 |
| 0,3 | −25 |
| 0,4 | −20 |
| 0,5 | −15 |
| 1 | 0 |
| Значения >1 увеличивают вероятность наличия заболевания | |
| 2 | +15 |
| 3 | +20 |
| 4 | +25 |
| 5 | +30 |
| 6 | +35 |
| 7 | |
| 8 | +40 |
| 9 | |
| 10 | +45 |
NLR — negative likelihood ratio (отношение правдоподобия отрицательного результата теста). Негативная диагностическая точность теста. Чем данный показатель ниже, тем выше вероятность корректного исключения диагноза.
Оба эти показателя имеют непосредственное отношение к способности теста прогнозировать результаты, то есть значимость его для дальнейшего клинического применения, важность для клинической практики.
Например, все тот же вышеупомянутый VEGFR-3 имеет показатель «дальнейшей диагностической клинической ценности» PLR 89,333 с 95% доверительным интервалом (confidence interval — CI) 15,867–1728,203, когда речь идет о его способности «прогнозировать» степень гематогенной диссеминации РЖ.
При этом зависимость носит обратный характер: чем выше (нео)лимфангиогенез, тем меньше гематогенная диссеминация по кровеносным капиллярам (V0–V3) и наоборот. Чем ниже (нео)лимфангиогенез, тем больше опухолевых эмболов в капиллярах (табл. 3).
Таблица 3. Исследование гистологических и ИГХ маркеров прогноза при РЖ: опухолевые эмболы и инвазия в кровеносные микрососуды (V)
| p53 V | VEGFR-3 V | Ki-67 V | Her2/new | |||||||||||
| + | − | + | − | + | − | + | − | |||||||
| V0 | 52 | 9 | 67 | 0 | 88 | 0 | 13 | 57 | ||||||
| V1 | 9 | 8 | 0 | 27 | 0 | 13 | 0 | 24 | ||||||
| V2 | 20 | 41 | 14 | 26 | 50 | 12 | 12 | 46 | ||||||
| V3 | 31 | 18 | 0 | 54 | 12 | 13 | 13 | 23 | ||||||
| Σ | 112 | 76 | 81 | 107 | 150 | 38 | 38 | 150 | ||||||
| р | р<0,0001 | р<0,0001 | р<0,0001 | р=0,711 | ||||||||||
| n | 95% CI | n | 95% CI | n | 95% CI | n | 95% CI | |||||||
| OR | 6,452 | 2,776 | 15,411 | 512,071 | 66,910 | 10 719, 582 | 53,935 | 7,619 | 1084,591 | 0,848 | 0,376 | 1,899 | ||
| Чувствительность | 0,464 | 0,409 | 0,503 | 0,827 | 0,774 | 0,839 | 0,587 | 0,560 | 0,587 | 0,342 | 0,209 | 0,496 | ||
| Специфичность | 0,882 | 0,800 | 0,938 | 0,991 | 0,951 | 1,000 | 1,000 | 0,893 | 1,000 | 0,620 | 0,586 | 0,659 | ||
| PPV | 0,852 | 0,751 | 0,923 | 0,985 | 0,922 | 0,999 | 1,000 | 0,954 | 1,000 | 0,186 | 0,114 | 0,269 | ||
| NPV | 0,528 | 0,479 | 0,562 | 0,884 | 0,849 | 0,892 | 0,380 | 0,339 | 0,380 | 0,788 | 0,745 | 0,838 | ||
| PLR | 3,921 | 2,049 | 8,164 | 89,333 | 15,867 | 1728,203 | 22,88 | 3,935 | 442,038 | 0,900 | 0,506 | 1,453 | ||
| NLR | 0,608 | 0,530 | 0,738 | 0,174 | 0,161 | 0,237 | 0,424 | 0,408 | 0,516 | 1,061 | 0,765 | 1,348 | ||
Клиническим выводом может быть, например, учет концентрации онкобелка VEGFR-3 в гастробиоптате как одного из факторов предоперационного планирования обширности удаления лимфоколлекторов при операциях на желудке, наряду с такими важнейшими факторами, как возраст больного, наличие тяжелых сопутствующих заболеваний, степень гистологической дифференцировки (имеются сообщения, что при перстневидно-клеточном раке D2 менее эффективны), преддиагностированные гематогенные метастазы (печень, яичники), определение клинического течения, социально-экономические ограничения и т.д.
Вычисления производились с помощью математических мощностей онлайн-калькуляторов, доступных на сайте http://statpages.info/. Полученные результаты, в зависимости от уровня точности, классифицировали на серую, синюю и красные зоны, как это показано в табл. 3. Серая зона — результат незначимый с точки зрения дальнейшего внедрения в клиническую практику, синяя зона — результат значимый в математическом аспекте, красная зона — высокоуровневый результат. Например, OR <1 является неинформативным, >1 информативным, >1 высокоинформативным. Как видно из приложенной табл. 3, высокоинформативные результаты не являлись редкостью.
Результаты и их обсуждение
Исследование доли больных с различной опухолевой дифференцировкой среди пациентов с РЖ с разной экспрессией ИГХ маркера
Распределение больных РЖ с экспрессией различных факторов было интересно с точки зрения выраженности того или иного маркера в группах: р53+ (49,52%), VEGFR-3+ (43,56%), Ki-67+ (33,33%), Her2/new+ (62,22%). Пациенты имели высокую и умеренную степень гистологической дифференцировки от всех ИГХ тестов с положительной экспрессией. Высокий уровень erbB2 конкретно для данной выборки больных являлся синонимом менее агрессивного течения; в противоположность остальным трем показателям. Почти то же самое, что и для рака грудной железы: Her2/new+, в отличие от тройного негативного рака, все-таки был более благоприятной формой заболевания (Her2, генетический вид рака грудной железы, наряду с люминальным А и В типами).
Подсчет вели не от всех 188 больных, а только от всех позитивных, а потом от всех негативных. р53– (22,89%), VEGFR-3– (35,63%), Ki-67– (65,79%), Her2new– (34,96%): пациенты имели высокую и умеренную степень гистологической дифференцировки от всех ИГХ тестов без экспрессии вообще (табл. 4). Исследовательская работа иногда сопряжена с тем, что какие-то результаты вообще невозможно объяснить или не хватает данных. Например, ясно, почему митотический индекс у большей части g1+g2 больных составлял <30. Такие опухоли медленнее делятся, медленнее прогрессируют, являются, таким образом, более «доброкачественными». Очевидно, что из-за низкого потенциала агрессии больных с VEGFR-3-позитивными опухолями в исследовании было меньше. То же самое относится еще к одному фактору генетической нестабильности — белку р53.
Таблица 4. Исследование гистологических и ИГХ маркеров прогноза при РЖ: степень дифференцировки
| p53 | VEGFR-3 | Ki-67 | Her2/new | |||||||||||||
| + | − | + | − | + | − | + | − | |||||||||
| g1g2 | 52 | 19 | 44 | 31 | 50 | 25 | 28 | 50 | ||||||||
| g3g4 | 53 | 64 | 57 | 56 | 100 | 13 | 17 | 93 | ||||||||
| р | р<0,0001 | р=0,298 | р<0,0001 | р=0,002 | ||||||||||||
| n | 95% CI | n | 95% CI | n | 95% CI | n | 95% CI | |||||||||
| OR | 3,305 | 1,667 | 6,600 | 1,394 | 0,742 | 2,626 | 0,260 | 0,114 | 0,585 | 3,064 | 1,452 | 6,509 | ||||
| Чувствительность | 0,495 | 0,430 | 0,552 | 0,436 | 0,366 | 0,503 | 0,333 | 0,300 | 0,372 | 0,622 | 0,484 | 0,746 | ||||
| Специфичность | 0,771 | 0,688 | 0,843 | 0,644 | 0,563 | 0,722 | 0,342 | 0,211 | 0,496 | 0,650 | 0,607 | 0,689 | ||||
| PPV | 0,732 | 0,636 | 0,816 | 0,586 | 0,493 | 0,677 | 0,667 | 0,600 | 0,745 | 0,359 | 0,280 | 0,430 | ||||
| NPV | 0,547 | 0,488 | 0,538 | 0,496 | 0,433 | 0,556 | 0,115 | 0,071 | 0,167 | 0,845 | 0,789 | 0,896 | ||||
| PLR | 2,163 | 1,380 | 3,510 | 1,223 | 0,836 | 1,808 | 0,507 | 0,380 | 0,739 | 1,780 | 1,233 | 2,400 | ||||
| NLR | 0,655 | 0,532 | 0,828 | 0,877 | 0,689 | 1,127 | 1,949 | 1,265 | 3,323 | 0,581 | 0,369 | 0,849 | ||||
р53+ (50,48%), VEGFR-3+ (56,43%), Ki-67+ (66,67%), Her2/new+ (37,78%): больные имели низкую степень или вообще отсутствовала гистологическая дифференцировка от всех ИГХ тестов с положительной экспрессией (плохой прогноз). Более агрессивные низкодифференцированные опухоли накапливали большее количество белков р53, VEGFR-3 и имели гораздо худшие показатели митотической активности. ИГХ анализ не является генетическим, и по нему нельзя судить о степени мутантности, например, р53, и о каких именно мутациях шла речь. Иммуногистохимическое исследование давало косвенную информацию. Если белка р53 становилось много, значит, существует повышенная экспрессия гена ТР53. Это можно было использовать наряду с обычными гистологическими маркерами.
р53– (77,11%), VEGFR-3– (64,37%), Ki-67– (34,21%), Her2/new– (65,04%): пациенты имели низкую степень или вообще отсутствовала гистологическая дифференцировка от всех ИГХ тестов без экспрессии вообще. Примечательно, что из группы отрицательных значений маркеров отсутствие erbB2 совпадало с анаплазией опухоли.
Исследование онкобелков среди g1g2 и g3g4
Общая процентная структура каждой комбинации маркеров у больных с различной опухолевой дифференцировкой также в ряде случаев требовала истолкования, поскольку здесь соотношение производили со всеми 188 больными, а не отдельно с «положительными» и «отрицательными». Это нужно было для того, чтобы увидеть так называемый общий фон, на котором происходили все события.
Сосудистый белок VEGFR-3 показал позитивную реакцию (из-за редкости его экспрессии положительным считался уровень, начиная с 1+) у g3g4-пациентов в 30,32%, значение 29,79% практически полностью совпало с группой, в которой у таких же больных он был негативным. Отрицательный результат — это тоже результат. В группе с митотическим индексом все было гораздо оптимистичнее: лидер Ki-67+ g3g4 отличался от ближайшего преследователя более чем вдвое с результатом 53,19% больных. Почти то же самое было и в группе Her2/new–: g3g4 — 49,47%.
Исследование доли больных с различной степенью прорастания стенки желудка опухолью среди пациентов с РЖ с разной экспрессией ИГХ маркера
В табл. 5 представлена степень прорастания стенки желудка опухолью у больных РЖ с разной экспрессией ИГХ маркера.
Таблица 5. Исследование гистологических и ИГХ маркеров прогноза при РЖ: агрессивность местного роста (T)
| p53 Т | VEGFR-3 Т | Ki-67 Т | Her2/new | ||||||||||||||
| + | − | + | − | + | − | + | − | ||||||||||
| Т1, Т2 | 30 | 0 | 19 | 18 | 37 | 0 | 0 | 35 | |||||||||
| Т3 | 19 | 0 | 0 | 20 | 25 | 0 | 13 | 14 | |||||||||
| Т4 | 64 | 75 | 72 | 59 | 75 | 51 | 36 | 90 | |||||||||
| Σ | 113 | 75 | 91 | 97 | 137 | 51 | 49 | 139 | |||||||||
| р | р<0,0001 | р<0,0001 | р<0,0001 | р<0,001 | |||||||||||||
| n | 95% CI | n | 95% CI | n | 95% CI | n | 95% CI | ||||||||||
| OR | 27,108 | 3,803 | 547,425 | 21,111 | 2,495 | 466,305 | 18,870 | 2,655 | 380,367 | 0,066 | 0,003 | 0,473 | |||||
| Чувствительность | 0,265 | 0,226 | 0,274 | 0,950 | 0,768 | 0,997 | 0,270 | 0,238 | 0,277 | -0,20 | 0,001 | 0,109 | |||||
| Специфичность | 0,987 | 0,929 | 0,999 | 0,526 | 0,430 | 0,551 | 0,981 | 0,895 | 0,999 | 0,765 | 0,759 | 0,795 | |||||
| PPV | 0,968 | 0,825 | 0,998 | 0,514 | 0,415 | 0,539 | 0,974 | 0,856 | 0,990 | 0,028 | 0,001 | 0,151 | |||||
| NPV | 0,475 | 0,447 | 0,481 | 0,952 | 0,779 | 0,997 | 0,338 | 0,308 | 0,344 | 0,699 | 0,694 | 0,727 | |||||
| PLR | 20,177 | 3,168 | 397,774 | 2,006 | 1,347 | 2,223 | 14,044 | 14,044 | 275,279 | 0,085 | 0,004 | 0,53 | |||||
| NLR | 0,744 | 0,727 | 0,833 | 0,095 | 0,005 | 0,540 | 0,744 | 0,744 | 0,852 | − | − | − | |||||
Теоретически p53 и VEGFR-3 могли бы быть использованы как факторы увеличения шансов выполнения более расширенных операций в длинном списке других, несомненно, более важных хирургических критериев, как например, инфильтративный характер роста опухоли (табл. 6), «плохая» гистология (G3, G4), молодой возраст и др. Как мы уже убедились ранее, значение PLR=20,177 дает более чем 45% прироста вероятности выполнения комбинированной операции при повышении в опухоли концентрации белкового продукта р53. То же самое (14,044) оказывается верным и в отношении фактора пролиферации Ki-67.
Таблица 6. Исследование гистологических и ИГХ маркеров прогноза при РЖ: вид инфильтрирующей активности (Inf) РЖ
| p53 | VEGFR-3 Inf α, βInf γ | Ki-67 Inf α, βInf γ | Her2/new | ||||||||||||||
| + | − | + | − | + | − | + | − | ||||||||||
| Inf α, β | 75 | 41 | 79 | 27 | 122 | 10 | 25 | 90 | |||||||||
| Inf γ | 30 | 42 | 28 | 54 | 34 | 22 | 26 | 47 | |||||||||
| р | р=0,002 | р<0,0001 | р<0,0001 | р=0,044 | |||||||||||||
| n | 95% CI | n | 95% CI | n | 95% CI | n | 95% CI | ||||||||||
| OR | 2,561 | 1,341 | 4,907 | 5,643 | 2,865 | 11,191 | 7,894 | 3,183 | 19,954 | 0,502 | 0,248 | 1,014 | |||||
| Чувствительность | 0,714 | 0,648 | 0,777 | 0,738 | 0,674 | 0,795 | 0,782 | 0,747 | 0,810 | 0,490 | 0,369 | 0,614 | |||||
| Специфичность | 0,506 | 0,422 | 0,585 | 0,687 | 0,581 | 0,742 | 0,688 | 0,518 | 0,824 | 0,343 | 0,298 | 0,389 | |||||
| PPV | 0,647 | 0,586 | 0,703 | 0,745 | 0,680 | 0,803 | 0,924 | 0,883 | 0,957 | 0,217 | 0,164 | 0,272 | |||||
| NPV | 0,583 | 0,486 | 0,674 | 0,659 | 0,574 | 0,733 | 0,393 | 0,296 | 0,471 | 0,644 | 0,559 | 0,730 | |||||
| PLR | 1,446 | 1,120 | 1,872 | 2,215 | 1,609 | 3,085 | 2,503 | 1,552 | 4,601 | 0,746 | 0,526 | 1,003 | |||||
| NLR | 0,565 | 0,382 | 0,835 | 0,393 | 0,276 | 0,561 | 0,317 | 0,231 | 0,487 | 1,486 | 0,992 | 2,118 | |||||
Кроме определения степени дифференцировки первичной опухоли, распространенности опухоли в желудке, прорастания в окружающие структуры и пр., исследовали количество пораженных лимфоузлов по группам № 1–16, наличие опухолевых эмболов в капиллярном русле (V), резидуальной опухолевой ткани (R) (табл. 7).
Таблица 7. Исследование гистологических и ИГХ маркеров прогноза при РЖ: резидуальная остаточная опухолевая болезнь (R)
| p53 | VEGFR-3 R | Ki-67 R | Her2/new | ||||||||||||||
| + | − | + | − | + | − | + | − | ||||||||||
| R− | 96 | 74 | 98 | 10 | 141 | 28 | 42 | 129 | |||||||||
| R+ | 9 | 9 | 3 | 17 | 3 | 16 | 8 | 9 | |||||||||
| р | р=0,626 | р<0,0001 | р<0,0001 | р=0,045 | |||||||||||||
| n | 95% CI | n | 95% CI | n | 95% CI | n | 95% CI | ||||||||||
| OR | 1,297 | 0,445 | 3,781 | 7,933 | 2,080 | 35,505 | 26,875 | 6,709 | 125,108 | 0,366 | 6,120 | 1,125 | |||||
| Чувствительность | 0,914 | 0,876 | 0,953 | 0,970 | 0,925 | 0,992 | 0,979 | 0,949 | 0,994 | 0,840 | 0,760 | 0,917 | |||||
| Специфичность | 0,108 | 0,059 | 0,157 | 0,195 | 0,143 | 0,221 | 0,364 | 0,265 | 0,413 | 0,065 | 0,036 | 0,093 | |||||
| PPV | 0,565 | 0,541 | 0,589 | 0,583 | 0,556 | 0,596 | 0,834 | 0,809 | 0,847 | 0,246 | 0,222 | 0,268 | |||||
| NPV | 0,500 | 0,274 | 0,726 | 0,850 | 0,624 | 0,960 | 0,842 | 0,614 | 0,958 | 0,529 | 0,295 | 0,754 | |||||
| PLR | 1,025 | 0,931 | 1,131 | 1,206 | 1,080 | 1,273 | 1,539 | 1,291 | 1,695 | 0,899 | 0,789 | 1,010 | |||||
| NLR | 0,790 | 0,299 | 2,091 | 0,152 | 0,036 | 0,520 | 0,057 | 0,014 | 0,192 | 2,453 | 0,898 | 6,593 | |||||
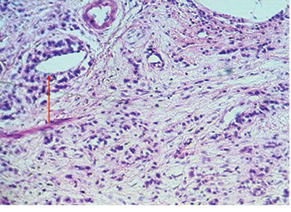
Степень сосудистой вовлеченности классифицировали по JRSGC [84]:
V0 — нет сосудистой инвазии;
V1 — минимальная сосудистая инвазия;
V2 — умеренная сосудистая инвазия;
V3 — выраженная (тяжелая) сосудистая инвазия (рис. 10).
Красным цветом в табл. 5–7 обозначены крупные, с точки зрения медицинской статистики биологических исследований, цифры. Например, OR=27,108 (95% CI 3,803–547,425) для р53 и OR=21,111 (95% CI 2,495–466,305) более характерно для математической точности физико-технических наук. Значительные показатели чувствительности Т/VEGFR-3 и специфичности Т/р53, а также показатели Т/р53/PPV, Т/VEGFR-3/NPV, Т/Ki-67/PLR соответствуют высокому качеству выполненного исследования. При этом практическая значимость полученных данных «супервысокой точности» сомнительна: можно было бы попытаться спрогнозировать скорость роста опухолей по критерию Т для различных концентраций онкобелков, но для этого не хватает данных (см. табл. 4).
Процентное соотношение больных, имевших в исследовании различную степень прорастания опухолью желудочной стенки, выглядит так: р53+ (43,36%), VEGFR-3+ (20,88%), Ki-67+ (27,00%), Her2/new+ (0%) — при прорастании слизистой и подслизистой оболочки опухолью; р53– (0%), VEGFR-3– (39,18%), Ki-67– (0%), Her2/new– (25,18%) — при прорастании слизистой и подслизистой оболочки опухолью; р53+ (56,64%), VEGFR-3+ (79,12%), Ki-67+ (73,00%), Her2/new+ (100%) — при прорастании серозной оболочки опухолью и прорастании в окружающие органы (плохой прогноз); р53– (100%), VEGFR-3– (60,82%), Ki-67– (100%), Her2/new– (74,82%) — при прорастании серозной оболочки опухолью и прорастании в окружающие органы. В целом, более скоростной местно-деструирующий рост характерен для опухолей с большей мутантностью р53, большим митотическим индексом и высокой склонностью к образованию микроскопических сосудов.
Прорастание всей стенки Т4 сравнивали с более ранними стадиями Т1–Т3. Как свидетельствуют данные табл. 8, концентрация онкобелков в местно-распространенных опухолях является выше, чем в более ранних. Возможно, это связано с более длительным периодом существования опухоли большего размера, накопление факторов агрессии происходит медленно. Примечательно наличие результатов «красной зоны»: OR >1, PPV >1.
Таблица 8. Поиск диагностически перспективных среди «оптимистичных» пар маркеров
| OR | Чувствительность | Специфичность | PPV | PLR | NLR |
| Т/p53 = 27,108 (3,803–547,425) | VEGFR-3/Т = 0,952 (0,779–0,997) |
VEGFR-3/V = 0,991 (0,951–1,000) |
VEGFR-3/V = 0,985 (0,922–0,999) |
Ki-67/Т = 14,044 (14,044–275,279) |
Т/VEGF = 0,952 (0,779–0,997) |
| VEGFR-3/Inf = 5,643 (2,865–11,191) | VEGFR-3/Т = 0,950 (0,768–0,997) |
Ki-67/V = 1,000 (0,893–1,000) |
Ki-67/V = 1,000 (0,954–1,000) |
VEGFR-3/V = 89,333 (15,867–1728,203) |
|
| p53/V = 6,452 (2,776–15,411) | VEGFR-3/R = 0,970 (0,925–0,992) |
p53/Т = 0,987 (0,929–0,999) |
PPV/p53/Т = 0,968 (0,825–0,998) |
Ki-67/V/PLR = 22,88 (3,935–442,038) |
|
| VEGFR-3/Т = 21,111 (2,495–466,305) | Т/VEGF = 0,950 (0,768–0,99) |
Т/p53 = 0,987 (0,929–0,99) |
Т/p53 = 0,968 (0,825–0,998) |
p53/Т = 20,177 (3,168–397,774) |
|
| VEGFR-3/V = 512,071 (66,910–10 719,582) | Ki-67/R = 0,979 (0,949–0,994) |
Т/p53 = 20,177 (3,168–397,774) |
|||
| p53/Т = 27,108 (3,803–547,425) | Т/Ki-67 = 14,044 (14,044–275,279) |
||||
| Ki-67/Inf = 7,894 (3,183–19,954) | |||||
| Ki-67/V = 53,935 (7,619–1084,591) | |||||
| Ki-67/R = 26,875 (6,709–125,108) | |||||
| VEGFR-3/R = 7,933 (2,080–35,505) | |||||
| Т/VEGF = 21,111 (2,495–466,305) | |||||
В табл. 8 серым цветом обозначены те математически «оптимистичные» маркеры прогрессирования, которые не имели, по нашему мнению, никакого практического приложения. Они не влияли на частоту микроскопической резидуальной опухолевой болезни, а также на метастазирование в лимфатические узлы (табл. 9), а степень и вид инфильтрации желудочной стенки были более зависимы от других факторов. Черным цветом оставлены те соотношения, чья клиническая значимость была сомнительной. И, наконец, темно-красным — то, что может быть использовано при дальнейшем планировании исследования, в том числе с участием более передовых молекулярно-генетических тестов (MSI).
Таблица 9. Исследование гистологических и ИГХ маркеров прогноза при РЖ: наличие метастазов в регионарных лимфатических узлах
| p53 | VEGFR-3 | Ki-67 | Her2/new | ||||||||||||||
| + | − | + | − | + | − | + | − | ||||||||||
| N0 | 55 | 22 | 55 | 29 | 11 | 17 | 26 | 58 | |||||||||
| N1 | 22 | 23 | 42 | 15 | 42 | 19 | 17 | 27 | |||||||||
| N2 | 22 | 44 | 16 | 28 | 43 | 29 | 15 | 39 | |||||||||
| N3 | 0 | 0 | 1 | 2 | 20 | 7 | 0 | 6 | |||||||||
| Σ | 99 | 89 | 117 | 71 | 116 | 72 | 58 | 130 | |||||||||
| р | р<0,0001 | p=0,234 | р=0,011 | р=1,000 | |||||||||||||
| n | 95% CI | n | 95% CI | n | 95% CI | n | 95% CI | ||||||||||
| OR | 3,807 | 1,952 | 7,472 | 1,447 | 0,766 | 2,738 | 0,339 | 0,137 | 0,830 | 1,009 | 0,516 | 1,969 | |||||
| Чувствительность | 0,556 | 0,485 | 0,618 | 0,482 | 0,421 | 0,541 | 0,095 | 0,055 | 0,140 | 0,448 | 0,337 | 0,563 | |||||
| Специфичность | 0,753 | 0,674 | 0,822 | 0,608 | 0,513 | 0,699 | 0,764 | 0,700 | 0,836 | 0,554 | 0,504 | 0,605 | |||||
| PPV | 0,714 | 0,624 | 0,794 | 0,655 | 0,571 | 0,735 | 0,393 | 0,229 | 0,579 | 0,310 | 0,233 | 0,388 | |||||
| NPV | 0,604 | 0,541 | 0,659 | 0,433 | 0,365 | 0,497 | 0,344 | 0,315 | 0,376 | 0,692 | 0,630 | 0,756 | |||||
| PLR | 2,247 | 1,490 | 3,473 | 1,231 | 0,864 | 1,797 | 0,402 | 0,185 | 0,853 | 1,005 | 0,679 | 1,424 | |||||
| NLR | 0,590 | 0,465 | 0,763 | 0,851 | 0,656 | 1,129 | 1,185 | 1,029 | 1,349 | 0,996 | 0,723 | 1,315 | |||||
Прослеженные тенденции, как в доступности онкогенетических маркеров, так и в их значимости, открывают перспективы дальнейшего развития онкологической науки. Обилие ежемесячно появляющихся доступных экспериментальных, практических, исследовательских данных постоянно пополняет поток медицинской информации. Углубление практической онкологии в генетическую, молекулярную сферу лишь короткое время выглядит отвлеченной от реальностей жизни схоластикой, тут же привнося в повседневную клиническую практику новые, еще более эффективные инструменты в борьбе за жизни пациентов. Выход «кабинетной науки» в люди является событием, значимым как для практикующего онколога, так и для пациента.
Выводы
1. Современное бурное развитие онкологической науки в сфере молекулярно-генетических исследований создает предпосылки для более индивидуального воздействия на опухоль.
2. Обширность ИГХ и генетических данных, получаемых при обследовании больных, рано или поздно выльется в более глубокое понимание биологии РЖ, в том числе в планировании хирургической операции у конкретного больного.
3. Повышение доступности полногеномного секвенирования в ближайшие 3–5 лет выведет изучение генетики РЖ и индивидуализацию лечения на новый уровень.
Список использованной литературы
1. De Silva N., Schulz L., Paterson A. et al. (2015) Molecular effects of Lapatinib in the treatment of HER2 overexpressing oesophago-gastric adenocarcinoma. Br. J. Cancer, 113(9): 1305–1312. doi: 10.1038/bjc.2015.342. Epub 2015 Oct 20. PMID:26484410.
2. Cidon E.U., Ellis S.G., Inam Y. et al. (2013) Molecular targeted agents for gastric cancer: a step forward towards personalized therapy. Cancers (Basel), 5(1): 64–91. doi: 10.3390/cancers5010064.
3. Kawata S., Yashima K., Yamamoto S. et al. (2015) AID (activation-induced cytidine deaminase), p53 and MLH1 expression in early gastric neoplasms and the correlation with the background mucosa. Oncol. Lett., 10(2): 737–743.
4. Liao X., Lochhead P., Nishihara R. et al. (2012) Aspirin use, tumor PIK3CA mutation, and colorectal-cancer survival. N. Engl. J. Med., 367: 1596–1606.
5. Герштейн Е.С., Ли С.Н., Рябов А.Б. и др. (2009) Сравнительное иммуноферментное исследование матриксных металлопротеиназ-2, -7, -9 и их тканевого ингибитора 2 типа в опухолях и плазме крови больных раком желудка. Бюлл. эксп. биол. мед., 148(12): 660–663.
6. Ayral-Kaloustian S., Salaski E.J. (2002) Protein farnesyltransferase inhibitors. Curr. Med. Chem., 9(10): 1003–1032.
7. Gou H.-F., Chen X.-C., Zhu J. et al. (2011) Expressions of COX-2 and VEGF-C in gastric cancer: correlations with lymphangiogenesis and prognostic implications. J. Exp. Clin. Cancer Res., 30(1): 14. PMCID: PMC3037339 (полнотекстовая).
8. Ananiev J., Gulubova M., Manolova I., Tchernev G. (2011) Prognostic significance of HER2/neu expression in gastric cancer. Article (PDF Available) in Wiener klinische Wochenschrift, 123(13–14): 450–454.
9. Jørgensen J.T., Hersom M. (2012) HER2 as a prognostic marker in gastric cancer — a systematic analysis of data from the literature. J. Cancer, 3: 137–144. doi:10.7150/jca.4090 (полнотекстовая).
10. Gravalos C., Jimeno A. (2008) HER2 in gastric cancer: a new prognostic factor and a novel therapeutic target. Ann. Oncol., 19(9): 1523–1529 (полнотекстовая).
11. Rüschoff J., Hanna W., Bilous M. et al. (2012) HER2 testing in gastric cancer: a practical approach. Mod. Pathol., 25: 637–650.
12. Zhang Y.Y., Gu K.S., Wu H.Y. et al. (2015) Correlation of ERCC1 expression in peripheral blood lymphocytes with outcomes of patients with gastric cancer treated with oxaliplatin-based adjuvant chemotherapy. Genet. Mol. Res., 14(4): 15921–15929 (полнотекстовая).
13. Huang Y., Wu P., Liu B., Du J. (2016) Successful personalized chemotherapy for metastatic gastric cancer based on quantitative BRCA1 mRNA expression level: A case report. Oncol. Lett., 11(6): 4183–4186. PMCID: PMC4888084.
14. Kim J.G. (2013) Molecular targeted therapy for advanced gastric cancer. Korean J. Intern. Med., 28(2): 149–155. PMCID: PMC3604602.
15. Muro K., Chung H.C., Shankaran V. et al. (2016) Pembrolizumab for patients with PD-L1-positive advanced gastric cancer (KEYNOTE-012): a multicentre, open-label, phase 1b trial. Lancet Oncol., 17(6): 717–726.
16. Kanayama K., Imai H., Yoneda M. et al. (2016) Significant intratumoral heterogeneity of human epidermal growth factor receptor 2 status in gastric cancer: A comparative study of immunohistochemistry, FISH, and dual-color in situ hybridization. Cancer Sci. Apr., 107(4): 536–542. doi: 10.1111/cas.12886. Epub 2016 Feb 19.
17. Amato M., Perrone G., Righi D. et al. (2016) HER2 status in gastric cancer: comparison between primary and distant metastatic disease. Pathol. Oncol. Res., 30: 1–7.
18. Chen T., Xu X.Y., Zhou P.H. (2016) Emerging molecular classifications and therapeutic implications for gastric cancer. Chin. J. Cancer, 35(1): 49. doi: 10.1186/s40880-016-0111-5. Review. PMID:27233623.
19. Nadauld L.D., Ford J.M. (2013) Molecular profiling of gastric cancer: toward personalized cancer medicine. J. Clin. Oncol., 31(7): 838–839. doi: 10.1200/JCO.2012.47.1714.
20. Stahl P., Seeschaaf C., Lebok P. et al. (2015) Heterogeneity of amplification of HER2, EGFR, CCND1 and MYC in gastric cancer. BMC Gastroenterol., 15: 7.
21. Zhang W. (2014) TCGA divides gastric cancer into four molecular subtypes: implications for individualized therapeutics. Chin. J. Cancer, 33(10): 469–470.
22. Kaneda A., Matsusaka K., Aburatani H., Fukayama M. (2012) Epstein — Barr virus infection as an epigenetic driver of tumorigenesis. Cancer Res., 72(14): 3445–3450. doi: 10.1158/0008-5472.CAN-11-3919.
23. Chen T., Sun Y., Ji P. et al. (2015) Topoisomerase IIα in chromosome instability and personalized cancer therapy. Oncogene, 34(31): 4019–4031. doi: 10.1038/onc.2014.332.
24. He D., Zhang Y.W., Zhang N.N. et al. (2015) Aberrant gene promoter methylation of p16, FHIT, CRBP1, WWOX, and DLC-1 in Epstein — Barr virus-associated gastric carcinomas. Med. Oncol., 32(4): 92.
25. Lugli A., Zlobec I., Singer G. et al. (2007) Napoleon Bonaparte’s gastric cancer: a clinicopathologic approach to staging, pathogenesis, and etiology. Nat. Clin. Pract. Gastroenterol. Hepatol., 4: 52–57.
26. Murphy G., Pfeiffer R., Camargo M.C., Rabkin C.S. (2009) Meta-analysis shows that prevalence of Epstein — Barr virus-positive gastric cancer differs based on sex and anatomic location. Gastroenterol., 137(3): 824–833.
27. Burke A.P., Yen T.S., Shekitka K.M., Sobin L.H. (1990) Lymphoepithelial carcinoma of the stomach with Epstein — Barr virus demonstrated by polymerase chain reaction. Mod. Pathol., 3(3): 377–380.
28. Shigeyasu K., Nagasaka T., Mori Y. et al. (2015) Clinical significance of MLH1 methylation and CpG Island methylator phenotype as prognostic markers in patients with gastric cancer. PLoS One, 10(6):e0130409.
29. Imyanitov E.N., Moiseyenko V.M. (2011) Drug therapy for hereditary cancers. Hered. Cancer Clin. Pract., 9(1): 5.
30. Guastadisegni C., Colafranceschi M., Ottini L., Dogliotti E. (2010) Microsatellite instability as a marker of prognosis and response to therapy: a meta analysis of colorectal cancer survival data. Eur. J. Cancer, 46: 2788–2798.
31. Vilar E., Gruber S.B. (2010) Microsatellite instability in colorectal cancer — the stable evidence. Nat. Rev. Clin. Oncol., 7: 153–162.
32. Li Z., Lai Y., Sun L. et al. (2016) PD-L1 expression is associated with massive lymphocyte infiltration and histology in gastric cancer. Hum. Pathol., 31. pii: S0046-8177(16)30093-4.
33. Laghi L., Bianchi P., Malesci A. (2008) Differences and evolution of the methods for the assessment of microsatellite instability. Oncogene, 27: 6313–6321. doi: 10.1038/onc.2008.217. [PubMed] [Cross Ref].
34. Boland C.R., Goel A. (2010) Microsatellite instability in colorectal cancer. Gastroenterol., 138: 2073–2087. doi: 10.1053/j.gastro.2009.12.064 [PMC free article].
35. Vilar E., Gruber S.B. (2010) Microsatellite instability in colorectal cancer-the stable evidence. Nat. Rev. Clin. Oncol., 7: 153–162.
36. Clark A.J., Barnetson R., Farrington S.M., Dunlop M.G. (2004) Prognosis in DNA mismatch repair deficient colorectal cancer: are all MSI tumours equivalent? Fam. Cancer, 3: 85–91.
37. Popat S., Hubner R., Houlston R.S. (2005) Systematic review of microsatellite instability and colorectal cancer prognosis. J. Clin. Oncol., 23: 609–618.
38. Guastadisegni C., Colafranceschi M., Ottini L., Dogliotti E. (2010) Microsatellite instability as a marker of prognosis and response to therapy: a meta-analysis of colorectal cancer survival data. Eur. J. Cancer, 46: 2788–2798. doi: 10.1016/j.ejca.2010.05.009. [PubMed] [Cross Ref].
39. Hewish M., Lord C.J., Martin S.A. et al. (2010) Mismatch repair deficient colorectal cancer in the era of personalized treatment. Nat. Rev. Clin. Oncol., 7: 197–208. doi: 10.1038/nrclinonc.2010.18 [PubMed] [Cross Ref].
40. Boland C.R., Thibodeau S.N., Hamilton S.R. (1998) A National Cancer Institute workshop on microsatellite instability for cancer detection and familial predisposition: development of international criteria for the determination of microsatellite instability in colorectal cancer. Cancer Res., 58: 5248–5257 [PubMed].
41. Vilar E., Scaltriti M., Balmaña J. et al. (2008) Microsatellite instability due to hMLH1 deficiency is associated with increased cytotoxicity to irinotecan in human colorectal cancer cell lines. Br. J. Cancer, 99: 1607–1612.
42. Papouli E., Cejka P., Jiricny J. (2004) Dependence of the cytotoxicity of DNA-damaging agents on the mismatch repair status of human cells. Cancer Res., 64: 3391–3394. doi: 10.1158/0008-5472.CAN-04-0513.
43. Yamane K., Schupp J.E., Kinsella T.J. (2007) BRCA1 activates a G2-M cell cycle checkpoint following 6-thioguanine-induced DNA mismatch damage. Cancer Res., 67: 6286–6292. doi: 10.1158/0008-5472.CAN-06-2205.
44. Valentini A.M., Armentano R., Pirrelli M., Caruso M.L. (2006) Chemotherapeutic agents for colorectal cancer with a defective mismatch repair system: the state of the art. Cancer Treat. Rev., 32: 607–618. doi: 10.1016/j.ctrv.2006.08.001.
45. Fink D., Zheng H., Nebel S. et al. (1997) In vitro and in vivo resistance to cisplatin in cells that have lost DNA mismatch repair. Cancer Res., 57: 1841–1845.
46. Martin S.A., Hewish M., Sims D. et al. (2011) Parallel high throughput RNA interference screens identify PINK1 as a potential therapeutic target for the treatment of DNA mismatch repair deficient cancers. Cancer Res., 71: 1836–1848. doi: 10.1158/0008-5472.CAN-10-2836.
47. Martin S.A., McCabe N., Mullarkey M. et al. (2010) DNA polymerases as potential therapeutic targets for cancers deficient in the DNA mismatch repair proteins MSH2 or MLH1. Cancer Cell., 17: 235–248. doi: 10.1016/j.ccr.2009.12.046.
48. Martin S.A., McCarthy A., Barber L.J. et al. (2009) Methotrexate induces oxidative DNA damage and is selectively lethal to tumour cells with defects in the DNA mismatch repair gene MSH2. EMBO Mol. Med., 1: 323–337. doi: 10.1002/emmm.200900040.
49. des Guetz G., Schischmanoff O., Nicolas P. et al. (2009) Does microsatellite instability predict the efficacy of adjuvant chemotherapy in colorectal cancer? A systematic review with meta-analysis. Eur. J. Cancer, 45: 1890–1896.
50. Ribic C.M., Sargent D.J., Moore M.J. et al. (2003) Tumor microsatellite-instability status as a predictor of benefit from fluorouracil-based adjuvant chemotherapy for colon cancer. N. Engl. J. Med., 349: 247–257. doi: 10.1056/NEJMoa022289.
51. Sargent D.J., Marsoni S., Monges G. et al. (2010) Defective mismatch repair as a predictive marker for lack of efficacy of fluorouracil-based adjuvant therapy in colon cancer. J. Clin. Oncol., 28: 3219–3226. doi: 10.1200/JCO.2009.27.1825.
52. de Vos tot Nederveen Cappel W.H., Meulenbeld H.J., Kleibeuker J.H. et al. (2004) Survival after adjuvant 5-FU treatment for stage III colon cancer in hereditary nonpolyposis colorectal cancer. Int. J. Cancer, 109: 468–471. doi: 10.1002/ijc.11712.
53. Sinicrope F.A., Sargent D.J. (2009) Clinical implications of microsatellite instability in sporadic colon cancers. Curr. Opin. Oncol., 21: 369–373. doi: 10.1097/CCO.0b013e32832c94bd.
54. de la Chapelle A., Hampel H. (2010) Clinical relevance of microsatellite instability in colorectal cancer. J. Clin. Oncol., 28: 3380–3387. doi: 10.1200/JCO.2009.27.0652.
55. Kim S.T., Lee J., Park S.H. et al. (2010) Clinical impact of microsatellite instability in colon cancer following adjuvant FOLFOX therapy. Cancer Chem. Pharmacol., 66: 659–667.
56. Zaanan A., Cuilliere-Dartigues P., Guilloux A. et al. (2010) Impact of p53 expression and microsatellite instability on stage III colon cancer disease-free survival in patients treated by 5-fluorouracil and leucovorin with or without oxaliplatin. Ann. Oncol., 21: 772–780.
57. Bertagnolli M.M., Niedzwiecki D., Compton C.C. et al. (2009) Microsatellite instability predicts improved response to adjuvant therapy with irinotecan, fluorouracil, and leucovorin in stage III colon cancer: Cancer and Leukemia Group B Protocol 89803. J. Clin. Oncol., 27: 1814–1821. doi: 10.1200/JCO.2008.18.2071.
58. Liang J.T., Huang K.C., Lai H.S. et al. (2002) High-frequency microsatellite instability predicts better chemosensitivity to high-dose 5-fluorouracil plus leucovorin chemotherapy for stage IV sporadic colorectal cancer after palliative bowel resection. Int. J. Cancer, 101: 519–525.
59. Brueckl W.M., Moesch C., Brabletz T. et al. (2003) Relationship between microsatellite instability, response and survival in palliative patients with colorectal cancer undergoing first-line chemotherapy. Anticancer Res., 23: 1773–1777.
60. des Guetz G., Mariani P., Cucherousset J. et al. (2007) Microsatellite instability and sensitivitiy to FOLFOX treatment in metastatic colorectal cancer. Anticancer Res., 27: 2715–2719.
61. Müller C.I., Schulmann K., Reinacher-Schick A. et al.; AIO Colorectal Study Group (2008) Predictive and prognostic value of microsatellite instability in patients with advanced colorectal cancer treated with a fluoropyrimidine and oxaliplatin containing first-line chemotherapy. A report of the AIO Colorectal Study Group. Int. J. Colorectal Dis., 23: 1033–1039.
62. Kim S.T., Lee J., Park S.H. et al. (2010) The effect of DNA mismatch repair (MMR) status on oxaliplatin-based first-line chemotherapy as in recurrent or metastatic colon cancer. Med. Oncol., 27: 1277–1285. doi: 10.1007/s12032-009-9374-x.
63. Fallik D., Borrini F., Boige V. et al. (2003) Microsatellite instability is a predictive factor of the tumor response to irinotecan in patients with advanced colorectal cancer. Cancer Res., 63: 5738–5744.
64. Charara M., Edmonston T.B., Burkholder S. et al. (2004) Microsatellite status and cell cycle associated markers in rectal cancer patients undergoing a combined regimen of 5-FU and CPT-11 chemotherapy and radiotherapy. Anticancer Res., 24: 3161–3167.
65. Bendardaf R., Lamlum H., Ristamäki R. et al. (2007) Mismatch repair status is a predictive factor of tumour response to 5-fluorouracil and irinotecan chemotherapy in patients with advanced colorectal cancer. Tumour Biol., 28: 212–220. doi: 10.1159/000107417.
66. Kim J.E., Hong Y.S., Ryu M.H. et al. (2011) Association between deficient mismatch repair system and efficacy to irinotecan-containing chemotherapy in metastatic colon cancer. Cancer Sci. (in press).
67. James P.A., Mitchell G., Bogwitz M., Lindeman G.J. (2013) The Angelina Jolie effect. Med. J., 99(10): 646.
68. Kriege M., Jager A., Hooning M.J. et al. (2012) The efficacy of taxane chemotherapy for metastatic breast cancer in BRCA1 and BRCA2 mutation carriers. Cancer, 118(4): 899–907.
69. Moiseyenko V.M., Chubenko V.A., Moiseyenko F.V. et al. (2014) Evidence for clinical efficacy of mitomycin C in heavily pretreated ovarian cancer patients carrying germ-line BRCA1 mutation. Med. Oncol., 31(10): 199. doi: 10.1007/s12032-014-0199-x. Epub 2014 Sep 4.
70. Munroe M., Kolesar J. (2016) Olaparib for the treatment of BRCA-mutated advanced ovarian cancer. Am. J. Health Syst. Pharm., 73(14): 1037–1041.
71. Nanda R., Chow L.Q., Dees E.C. et al. (2016) Pembrolizumab in patients with advanced triple-negative breast cancer: phase Ib KEYNOTE-012 Study. J. Clin. Oncol., 2. pii: JCO648931. [Epub ahead of print].
72. Moliterni A., Ménard S., Valagussa P. et al. (2003) HER2 overexpression and doxorubicin in adjuvant chemotherapy for resectable breast cancer. doi: 10.1200/JCO.2003.04.021. JCO, 21(3): 458–462 (http://jco.ascopubs.org/content/21/3/458.full).
73. Huang G., Chen S., Wang D. et al. (2016) High Ki67 expression has prognostic value in surgically-resected T3 gastric adenocarcinoma. Clin. Lab., 62(1–2):141–53.
74. Sheffield B.S., Garratt J., Kalloger S.E. et al. (2014) HER2/neu testing in gastric cancer by immunohistochemistry: assessment of interlaboratory variation. Arch. Pathol. Lab. Med., 138(11): 1495–1502. doi: 10.5858/arpa.2013-0604-OA.
75. Penault-Llorca F., André F., Sagan C. et al. (2009) Ki67 expression and docetaxel efficacy in patients with estrogen receptor-positive breast cancer. J. Clin. Oncol., 27(17): 2809–2815. doi: 10.1200/JCO.2008.18.2808. Epub 2009 Apr. 20.
76. Cao W., Fan R., Yang W., Wu Y. (2014) VEGF-C expression is associated with the poor survival in gastric cancer tissue. Tumor Biology, 35(4): 3377–3383.
77. Tsai H.L., Lin C.H., Huang C.W. et al. (2015) Decreased peritherapeutic VEGF expression could be a predictor of responsiveness to first-line FOLFIRI plus bevacizumab in mCRC patients. Int. J. Clin. Exp. Pathol., 8(2): 1900–1910.
78. Ishikawa M., Kitayama J., Kazama S., Nagawa H. (2016) Expression of vascular endothelial growth factor C and D (VEGF-C and -D) is an important risk factor for lymphatic metastasis in undifferentiated early gastric carcinoma. Jap. J. Clin. Oncol., 33 (1): 21–27 (полнотекстовая).
79. Yonemura Y., Endo Y., Tabata K. et al. (2005) Role of VEGF-C and VEGF-D in lymphangiogenesis in gastric cancer. Int. J. Clin. Oncol., 10(5): 318–327.
80. Qiao G.L., Qi W.X., Jiang W.H. et al. (2016) Prognostic significance of circulating tumor cells in esophageal carcinoma: a meta-analysis. Onco Targets Ther., 9: 1889–1897.
81. Tsai W.S., Chen J.S., Shao H.J. et al. (2016) Circulating tumor cell count correlates with colorectal neoplasm progression and is a prognostic marker for distant metastasis in non-metastatic patients. Sci. Rep., 6: 24517.
82. Gao Z.H., Wang Q.Q. (2015) Curative effect of paclitaxel and cisplatin combined chemotherapy on cervical cancer and its relation with tissue micro vascular and lymphatic vessels density. Pak. J. Pharm. Sci., 28(5 Suppl.): 1849–1852.
83. McGee S. (2002) Simplifying likelihood ratios. J. Gen. Intern. Med.,17(8): 647–650.
84. Japanese Classification of Gastric Carcinoma — 2 English Edition — Japanese Gastric Cancer Association (1998) Gastric Cancer, 1: 10–24.
Адрес:
Машуков Артем Алексеевич
65055, Одесса, ул. Неждановой, 32
КУ «Одесский областной онкологический диспансер»
E-mail: mashukster@gmail.com














Leave a comment