Результати хірургічного лікування при вторинних ураженнях хребта
Бойчук С.І.1, Дєдков А.Г.1, Самоненко Ю.М.2, Волков І.Б.1, Максименко Б.В.1, Васильєв О.В.1, Дорожинський В.І.1
- 1Національний інститут раку, Київ
- 2Науково-практичний центр ендоваскулярної нейрорентгенохірургії НАМН, Київ
Резюме. Вступ. Ураження хребців кістковими метастазами в онкологічних хворих відмічають у 30–40% випадків. У структурі пухлинної патології хребта саме метастатичне його ураження становить до 96% та переважно локалізується в грудному відділі, що обумовлене гематогенним шляхом метастазування більшості злоякісних новоутворень. Мета: покращення якості життя даної категорії хворих за допомогою хірургічного лікування пухлин хребців шляхом зниження інтенсивності больового синдрому, попередження незворотних неврологічних змін у вигляді парезів та паралічів, відновлення втраченої рухової функції кінцівок. Матеріали та методи. Прооперовано 27 хворих з метастатичним ураженням хребців, чоловіків — 15 (55,6%), жінок — 12 (44,4%), середній вік хворих — 48,9±2,4 року. Перед хірургічним лікуванням усім пацієнтам проводилося повне клінічне обстеження, що включало оцінку кісткової та вісцеральної дисемінації, загального стану хворого, вираженості больового синдрому (за візуальною аналоговою шкалою), якості життя (за шкалою Karnofski), неврологічного статусу (за шкалою Frankel), очікуваної тривалості життя (за прогностичною шкалою Tokuhashi). Результати. Оцінка результатів хірургічного лікування хворих проводилася відповідно до ортопедичних та онкологічних критеріїв. Покращення неврологічного статусу після хірургічного лікування досягнуто у 19 (70,37%) хворих, неврологічний статус у 3 (11,2%) пацієнтів не змінився. Погіршення неврологічної симптоматики відмічено у 5 (18,51%) хворих. Підвищення якості життя відмічено у 17 (62,96%) хворих, погіршення — у 3 (11,2%). Не відмічено динаміки у 7 (25,92%) прооперованих хворих. Середня виживаність хворих на метастатичний нирково-клітинний рак становила 8,1 ± 1,64 міс. При порівнянні показників фактичної та прогнозованої виживаності (за шкалою Tokuhashi) виявилося, що очікувана 1-річна виживаність фіксувалася на рівні 21%, а фактична — 27%. Середня тривалість життя хворих з кістковими метастазами раку передміхурової залози становила 15,2 ± 3,2 міс. За прогностичною шкалою Tokuhashi очікувана 1-річна виживаність зафіксована на позначці 42%, а фактична — 67%. Висновки. Отримані дані свідчать про значну роль паліативного хірургічного лікування вторинних кісткових уражень хребта, що суттєво підвищує якість життя хворих (62,96%) шляхом зниження інтенсивності больового синдрому (до 81,48%), відновлення неврологічних та рухових функцій кінцівок (у 70,37% випадків). У решти хворих — негативна динаміка у зв’язку з генералізацією пухлинного процесу.
DOI: 10.32471/clinicaloncology.2663-466X.43-3.28232
Одержано 26.10.2021
Прийнято до друку 6.11.2021
Вступ
Ураження хребців кістковими метастазами (КМ) у онкологічних хворих відмічається в 30–40% випадків. У структурі пухлинної патології хребта саме метастатичне його ураження складає до 96% та переважно локалізується в грудному відділі, що обумовлено гематогенним шляхом метастазування більшості злоякісних новоутворень [1]. Найбільш поширеною причиною, що різко погіршує якість життя пацієнтів, є виражений біль та неврологічні розради, що виникають внаслідок компресії спинного мозку [2–4]. Компресія спинного мозку з розвитком плегій та парезів є найбільш небезпечним ускладненням та діагностується у 5–10% усіх онкологічних хворих [5, 6]. Як правило, прогноз для пацієнтів з метастазами в хребетний стовп є досить незадовільним, незважаючи на наявну таргетну терапію при деяких пухлинах. Так, 5-річна виживаність становить 9% порівняно з 30% виживаності у пацієнтів з метастазами в трубчасті кістки [7, 8].
Хірургічне лікування є основним методом спеціальної терапії при патологічних переломах хребців, особливо в гострий період, коли є компресія спинного мозку, що попереджає незворотні неврологічні зміни на відміну від консервативного лікування за допомогою хіміотерапії, променевої терапії, радіонуклідної терапії радіофармпрепаратами, гормонотерапії та використання бісфосфонатів [9–13]. Зважаючи на тип ураження, а саме множинне чи солідне метастатичне ураження, обсяг оперативного втручання, як правило, відрізняється. Так, при солідному пошкодженні можливе повне видалення метастазу зі збереженням принципів абластичності, при множинному ураженні хірургічна мета в основному полягає в стабілізації хребетного стовпа та декомпресії нервових структур від пухлинних мас [7].
Метою нашої роботи було підвищення якості життя даної категорії хворих за допомогою хірургічного лікування пухлин хребців шляхом зниження інтенсивності больового синдрому, попередження незворотних неврологічних змін у вигляді парезів та паралічів, відновлення втраченої рухової функції кінцівок.
Матеріали та методи
У науково-дослідному відділенні онкоортопедії прооперовано 27 хворих з метастатичним ураженням хребців: чоловіків — 15 (55,6%), жінок — 12 (44,4%), середній вік хворих — 48,9±2,4 року. Перед хірургічним лікуванням усім пацієнтам проводили повне клінічне обстеження, що включало в себе оцінку кісткової та вісцеральної дисемінації, загального стану хворого, вираженості больового синдрому (за візуальною аналоговою шкалою), якості життя (за шкалою Karnofski), неврологічного статусу (за шкалою Frankel), очікуваної тривалості життя (за прогностичною шкалою Tokuhashi) [14, 15]. Розподіл хворих за нозологічними формами та локалізацією ураження хребців представлено в табл. 1.
Таблиця 1. Нозологічні форми та локалізація ураження хребців
| Нозологічна форма | Кількість хворих | Локалізація ураження хребців | Відсоток від загальної кількості | ||
| Th | L | S | |||
| Нирково-клітинний рак | 7 | 4 | 3 | 0 | 25,92 |
| Рак передміхурової залози | 5 | 3 | 2 | 0 | 18,51 |
| Рак грудної залози | 4 | 2 | 2 | 0 | 14,81 |
| Саркоми кісток та м’яких тканин | 4 | 1 | 2 | 1 | 14,81 |
| Рак легені | 3 | 2 | 0 | 1 | 11,12 |
| Рак прямої кишки | 2 | 0 | 1 | 1 | 7,4 |
| Рак носоглотки | 1 | 1 | 0 | 0 | 3,7 |
| Рак матки | 1 | 1 | 0 | 0 | 3,7 |
| Усього | 27 | 14 | 10 | 3 | 100 |
Найчастіше відмічали кісткові метастази нирково-клітинного раку (25,92%) та раку передміхурової залози (18,51%). Солітарне ураження хребців діагностовано у 4 (14,81%), поодиноке — у 5 (18,51%) хворих. Переважали хворі з множинними кістковими метастазами — 18 (66,7%). Вісцеральні метастази відмічали у 13 (48,14%) хворих.
Оцінка якості життя хворих здійснювалася за шкалою Karnofski до початку та після проведеного хірургічного лікування. У табл. 2 представлені дані оцінки загального стану хворих до початку лікування.
Таблиця 2. Оцінка загального стану хворих за шкалою Karnofski
| Показник | Бал | Кількість хворих | Відсоток від загальної кількості |
| Практично здоровий | 100 | 0 | 0 |
| Мінімальні симптоми | 90 | 4 | 14,81 |
| Задовільна активність, чіткі симптоми | 80 | 5 | 18,51 |
| Самостійно обслуговує себе, але не може працювати | 70 | 4 | 14,81 |
| Не постійно потребує допомоги | 60 | 6 | 22,3 |
| Потребує сторонньої допомоги | 50 | 3 | 11,2 |
| Глибока інвалідність | 40 | 5 | 18,51 |
| Усього | 27 | 100 |
Незначне зниження якості життя (Karnofski — 80–90%) відмічалось у 9 (33,4%) хворих; 10 (37,03%) пацієнтів до операції могли самостійно обслуговувати себе (Karnofski — 60–70%); 5 (18,51%) хворих потребували сторонньої допомоги (Karnofski — <50%).
Поява больового синдрому була першою ознакою захворювання у 14 (51,85%) хворих. Середня тривалість больового синдрому від моменту появи болю до діагностування КМ в хребцях становила 6,5 ± 3,3 міс (від 1 до 36 міс). Середній термін повної компресії спинного мозку — 9,4 ± 2,1 діб (від 1 до 28 діб). Дані про вираженість неврологічного дефіциту у хворих до хірургічного лікування представлено в табл. 3. Оцінка вираженості больового синдрому за шкалою ВАШ до хірургічного лікування представлена в табл. 4.
Таблиця 3. Оцінка неврологічного дефіциту
| Вираженість неврологічного дефіциту | За Frankel | Кількість хворих | Відсоток від загальної кількості |
| Плегія | A | 7 | 25,92 |
| Виражений парапарез | B | 3 | 11,2 |
| Помірний парапарез | C–D | 8 | 29,62 |
| Без неврологічних порушень | E | 9 | 33,4 |
| Усього | 27 | 100 |
Таблиця 4. Оцінка больового синдрому за візуальною аналоговою шкалою до лікування
| Вираженість болю, мм | Кількість хворих | Відсоток від загальної кількості |
| 0–31 | 4 | 14,81 |
| 31–50 | 3 | 11,2 |
| 51–70 | 7 | 25,92 |
| 71–90 | 8 | 29,62 |
| ≥91 | 5 | 18,51 |
| Усього | 27 | 100 |
У більшої половини хворих переважала ламінектомія, декомпресія спинного мозку — 14 (51,85%); ламінектомію, декомпресію та транспедикулярну стабілізацію проведено третині хворих — 9 (33,3%); ламінектомію, декомпресію, корпоректомію, ендопротезування хребців здійснено у хворих з солітарними КМ — 4 (14,81%). Розподіл хворих за типом хірургічних втручань представлено в таблиці 5.
Таблиця 5. Види хірургічних втручань у хворих
| Тип хірургічного втручання | Кількість хворих | Відсоток від загальної кількості |
| Ламінектомія, декомпресія спинного мозку | 14 | 51,85 |
| Ламінектомія, декомпресія, транспедикулярна стабілізація | 9 | 33,3 |
| Ламінектомія, декомпресія, корпоректомія, ендоендопротезування | 4 | 14,81 |
Очікувана тривалість життя 16 (59,25%) хворих становила 6 міс. У 4 (14,81%) пацієнтів очікувана тривалість життя склала більше 12 міс. Прогноз виживаності за шкалою Tokuhashi представлено в табл. 6.
Таблиця 6. Розподіл хворих з метастатичним ураженням хребта за прогностичною шкалою Tokuhashi
| Бал | Кількість хворих | Відсоток від загальної кількості |
| 0–8 | 16 | 59,25 |
| 9–11 | 7 | 25,92 |
| 12–15 | 4 | 14,81 |
| Усього | 24 | 100 |
Результати
Оцінка результатів хірургічного лікування хворих проводилася за ортопедичними та онкологічними критеріями. До ортопедичних критеріїв належали: оцінка якості життя, ступінь вираженості больового синдрому та неврологічного дефіциту до та після хірургічного лікування.
До онкологічних критеріїв віднесено: виникнення локального рецидиву пухлини, прогресування захворювання, виживаність хворих. Проведена оцінка виживаності та тривалості життя хворих за шкалою Tokuhashi для метастатичних пухлин. Динаміка неврологічного статусу хворих (за Frankel) після хірургічного лікування представлена в табл. 7 [16].
Таблиця 7. Динаміка неврологічного статусу хворих (за Frankel)
| Неврологічний статус | Кількість хворих | Відсоток від загальної кількості |
| Покращення | 19 | 70,37 |
| Без динаміки | 3 | 11,2 |
| Погіршення | 5 | 18,51 |
| Усього | 27 | 100 |
Покращення неврологічного статусу після хірургічного лікування досягнуто у 19 (70,37%) хворих, неврологічний статус в 3 (11,2%) пацієнтів не змінився. Погіршення неврологічної симптоматики відмічено у 5 (18,51%) хворих. Зміна якості життя після хірургічного лікування представлена в табл. 8.
Таблиця 8. Зміна якості життя після хірургічного лікування (за Karnofski)
| Якість життя | Кількість хворих | Відсоток від загальної кількості |
| Покращення | 17 | 62,96 |
| Без динаміки | 7 | 25,92 |
| Погіршення | 3 | 11,2 |
| Усього | 27 | 100 |
Покращення якості життя відмічено у 17 (62,96%) хворих, погіршення — у 3 (11,2%). Не відмічено динаміки у 7 (25,92%) прооперованих хворих. Динаміку вираженості больового синдрому представлено в табл. 9.
Таблиця 9. Динаміка вираженості больового синдрому після хірургічного лікування за візуальною аналоговою шкалою
| Вираженість болю | Кількість хворих | Відсоток від загальної кількості |
| Без динаміки | 3 | 11,2 |
| Зниження інтенсивності болю | 22 | 81,48 |
| Посилення болю | 2 | 7,4 |
| Усього | 27 | 100 |
З-під спостереження вибуло 3 (11,2%) хворих. Середній термін спостереження за пацієнтами становив 36 ± 8,2 міс.
Аналіз виживаності хворих у нашому дослідженні зроблено в найбільших групах хворих (КМ нирково-клітинного раку та раку передміхурової залози) та співставлено отримані дані з результатами прогностичної шкали Tokuhashi.
Середня виживаність хворих на метастатичний нирково-клітинний рак становила 8,1 ± 1,64 міс. Під час порівняння показників фактичної та прогнозованої виживаності (за шкалою Tokuhashi) виявилося, що очікувана 1-річна виживаність становила 21%, а фактична — 27%. Середня тривалість життя хворих з КМ раку передміхурової залози становила 15,2 ± 3,2 міс. За прогностичною шкалою Tokuhashi очікувана 1-річна виживаність становила 42%, а фактична — 67%.
Висновки
Отримані дані свідчать про значну роль паліативного хірургічного лікування вторинних кісткових уражень хребта, що суттєво підвищує якість життя хворих (62,96%) шляхом зниження інтенсивності больового синдрому (до 81,48%), відновлення неврологічних та рухових функцій кінцівок (у 70,37% випадків). У решти хворих — негативна динаміка у зв’язку з генералізацією пухлинного процесу.
Співпадіння результатів фактичної та очікуваної тривалості життя хворих дозволяє запропонувати використання прогностичної шкали Tokuhashi для розрахунку показників виживаності у хворих з КМ нирково-клітинного раку.
У подальшому використання консервативних методів спеціального лікування (хіміотерапія, променева терапія, радіонуклідна терапія радіофармпрепаратами, гормонотерапія, бісфосфонати) дозволяє підвищити якість та подовжити тривалість життя даної категорії хворих.
Клінічні випадки
Хвора М. 1989 р.н. (32 роки). Звернулася за допомогою до НІР 11.01.2021 р. зі скаргами на біль у попереково-крижовому відділі хребта з іррадіацією в праву ногу. Хворіє з вересня 2020 р., коли помітила ниючий біль у попереку. У грудні 2020 р. гінекологом за місцем проживання діагностовано пухлину заочеревинного простору справа, хвору направлено в НІР. Клініко-рентгенологічно (за даними комп’ютерної (КТ) та магнітно-резонансної томографії (МРТ) діагностовано пухлину заочеревинного простору справа з інвазією m.ileopsoas dexter, L4 хребця, інтимне прилягання до v.cava inferior (рис. 1).
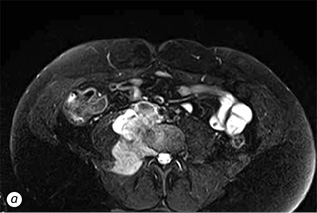
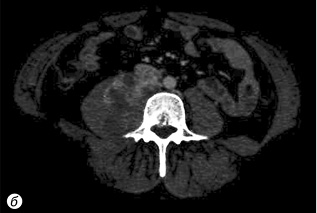
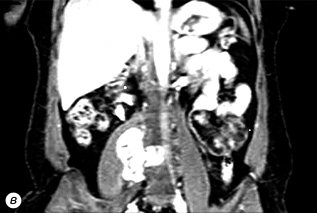
За даними трепан-біопсії пухлини має місце лейоміосаркома (G-2) (патологогістологічний висновок від 13.01.2021 р. № 852/21). Хвору представлено на мультидисциплінарному консиліумі за участю абдомінального хірурга та нейрохірурга. Хворій показано хірургічне лікування в обсязі транспедикулярної стабілізації хребців L3–L5, ламінектомії, видалення саркоми заочеревинного простору справа з корпоректомією L4 хребця, ендопротезування титановим кейджем. Остаточну хірургічну тактику вирішено визначити інтраопераційно. При інвазії пухлиною (v.cava inferior) буде проведено резекцію вени та протезування. 23.03.2021 р. хвору прооперовано, при ревізії — v.cava inferior інтактна. Хворій виконано транспедикулярну стабілізацію хребців L3–L5, ламінектомію, видалення саркоми заочеревинного простору справа з корпоректомією L4 хребця, ендопротезування титановим кейджем з двох доступів (заднього — першим етапом та переднього — другим етапом) (рис. 2).
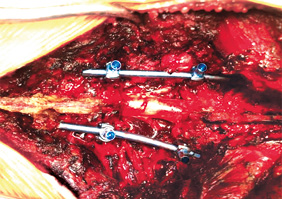
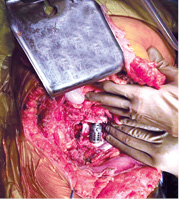
Контрольна рентгенографія поперекового відділу хребта представлена на рис. 3.
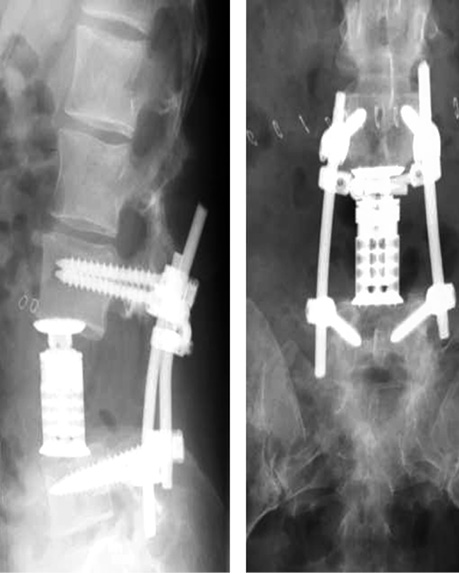
Післяопераційні рани зажили первинно, шви знято на 14-ту добу після операції. Внаслідок проведеної операції загальний стан хворої покращився, больовий синдром відсутній, відмічається незначна парестезія правої кінцівки. Враховуючи умовно-радикально проведену операцію та ступінь диференціювання пухлини (G-2) подальшого спеціального лікування хвора не потребувала, в задовільному стані виписана додому. Хворій проводяться реабілітаційні заходи за місцем проживання. Клініко-рентгенологічно протягом 9 міс ознак прогресування не відмічено.
Хворий К. 1970 р.н. (51 рік). Звернувся за допомогою в НІР зі скаргами на ниючий біль у грудному відділі хребта, парестезію лівої руки. Вищевказані симптоми турбують хворого протягом 4 міс з тенденцією до наростання. З анамнезу відомо, що у 2009 р. хворий отримав комбіноване спеціальне лікування з приводу раку правої нирки (нефректомія, ад’ювантна імунотерапія). Клініко-рентгенологічно (за даним СКТГ та МРТ) діагностовано солітарне метастатичне ураження Th4 хребця, патологічний перелом, компресію спинного мозку на цьому рівні (рис. 4).
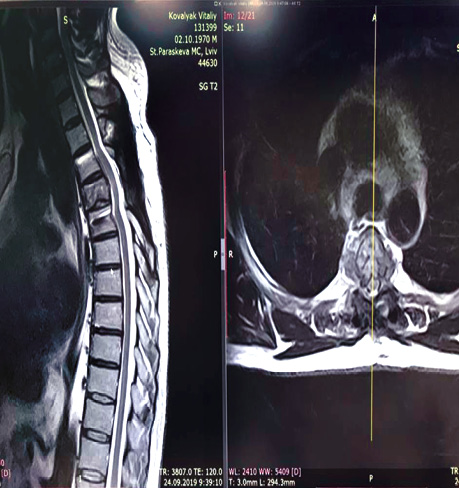
Хворого представлено на мультидисциплінарному консиліумі за участю нейрохірурга та торакального онкохірурга. Вирішено провести хірургічне лікування в обсязі транспедикулярної стабілізації хребців Th3–L5, ламінектомії, корпоректомії хребця Th4 з пухлиною, ендопротезування. 02.10.2019 р. хворого прооперовано, виконано транспедикулярну стабілізацію Th3–Th5 хребців, ламінектомію, корпоректомію Th4 хребця з пухлиною, ендопротезування титановим кейджем (рис. 5).
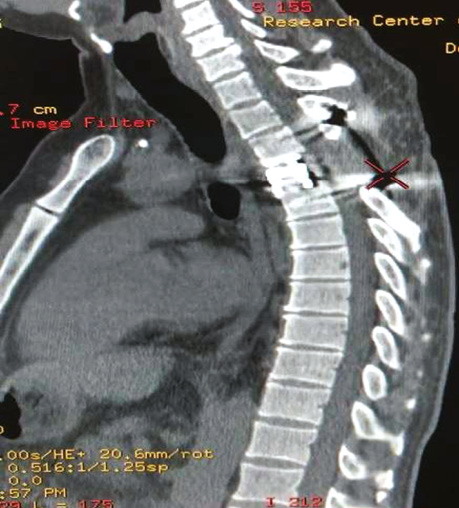
Післяопераційна рана зажила первинно, шви знято на 14-ту добу після хірургічного втручання. Внаслідок проведеної операції загальний стан хворого значно покращився, больовий синдром відсутній, неврологічної симптоматики немає. Ад’ювантно хворий протягом 24 міс отримує бісфосфонати, клініко-рентгенологічно — ознак прогресування не зафіксовано.
Список використаної літератури
1. Кулага, А. В., Мусаев, Э. Р., Валиев, А. К., Борзов К. А., Кабардаев, Р. М., & Алиев, М. Д. (2015). Факторы прогноза при метастатическом поражении позвоночника. Cаркомы костей, мягких тканей и опухоли кожи, 79(3), 34–44.
2. Тепляков, В. В., Шапошников, А. А., & Сергеев, П. С. (2016). Частота востребованности хирургического компонента в комплексном лечении метастатического поражения костей. Саркомы костей, мягких тканей и опухоли кожи, 1, 16–28.
3. Тепляков, В. В., Карпенко, В. Ю., & Бухаров, А. В. (2010). Результаты хирургического лечения пациентов с метастазами в длинные трубчатые кости. Саркомы костей, мягких тканей и опухоли кожи, 3, 10–15.
4. Радченко, В. О., Куценко, В. О., Попов, А. І., Карпінський, М. Ю., & Карпінська, О. Д. (2017). Моделювання варіантів транспедикулярної фіксації грудного відділу хребта при резекції одного-трьох хребців. Травма, 18(5), 95–102. doi: 10.22141/1608-1706.5.18.2017.114125.
5. Алиев, М. Д., Степанова, А. М., Мусаев, Э. Р., Валиев, А. К., & Гуторов, С. Л. (2015). Метастатическое поражение позвоночника у больных раком молочной железы. Факторы прогноза. Сибирский онкологический журнал, 3, 61–67.
6. Cameron, C., Pron, G., Moher, D., & Coyle, D. (2016). Vertebral Augmentation Involving Vertebroplasty or Kyphoplasty for Cancer-Related Vertebral Compression Fractures: A Systematic Review. Ontario Health Technology Assessment Series, 16(11), 1–202. Retrieved from: https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4902848.
7. Заборовский, Н. С., Кострицкий, С. В., Пташников, Д. А., & Широкорад, В. И. (2017). Метастатическое поражение позвоночника на фоне почечно-клеточного рака: результаты лечения и выживаемость после удаления опухоли. Хирургия позвоночника, 14(4), 110–116.
8. Sørensen, S. T., Kirkegaard, A. O., Carreon, L., Rousing, R., & Andersen, M. Ø. (2019). Vertebroplasty or kyphoplasty as palliative treatment for cancer-related vertebral compression fractures: a systematic review. The Spine Journal, 19(6), 1067–1075. Retrieved from: https://pubmed.ncbi.nlm.nih.gov/30822527.
9. Лешко, М. М., Слинько, Є. І., & Хонда, О. М. (2016). Результати лікування метастатичних пухлин крижової кістки. XVI конгрес світової федерації українських лікарських товариств. Берлін-Київ.
10. Лешко, М. М., & Слинько, Є. І. (2016). Технологія та результати видалення пухлин крижів єдиним блоком. Клінічна хірургія, 12 (896), 58–60.
11. Кострицкий, С. В., Широкорад, В. И., Семенов, Д. В., Пташников, Д. А., Щупак, М. Ю., Махсон, А. Н., … Митрофанов, П. П. (2014). Хирургическое лечение больных с метастазами рака почки в позвоночник. Онкоурология, 3, 40–42.
12. Du, Z. Y., Zang, J., Tang, X. D., & Guo, W. (2010). Experts’agreementon therapy for bone metastases. Orthopedic surgeons, 2(4), 241–253. doi: 10.1111/j.1757-7861.2010.00095.x.
13. Ассоциация нейрохирургов России. (2016). Клинические рекомендации по лечению пациентов с метастатическим поражением позвоночника. Методические рекомендации: Москва. Режим доступа: http://www.mst.ru/information/manual/spinal_metastasis.pdf.
14. Tokuhashi, Y., Matsuzaki, H., Toriyama, S., Kawano, H., & Oshaka, S. (2000). Scoring system for preoperative evaluation of metastatic spine tumor prognosis. Spine, 15(11), 1110-3. doi: 10.1097/00007632-199011010-00005.
15. Watkins, R. G., Brien, J. P. O, & Jones, D. (1986). Comparisons of preoperative and postoperative MMPI data in chronic back pain patient. Spine, 11(4), 385-90. doi: 10.1097/00007632-198605000-00018.
16. Frankel, H. L., Hancock, D. O., Hyslop, G., Melzak, J., Michaelis, L. S., Ungar, G. H., … Walsh, J. J. (1969). The value of postural reduction in the initial management of close dinjuries of the spine with paraplegia and tetraplegia. Paraplegia, 1969, 7(3), 179–192. doi: 10.1038/sc.1969.30.
Адреса:
Бойчук Сергій Іванович
03022, Київ, вул. Ломоносова, 33/43
Національний інститут раку
E-mail: sergeyboichuk@yahoo.com
Correspondence:
Boichuk Sergey
33/43 Lomonosova str., Kyiv 03022
National Cancer Institute
E-mail: sergeyboichuk@yahoo.com














Leave a comment