Порівняльний аналіз та оцінка діагностичної ефективності сцинтиграфічного, морфологічного та метаболічного зображення для виявлення йод-негативних метастазів та рецидивів диференційованого раку щитоподібної залози
Солодянникова О.І.1, Даниленко В.В. 1, Кметюк Я.В.2
- 1Державне некомерційне підприємство «Національний інститут раку», Київ, Україна
- 2Всеукраїнський центр радіохірургії при лікарні «Феофанія» Державного управління справами, Київ, Україна
Резюме. Мета. Розробити алгоритм післяопераційного ведення хворих з йод-негативними метастазами диференційованого раку щитоподібної залози (ДРЩЗ). Матеріали та методи дослідження. Обстежено 115 хворих з йод-негативними метастазами ДРЩЗ, з яких сцинтиграфію всього тіла (СВТ) з технецієм (99mTс) сестамібі (Technetium-99m sestamibi — 99mTc-MIBI) проведено 30 пацієнтам, СВТ з технецієм (99mTс) димеркаптосукциновою кислотою (Technetium-99m-dimercaptosuccinic acid — 99mTc-DMCA) — 30, позитронно-емісійну томографію (ПЕТ) з 18F-фтордезоксиглюкозою (ФДГ) ПЕТ — 30, комп’ютерну томографію (КТ) — 25. 10 пацієнтам з групи, в якій проводилася СВТ з 99mTc-MIBI, додатково було проведено комплексне сцинтиграфічне дослідження з 99mTc-пертехнетатом, яке включало динамічну та статичну сцинтиграфії з метою одержання ангіографічних кривих з метастатичними вогнищами ДРЩЗ. Для діагностики йод-негативних метастазів ДРЩЗ використовували наступні методики із застосуванням нейодних радіофармацевтичних препаратів (РФП), а саме мічені 99mTc-MIBI, 99mTc-DMCA та 99mTc-пертехнетатом. Результати. Порівняльна оцінка йод-негативних РФП, КТ та ПЕТ / КТ з 18F-ФДГ виявила найбільш високі відсотки чутливості і специфічності сцинтиграфічного зображення при ПЕТ / КТ з 18F-ФДГ, що становили 92,8±11,2 та 89,4±9,2 відповідно. Висновки. Доведено, що створення та використання алгоритму післяопераційного ведення хворих з йод-негативними формами ДРЩЗ дозволять вчасно виявляти рецидиви та метастази і проводити відповідне лікування, а саме хірургічне, променеве та таргетне.
Одержано 11.02.2026
Прийнято до друку 20.02.2026
DOI: 10.32471/clinicaloncology.2663-466X.35444
ВСТУП
За даними світової наукової літератури, розвиток йод-негативних метастазів відмічається у 7–25% випадків [1, 2]. Незважаючи на широкий спектр діагностичних методик для виявлення метастазів та рецидивів ДРЩЗ, проблема їх ранньої діагностики, прогнозування і лікування залишається нерозв’язаною, а пошуки найбільш оптимального діагностичного алгоритму післяопераційного ведення таких хворих є надзвичайно актуальними [3].
Можливості сцинтиграфії щитоподібної залози з 99mTc-пертехнетатом у виявленні йод-негативних метастазів ДРЩЗ дещо обмежені, оскільки мінімальний розмір вогнища, що візуалізується, становить 1 см. При діаметрі 1,5 см метастаз виявляється лише в 37% випадків. Для підвищення специфічності сцинтиграфічного дослідження використовували двофазне радіонуклідне дослідження з РФП з носієм та без. При цьому інформативність методики виявлення йод-негативних метастазів вдалося підвищити до наступних величин: чутливість становила 55–83% при специфічності 65–75% і точності 67–77% [3]. Однак з появою нових носіїв для 99mTc двофазні радіонуклідні дослідження потребують подальшого вивчення.
КТ використовується для виявлення вогнищ невеликих розмірів і одержання інформації про взаємовідношення метастазів з навколишніми анатомічними структурами при післяопераційному обстеженні хворих на ДРЩЗ. Проте часто виникають проблеми з диференційною діагностикою післяопераційних рубцевих змін і рецидиву пухлини, а також неспецифічного збільшення лімфовузлів і їх метастатичного ураження [4]. Для розв’язання подібних проблем доцільно використовувати радіонуклідні методи дослідження.
Найбільшу діагностичну значущість для виявлення метастазів у пацієнтів з негативним результатом 131I-сканування та високим рівнем тиреоглобуліну (Тg) має ПЕТ з 18F-ФДГ [5]. У середньому чутливість ПЕТ для ідентифікації йод-негативного вогнища становить 70–90% [6]. Важливість виявлення таких вогнищ за допомогою ПЕТ змінює тактику лікування хворих на йод-негативні форми ДРЩЗ, включно з повторною операцією чи променевою терапією замість радіойодотерапії (РЙТ).
За даними деяких авторів, чутливість та специфічність 131I-позитивних метастазів становлять 65%, специфічність — 100% відповідно. Для 131I-негативних ці показники становили: чутливість — 85%, специфічність — 100%. Дані щодо чутливості ПЕТ у виявленні 131I-негативних рецидивів і метастазів залежно від рівня тиреотропного гормону (ТТГ) різняться. Водночас інші автори не відмітили різниці в результатах ПЕТ при різних рівнях ТТГ: M. Schlumberger, M. Brose, T. Trubek та співавт. встановили, що введення рекомбінантного ТТГ достовірно підвищує чутливість ПЕТ-дослідження [7–9].
Останнім десятиріччям в європейській та американській онкології широко досліджується можливість використання найновіших діагностичних технологій для виявлення рецидивів та метастазів у хворих з йод-негативними вогнищами при ДРЩЗ. Так, консенсусною групою S.J. Rosenbaum-Krumme та співавт. вперше вивчалося застосування 18F-ФДГ ПЕТ / КТ при плануванні лікування ДРЩЗ з високим рівнем ризику розвитку метастазів та спостереженні цих пацієнтів після першого курсу РЙТ [10]. Дійшли висновку про більш високі можливості 18F-ФДГ ПЕТ / КТ у виявленні метастазів ДРЩЗ, включно з інсидентальними вогнищами. В інших дослідженнях [11] проводився порівняльний аналіз можливостей гібридних діагностичних модальностей на етапі постабляційного моніторингу хворих на ДРЩЗ. Встановлено, що такі методики, як однофотонна емісійна комп’ютерна томографія (ОФЕКТ) / КТ та ПЕТ / КТ значно підвищують діагностичний рівень спостереження та зменшують кількість псевдопозитивних результатів. Інші дослідники порівнювали можливості ультразвукового (УЗД), сцинтиграфічного досліджень (99mTc-MIBI та 18F-ФДГ ПЕТ / КТ) у виявленні лімфатичних вузлів при пролонгації ДРЩЗ. Вивчався також вплив застосування 18F-ФДГ ПЕТ / КТ на зміну лікувальної стратегії у хворих з ДРЩЗ. У роботі, опублікованій у 2015 р. [12], наведені результати порівняльного аналізу можливостей таких інноваційних технологій, як 18F-ФДГ ПЕТ / КТ та 18F-ФДГ ПЕТ / магнітно-резонансна томографія (МРТ) у виявленні метастазів у легені у хворих з негативними йодними сканами.
Радіойодрефрактерні форми ДРЩЗ, за останніми статистичними даними, становлять близько 5% від загальної кількості хворих на тиреоїдний рак. Для прикладу, у Франції кожен рік з’являється близько 250 пацієнтів з первинною або вторинною йодрефрактерністю. Здебільшого це особи старшого віку, з великою кількістю метастатичних вогнищ і ознаками зниження диференціації пухлинних клітин. Також є дані про те, що у пацієнтів з рефрактерним ДРЩЗ у середньому через 3–6 років розвиваються віддалені метастази і 10-річна виживаність становить лише 10%.
Усі пацієнти, ліковані йодом 131, контролюються рівнем Тg, відсотком накопичення 131I у вогнищах на постлікувальному скані або розміром пухлини на анатомічному зображенні КТ чи МРТ.
Більшість пацієнтів йодрефрактерним ДРЩЗ розподіляються на 4 категорії:
- особи з метастатичною формою, у яких відсутнє накопичення йоду на момент першої РЙТ. У цій групі РЙТ неефективна;
- пацієнти, у яких зменшення накопичення йоду відмічається після декількох курсів РЙТ. У таких хворих диференціація тиреоцитів зберігається, однак відсоток накопичення РФП у вогнищі знижується;
- хворі, у яких накопичення йоду в деяких вогнищах зберігається, але не у всіх. Це, як правило, пацієнти, у яких попередньо проведено ПЕТ / КТ або КТ і при неефективній РЙТ відмічалося накопичення 18F-ФДГ [13];
- особи з метастазами, у яких прогресує втрата чутливості до 131I та знижується ефективність РЙТ.
Останніми роками інтенсивно розробляються діагностичні та лікувальні алгоритми для пацієнтів з рефрактерними формами ДРЩЗ. Групою авторів розроблені основи менеджменту рефрактерного ДРЩЗ.
Один із варіантів ведення хворих на рефрактерний ДРЩЗ складається з наступних етапів:
- супресивна гормональна терапія тироксином під контролем рівня ТТГ <0,1 мОд/л;
- за необхідності — лікування (променеве) окремого локусу;
- діагностичне дослідження з одержанням зображення кожні 4–6 міс;
- при стабілізації — повторні обстеження
У разі прогресування >20% (RECIST) в інтервалі 6–12 міс — назначається таргетна терапія першої лінії (сорафеніб, нексавар).
Загалом алгоритм ведення рефрактерного ДРЩЗ складається з 2 етапів:
- 1-й етап — встановлення РР-форми ДРЩЗ за відсутності накопичення 131I на посттерапевтичному скані, безпосередньо в tumor foci та збільшення об’ємів пухлинних вогнищ за іншими методами дослідження;
- 2-й етап — індикація системної терапії за розмірами пухлини та швидкістю прогресування.
Мета: розробити алгоритм післяопераційного ведення хворих з йод-негативними метастазами диференційованого раку щитоподібної залози.
МАТЕРІАЛИ ТА МЕТОДИ ДОСЛІДЖЕННЯ
У групу дослідження залучено 115 хворих з йод-негативними метастазами ДРЩЗ, з яких проведено СВТ з 99mTc-MIBI — 30 хворим, СВТ з 99mTc-DMCA — 30, ПЕТ з 18F-ФДГ — 30, КТ — 25.
Десяти пацієнтам з групи, в якій проведено СВТ з 99mTc-MIBI, додатково виконано комплексне сцинтиграфічне дослідження з 99mTc-пертехнетатом, яке включало динамічну та статичну сцинтиграфії з метою отримання ангіографічних кривих з метастатичними вогнищами ДРЩЗ.
Для діагностики йод-негативних метастазів ДРЩЗ використовували наступні методики з використанням нейодних РФП, а саме мічені 99mTc-MIBI, 99mTc-DMCA та 99mTc-пертехнетатом.
Методика з 99mTc-MIBI. 99mTc-MIBI в індикаторній дозі 450–500 МБк вводився внутрішньовенно. Дослідження проводилися на гамма-камері з використанням низькоенергетичного паралельного коліматора високого розрішення при налаштуванні на фотопік 140 кеВ і шириною вікна дискримінації 10%. Запис діагностичного зображення здійснювався через 40–60 хв після внутрішньовенного введення 450–500 МБк з 99мТс-MIBI з наступними параметрами:
- розмір матриці 128×128;
- швидкість просування столу залежно від маси тіла пацієнта становила 6–10 см/хв;
- включена функція розпізнавання контуру тіла.
За необхідності здійснювалася планарна прицільна сцинтиграфія з 99мТс-MIBI з розміром матриці 128×128 і набором не менше ніж 250 000 імпульсів на кадр.
Методика з 99mTc-DMCA. 99mTc-DMCA в індикаторній дозі 450–500 МБк вводився внутрішньовенно. Дослідження проводилися на гамма-камері з використанням низькоенергетичного паралельного коліматора високого розрішення при налаштуванні на фотопік 140 кеВ і шириною вікна дискримінації 10%. Запис діагностичного зображення здійснювався через 40–60 хв після внутрішньовенного введення 450–500 МБк з 99mТс-DMCA з наступними параметрами:
- розмір матриці 256×256;
- швидкість просування столу залежно від маси тіла пацієнта становила 6–10 см/хв;
- включена функція розпізнавання контуру тіла.
У разі необхідності здійснювалася планарна прицільна сцинтиграфія з 99mТс- DMCA з розміром матриці 256×256 і набором не менше ніж 500 000 імпульсів на кадр.
Методика з 99mTc-пертехнетатом. Дослідження проводилися з елюатом 99mTc-пертехнетату, що отримувався з генераторів виробництва «Polatom» (Польща).
Дослідження включало послідовне виконання непрямої радіонуклідної ангіографії, динамічної та статичної сцинтиграфії або ОФЕКТ. Радіонуклідну ангіографію виконували безпосередньо після внутрішньовенного болюсного введення 99mTc-пертехнетату активністю 300–400 МБк протягом 60 с, запис проводили на матрицю 256×256 зі швидкістю 1 кадр/с. Укладення хворих здійснювалося таким чином, щоб у полі зору детектора знаходилася зона шиї та органи грудної порожнини. Після закінчення ангіографії проводилася динамічна сцинтиграфія протягом 30 хв зі швидкістю 1 кадр/хв на матрицю 256×256, яка по завершенні доповнювалася статичною сцинтиграфією в передній і задній прямих, бокових, а за необхідності й косих проєкціях або ОФЕКТ.
Отримані дані оброблялися за допомогою комп’ютерного забезпечення «Syngo» (фірма Siemens Healthcare). Комп’ютерна обробка містила стандартні операції контрастування зображень, кадрової алгебри, побудову «зон інтересу», кривих «активність — час», визначення коефіцієнтів відносного накопичення РФП «осередок / фон». Побудова кривих «активність — час» дозволяла виявити оптимальні інтервали для сумації кадрів, а проведення статичної сцинтиграфії в декількох проєкціях або ОФЕКТ — підвищити точність топографічної діагностики. При виявленні осередкових ділянок гіперфіксації РФП в зоні шиї та середостіння за даними динамічної та статичної сцинтиграфій оцінювали результати радіонуклідної ангіографії. У разі гіперваскуляризації осередків гіперфіксації РФП в ангіографічну фазу діагностували наявність йод-негативних метастазів.
Усім хворим радіонуклідні дослідження виконували на дводетекторній гамма-камері фірми Mediso (Угорщина) та однофотонному емісійному комп’ютерному томографі «E. CAM 180» фірми Siemens (Німеччина).
ПЕТ / КТ обстеження складається з декількох етапів: консультативний запис пацієнта та визначення протоколу обстеження; підготовка пацієнта до ПЕТ / КТ; проведення ПЕТ- / КТ-обстеження; аналіз результатів; відпочинок пацієнта після обстеження і видача висновку у вигляді твердої копії.
Перед проведенням обстеження проводиться вимірювання зросту та маси тіла пацієнта. Останні повинні бути визначені точно, оскільки на їх основі визначається рівень накопичення РФП.
Перед дослідженням проводиться контроль рівня глюкози в плазмі крові, і лише після встановлення допустимих показників <11 ммоль/л або <200 мг/дл дослідження ПЕТ з 18F-ФДГ може бути виконаним. Якщо рівень глюкози в плазмі крові становить >11 ммоль/л, дослідження має бути перенесене. Аналіз крові на рівень глюкози повинен бути виконаний за допомогою каліброваного і затвердженого методу, оскільки використовується в якості поправки при визначенні рівня накопичення РФП. Для клінічних досліджень рекомендовані верхні показники рівня глюкози в межах 7–8,3 ммоль/л.
Дозування РФП здійснюється стандартним методом, виходячи з маси тіла пацієнта. Введення препарату здійснюється внутрішньовенно з подальшим промиванням місця ін’єкції 10 мл фізіологічного розчину.
Під час ін’єкції 18F-ФДГ і подальшої фази поглинання РФП пацієнт повинен сидіти або лежати спокійно, щоб мінімізувати накопичення 18F-ФДГ у м’язах. З метою мінімізації накопичення 18F-ФДГ у «бурій жировій тканині» увесь час пацієнт має перебувати в теплому приміщенні.
Для хворих з цукровим діабетом (ЦД) визначається особливий протокол залежно від типу захворювання. При I типі ЦД дослідження може бути заплановане на пізній ранок чи опівдні. Для пацієнтів, що знаходяться на безперервній інфузії інсуліну, обстеження має бути заплановане на ранній ранок. При II типі ЦД ПЕТ-дослідження рекомендується проводити пізнім ранком.
Показник активності 18F-ФДГ визначається типом сканування та розраховується згідно з масою тіла. Так, у разі 2D-сканування — 5 МБк/кг маси тіла, у випадку 3D-сканування — 2,5 МБк/кг маси тіла. У середньому при масі тіла 75–80 кг і введеній активності 180 МБк ефективна доза опромінення при ПЕТ-дослідженні становить близько 6–11 мЗв. Складова від 18F-ФДГ дорівнює близько 3–4 мЗв, решта належить до КТ.
Рекомендований інтервал між часом введення 18F-ФДГ та початком сканування становить 60 хв. Зміни часового інтервалу повинні чітко фіксуватися, оскільки від цього залежить вимірювання показників накопичення РФП.
Стандартна діагностична КТ з внутрішньовенним введенням контрастної речовини здійснюється відповідно до затверджених методик: після низькодозової КТ та ПЕТ-збору даних.
Лікар з ядерної медицини оцінює зображення ПЕТ та КТ на екрані спеціалізованої робочої станції. Пакети програмного забезпечення дозволяють візуалізувати зображення ПЕТ, КТ та ПЕТ / КТ, поєднувати їх в аксіальній, коронарній та сагітальній площинах. Наявність або відсутність аномального накопичення 18F-ФДГ оцінюються поєднано з його розміром та інтенсивністю. Стандартизований показник накопичення (SUV) використовується як додаток до візуальної оцінки і розраховується за формулою:
| SUV = | Actvoi (kBq/ml) |
| Actadministered (MBq)/BW (kg) |
де Actvoi – активність, виміряна в обсязі інтересу;
Actadministered – введена активність з поправкою на фізичний розпад 18F-ФДГ;
BW – маса тіла.
Статистичну обробку отриманих даних виконували за допомогою пакетів програм «Axum v 5.0», «Statistica v 5.0».
ОТРИМАНІ РЕЗУЛЬТАТИ ТА ЇХ ОБГОВОРЕННЯ
Обстежено 60 хворих з ДРЩЗ, з них у 30 проведено СВТ з 99mTc-MIBI, у 30 пацієнтів з 99mTc-DMCA з метою оцінки діагностичної ефективності сцинтиграфічного зображення.
Наводимо клінічний приклад СВТ з 99mTc-MIBI у пацієнта з йодрефрактерністю за результатами останніх постлікувальних сканувань (рис. 1).
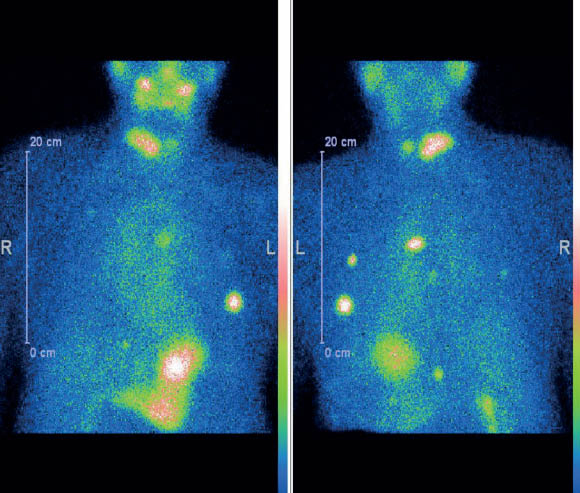
Рис. 1. СВТ з 99mTc-MIBI, локальний рецидив ДРЩЗ та множинне ураження легень (йод-негативні вогнища)
Після проведення діагностичного обстеження пацієнту призначено таргетну терапію препаратом Нексавар. Подальший моніторинг ефективності протипухлинного лікування проводився за допомогою СВТ з 99mTc-MIBI.
При проведенні ПЕТ / КТ з 18F-ФДГ пухлинні вогнища візуалізуються у вигляді осередків гіперфіксації 18F-ФДГ. Метастази в регіонарних лімфатичних вузлах, скелеті, легенях та інших органах також виглядають як осередки гіперфіксації 18F-ФДГ.
Обстежували пацієнтів з підозрою на метастази ДРЩЗ, але без виявлення їх на скані (діагностичному чи постлікувальному) з 131I-NaI. Ознаками можливої пролонгації захворювання були показники ТГ та ТТГ, а також дані УЗД та КТ. У середньому обстеженим хворим проведено від 5 до 8 курсів РЙТ. У 42% з них відмічено відсутність накопичення радіойоду в лімфатичних вузлах шиї, у 10% — легенях, у 8% — кістках. У всіх пацієнтів відсутність накопичення йоду встановлена на 2 останніх постлікувальних сканах. З метою підтвердження наявності чи відсутності вогнищ, виявлених іншими методами діагностики, хворим проводили ПЕТ / КТ з 18F-ФДГ.
Наступними етапами обстеження було проведення топограми, низькодозової КТ (від голови до дна таза) та КТ з контрастним посиленням. Після чого проводився запис ПЕТ-дослідження, суміщення зображень апаратними методами та інтерпретація результатів.
В якості ілюстрації наводимо клінічні випадки проведення ПЕТ / КТ з 18F-ФДГ у пацієнтів з йод-негативними вогнищами ДРЩЗ, виявленими іншими методами дослідження.
Хворий А., папілярний рак щитоподібної залози, 4 курси РЙТ, відсутність накопичення 131I-NaI на постлікувальному скані після 3-го курсу. За даними УЗД та КТ обстеження — підозра на можливі вогнища в зоні шиї та легень. Хворому призначено ПЕТ / КТ з 18F-ФДГ (рис. 2).
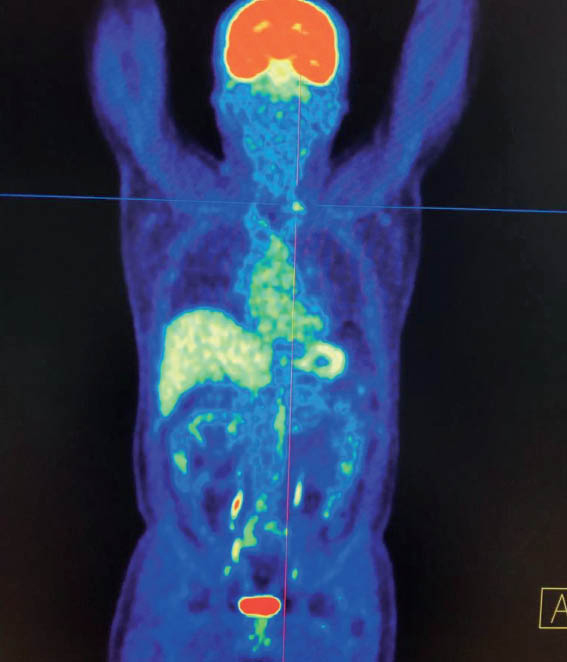
Рис. 2. ПЕТ / КТ з 18F-ФДГ. Візуалізується вогнище в зоні шиї
За даними ПЕТ / КТ з 18F-ФДГ у цього пацієнта підтверджена наявність вогнища гіперфіксації РФП в зоні шиї, водночас не виявлено ознак пролонгації процесу в легенях. Вірогідно, знайдені вогнища, за даними КТ, відповідають фіброзним змінам після перенесених запальних процесів.
Проведений порівняльний аналіз ефективності нейодних РФП та ПЕТ / КТ при йодрефрактерних формах ДРЩЗ.
Вивчення діагностичної ефективності нейодних РФП у діагностиці йод-негативних метастазів ДРЩЗ та проведення порівняльного аналізу виявили наступні результати (табл. 1, 2).
| Показник ефективності | 99mTc-MIBI |
| Чутливість, % | 90,6 |
| Специфічність, % | 100,0 |
| Точність, % | 95,4 |
| Показник ефективності | 99mTc-DMCA |
| Чутливість, % | 85 |
| Специфічність, % | 100,0 |
| Точність, % | 86,2 |
Як видно з представлених таблиць, 99mTc-MIBI характеризується більш високими показниками чутливості, специфічності та точності. Водночас 99mTc-DMCA, вірогідно, має нижчі показники чутливості та точності при збереженні максимального показника специфічності.
Отже, порівняння показників інформативності СВТ з нейодними РФП, ПЕТ з 18F-ФДГ та рентгенівської КТ виявило, що найвищий показник чутливості характерний для ПЕТ з 18F-ФДГ. Специфічність найбільш висока (100,0%) при СВТ з 99mTc-MIBI і 99mTc-DMCA. Рентгенівська КТ у виявленні йод-негативних метастазів ДРЩЗ характеризується достовірно нижчими показниками як чутливості, так і специфічності та точності (табл. 3).
| Показник ефективності | ПЕТ з 18F-ФДГ | КТ |
| Чутливість, % | 93,1 | 66,5 |
| Специфічність, % | 80,4 | 56,2 |
| Точність, % | 90,2 | 59,8 |
ВИСНОВКИ
- Проведені дослідження підтвердили можливість використання методик з нейодними РФП (99mTc-MIBI, 99mTc-DMCA) для виявлення йод-негативних метастазів ДРЩЗ.
- ПЕТ / КТ з 18F-ФДГ є високоінформативною методикою виявлення йод-негативних метастазів ДРЩЗ при пролонгації процесу в легені.
- Порівняльна оцінка йод-негативних РФП, КТ та ПЕТ / КТ з 18F-ФДГ виявила найбільш високі відсотки чутливості та специфічності сцинтиграфічного зображення при ПЕТ / КТ з 18F-ФДГ, що становили 92,8±11,2 та 89,4±9,2 відповідно.
- Створення та використання алгоритму післяопераційного ведення хворих з йод-негативними формами ДРЩЗ дозволить вчасно виявляти рецидиви та метастази і проводити відповідне лікування, а саме хірургічне, променеве та таргетне.
список ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
- Зелінська, Г. В., Кулиніченко, Г. М., & Устименко, Г. Я. (2016). Субклональна структура популяції тироцитів радіойодрефрактерних та радіойодчутливих метастазів папілярного раку щитоподібної залози. Український радіологічний журнал, 3, 15–18. [Zelinska, G. V., Kulynichenko, G. M., & Ustymenko, G. Ya. (2016). Subklonalʹna struktura populyatsiyi tyrotsytiv radioyodrefrakternykh ta radioyodchutlyvykh metastaziv papilyarnoho raku shchytopodibnoyi zalozy. Ukrainian Radiological Journal, 3, 15–18. Ukrainіan].
- Avram, A. M. (2012). Radioiodine scintigraphy with SPECT/KT: an important diagnostic tool for thyroid cancer staging and risk stratification. The Journal of Nuclear Medicine, 53, 754–764. doi: 10.2967/jnumed.111.104133.
- Bible, K. C., Suman, V. J., Molina, J. R., Smallridge, R. C., Maples, W. J., Menefee, M. E., … Erlichman, C. (2010). Efficacy of pazopanib in progressive, radioiodine-refractory, metastatic differentiated thyroid cancer results of a phase 2 consortium study. Lancet Oncology, 11(10), 962–972. doi: 10.1016/S1470-2045(10)70203-5.
- Car, I. I., Mankoff, D. A., Goulart, B. H., Eaton, K. D., Capell, P. T., Kell, E. M., … Martins, R. G. (2010). Phase II study of daily sunitinib in FDG-PET-positiv, iodine-refractory thyroid cancer and metastatic medullary carcinoma of the thyroid with functional imaging correlation. Clinical Cancer Research, 6(21), 5260–5268. doi: 10.1158/1078-0432.CCR-10-0994.
- Deandries, D., Leboulleux, S., Dromain, C., Auperin, A., Coulot, J., Lumbroso, J., … de Baère, T. (2011). Role FDG PET/KT and chest CT in the follow-up of lung lesions treated with radiofrequency ablation. Radiology, 258(1), 270–276. doi: 10.1148/radiol.10092440.
- Robbins, R. J., Wan, Q., Grewal, R. K., Reibke, R., Gonen, M., Strauss, H. W., … Larson, S. M. (2006). Real-time prognosis for metastatic thyroid carcinoma based on 2-18Fflouro-2-deoxy-D-glucose positron emission tomography scanning. Journal of Clinical Endocrinology & Metabolism, 91(2), 498–505. doi: 10.1210/jc.2005-1534.
- Rothenberg, S. M., McFadden, D. G., Palmer, E. L., Daniels, G. H., & Wirth, L. J. (2015). Redifferentiation of iodine-refractory BRAF V600E-mutant metastatic papillary thyroid cancer with dabrafenib. Clinical Cancer Research, 21(5), 1028–1035. doi: 10.1158/1078-0432.CCR-14-2915.
- Schlumberger, M., & Brose, M. (2014). Definition and management of radioactive iodine-refractory differentiated thyroid cancer. Lancet Diabetes Endocrinol, 2, 356–358. doi: 10.1016/S2213-8587(13)70215-8.
- Trubek, T., Kowalska, A., Lesiak, J., & Młynarczyk, J. (2014). The role of 18F-fluorodeoxyglucose positron emission tomography in patients with suspected recurrence or metastatic differentiated thyroid carcinoma with elevated serum thyroglobulin and negative I-131 whole body scan. Nuclear Medicine Review. Central & Eastern Europe, 17(2), 87–93. doi: 10.5603/NMR.2014.0023.
- Rosenbaum-Krumme, S. J., Görges, R., Bockisch, A., & Binse, I. (2012). 18FDG-PET/CT changes therapy in high-risk DTC after first radioiodine. European Journal of Nuclear Medicine and Molecular Imaging, 39(9), 1373–1380. doi: 10.1007/s00259-012-2065-4.
- Wierts, R., Brans, B., Havekes, B., Kemerink, G. J., Halders, S. G., Schaper, N. N., … Jentzen, W. (2016). Dose-Response Relationship in Differentiated Thyroid Cancerpatients Under-going Radioiodine Treatment Assessed by Means of 124I PET/CT. Journal of Nuclear Medicine, 57(7), 1027–1032. doi: 10.2967/jnumed.115.168799.
- Афанасьєва, Н. І., & Луховицька, Н. І. (2008). Порівняння інформативності сцинтиграфії з 99mTc-пертехнетатом, 99mTc-МІВІ та 99mTc-(V)DMSA у візуалізації йодонегативних метастазів та/або рецидивів диференційованого тиреоїдного раку. Український радіологічний журнал, 16(2), 146–152. [Afanasʹyeva, N. I. & Lukhovytsʹka, N. I. (2008). Porivnyannya informatyvnosti stsyntyhrafiyi z 99mTc-pertekhnetatom, 99mTc-MIVI ta 99mTc-(V)DMSA u vizualizatsiyi yodonehatyvnykh metastaziv ta/abo retsydyviv dyferentsiyovanoho tyreoyidnoho raku. Ukrainian Radiological Journal, 16(2), 146–152. Ukrainіan].
- Bannas, P., Derlin, T., Groth, M., Apostolova, I., Adam, G., Mester, J., & Klutmann, S. (2012). Can (18)F-FDG PET/CT be generally recommended in patients with differentiated thyroid carcinoma and elevated thyroglobulin levels but negative 131I wholebody scan? Annals of Nuclear Medicine, 26(1), 77–85. doi: 10.1007/s12149-011-0545-4.
Адреса для листування:
Солодянникова Оксана Іванівна
03022, Київ, вул. Здановської Юлії, 33/43
Державне некомерційне підприємство «Національний інститут раку»
E-mail: oik2000@ukr.net
Correspondence:
Oksana Solodyannykova
33/43 Yulii Zdanovskoi str., Kyiv, 03022
Nonprofit Organization National Cancer Institute
E-mail: oik2000@ukr.net














Leave a comment