Фактори ризику розвитку післяопераційних пневмоній у пацієнтів після операцій з резекції легень
Перконос А.П., Стабровська І.М.
Резюме. Мета. Визначити фактори ризику розвитку післяопераційної пневмонії (ПОП) у пацієнтів після резекції легень. Матеріали та методи дослідження. Проведено ретроспективний аналіз 166 випадків резекції легень у пацієнтів, прооперованих у Державному некомерційному підприємстві (ДНП) «Національний інститут раку» в період із червня до грудня 2023 р. Критерії виключення: пневмонектомія, діагностичні атипові резекції, комбіновані втручання з резекцією ребер або грудної стінки, дитячий вік. Діагноз ПОП встановлювали на підставі рентгенологічних даних. Для оцінки супутньої патології використано індекс коморбідності Чарлсона. Статистичний аналіз включав описову статистику, point-biserial (точково-бісеріальну) кореляцію, χ²-тест та мультиваріативну логістичну регресію (програмне забезпечення Python 3.12, бібліотеки Pandas, SciPy та Statsmodels). Рівень значущості p <0,05. Результати. ПОП зареєстровано у 38 пацієнтів (22,9%), що призводило до подовження госпіталізації в середньому на 3,26 доби (середня тривалість лікування осіб з ПОП — 13,11 доби; без ПОП — 9,85 доби). Значущими факторами ризику виявилися вищий індекс коморбідності (rpb=0,18; p=0,02), наявність метастазів (χ²=4,82; p=0,03) та нижчий абсолютний об’єм форсованого видиху за 1-шу секунду (ОФВ1) (rpb=−0,15; p=0,05). Мультиваріативна логістична регресія підтвердила незалежну прогностичну цінність індексу коморбідності (співвідношення шансів (Odds ratio — OR) = 1,18; 95% довірчий інтервал (ДІ) 1,03–1,35; p=0,02) та наявності метастазів (OR=2,45; 95% ДІ 1,12–5,36; p=0,02). Знижений ОФВ1 мав тенденцію до асоціації з підвищеним ризиком ПОП, однак у мультиваріативній моделі ефект був граничним (p=0,08). Рестриктивна інтраопераційна інфузійна терапія (<5 мл/кг/год) асоціювалася з вищою частотою пневмоній (26,3 проти 20,4% при 5–8 мл/кг/год та 19,3% при ≥8 мл/кг/год), але різниця статистично не значуща (p >0,05). Тривалість наркозу та однолегеневої вентиляції не чинили значущого впливу на ризик ПОП (rpb=0,09 та 0,11 відповідно; p >0,10). Тривалість однолегеневої вентиляції, доза морфіну та тип післяопераційного знеболення також не мали значущого зв’язку з ризиком пневмонії (p >0,05). Вищу частоту ПОП виявлено після «малих» резекцій порівняно з лобектоміями, що може бути пов’язане з меншою частотою використання регіонарних методів аналгезії в цій групі. Висновки. Основними факторами ризику ПОП є високий індекс коморбідності та наявність метастазів. Використання регіонарних методів анальгезії та інфузійна терапія не чинили незалежного впливу в цій когорті на ризик розвитку пневмоній. Необхідні подальші дослідження для уточнення отриманих результатів.
Одержано 20.01.2026
Прийнято до друку 26.01.2026
DOI: 10.32471/clinicaloncology.2663-466X.35483
ВСТУП
Післяопераційні легеневі ускладнення залишаються однією з основних причин захворюваності та подовження госпіталізації після торакальних хірургічних втручань. Незважаючи на впровадження малоінвазивних хірургічних технологій, стандартизацію анестезіологічного забезпечення та розвиток програм прискореного післяопераційного відновлення, частота ПОП після резекцій легень залишається клінічно значущою і, за даними різних досліджень, коливається в межах 5–20% [12, 13, 17, 21]. Розвиток цього ускладнення асоціюється зі збільшенням тривалості перебування в стаціонарі, зростанням потреби в інтенсивній терапії, підвищенням частоти повторних госпіталізацій, а також із погіршенням віддалених результатів лікування та зниженням виживаності пацієнтів [6, 16, 18]. У клінічній практиці ПОП залишається одним із ключових чинників, що визначають перебіг раннього післяопераційного періоду у хворих після резекцій легень.
Ризик розвитку ПОП у пацієнтів після резекції легень формується внаслідок поєднання хірургічних, анестезіологічних та пацієнтоорієнтованих факторів [5]. До основних патофізіологічних передумов належать порушення вентиляційно-перфузійних співвідношень під час однолегеневої вентиляції, зменшення функціонального резерву легеневої тканини внаслідок резекції, а також вплив післяопераційного больового синдрому на глибину дихання та ефективність кашльового рефлексу [2, 4]. Сукупність цих механізмів спричиняє розвиток ателектазів, затримку бронхіального секрету та порушення мукоциліарного кліренсу, що створює сприятливі умови для бактеріальної колонізації та інфекційного процесу. Додаткове значення мають вихідний стан дихальної системи, наявність хронічних обструктивних або рестриктивних порушень вентиляції, супутні серцево-судинні та метаболічні захворювання, а також імунний статус пацієнтів [1, 9, 11].
Особливу увагу в сучасних дослідженнях приділяють ролі коморбідності як інтегрального показника загального соматичного стану пацієнта та його здатності адаптуватися до хірургічного стресу. Індекс коморбідності Чарлсона широко використовується для стратифікації ризику післяопераційних ускладнень і смертності у хворих на онкопатологію та захворювання органів грудної клітки [9, 19]. Високі показники індексу коморбідності відображають кумулятивний вплив супутніх захворювань на перебіг післяопераційного періоду, включно зі зниженням резервних можливостей серцево-легеневої системи та підвищеною вразливістю до інфекційних ускладнень. Окремі дослідження також вказують на можливий вплив онкологічного статусу, зокрема наявності метастатичного процесу, який може розглядатися як маркер системної запальної відповіді, хронічної імуносупресії та загальної кахексії, що потенційно спричиняє розвиток післяопераційних інфекцій [3, 5, 9, 15].
Періопераційні фактори, зокрема тривалість наркозу та однолегеневої вентиляції, характер інтраопераційної інфузійної терапії, а також методи післяопераційного знеболення залишаються предметом активної наукової дискусії. Дані наукової літератури щодо їх незалежного впливу на розвиток ПОП є суперечливими [13, 22, 24]. У клінічній практиці торакальної анестезіології традиційно використовуються рестриктивні підходи до інфузійної терапії з метою зниження ризику легеневого набряку та порушень газообміну, однак оптимальні об’єми інтраопераційної інфузії та їхній зв’язок із післяопераційними інфекційними ускладненнями залишаються недостатньо вивченими [23, 24]. Аналогічно вплив регіонарних методів анальгезії на частоту ПОП оцінюється неоднозначно, що частково зумовлено відмінностями в обсязі хірургічних втручань, селекцією пацієнтів та відсутністю рандомізації в більшості клінічних досліджень [8, 14].
У зв’язку із цим ідентифікація незалежних факторів ризику розвитку ПОП у пацієнтів після резекції легень залишається актуальним завданням клінічної анестезіології, інтенсивної терапії та торакальної хірургії. Аналіз власних клінічних даних з урахуванням сучасних підходів до хірургічного та анестезіологічного забезпечення дозволяє уточнити значущість окремих пацієнт- та процедура-асоційованих чинників, а також створює підґрунтя для подальшої оптимізації періопераційної тактики з метою зниження частоти післяопераційних легеневих ускладнень.
МЕТА ДОСЛІДЖЕННЯ
Встановити вплив клінічниx, функціональних та періопераційних факторів ризику на розвиток ПОП у пацієнтів, яким виконано хірургічні втручання з резекції легень.
МАТЕРІАЛИ І МЕТОДИ ДОСЛІДЖЕННЯ
Дослідження проведено на базі ДНП «Національний інститут раку». Виконано ретроспективний аналіз медичної документації пацієнтів, яким у період з 1 червня до 31 грудня 2023 р. виконані хірургічні втручання з резекції легень через онкологічну патологію.
Критеріями залучення в дослідження були пневмонектомія, діагностичні атипові резекції, комбіновані оперативні втручання з резекцією ребер або грудної стінки, а також дитячий вік. Після застосування критеріїв відбору до фінального аналізу включено 166 клінічних випадків. Діагноз ПОП встановлювали на підставі рентгенологічних даних з урахуванням клінічної картини в післяопераційний період. Для кількісної оцінки супутньої патології використовували індекс коморбідності Чарлсона [19], який включає вік пацієнта та наявність захворювань серцево-судинної, дихальної, нервової систем, цукрового діабету, уражень печінки та нирок, системних захворювань, злоякісних новоутворень, лейкемії, лімфоми та імунодефіцитних станів.
Статистичну обробку даних проводили із застосуванням методів описової та аналітичної статистики. Для числових змінних визначали середні показники та стандартне відхилення або медіану і міжквартильний розмах залежно від характеру розподілу. Категоріальні змінні описували у вигляді абсолютних та відносних частот.
Уніваріативний аналіз виконували з метою первинної оцінки асоціацій між окремими клінічними, функціональними та періопераційними змінними і розвитком ПОП. Для категоріальних змінних використовували χ²-тест або точний тест Фішера. Для числових змінних використовували уніваріативну логістичну регресію з розрахунком OR, 95% ДІ та відповідних p-показників.
Змінні, що мали статистичну значущість p <0,10 в уніваріативному аналізі, а також клінічно значущі фактори включали до мультиваріативної логістичної регресійної моделі з метою визначення незалежних предикторів розвитку ПОП. Для оцінки мультиколінеарності між предикторами розраховували коефіцієнт variance inflation factor. Для числових змінних додатково перевіряли можливу нелінійність зв’язку з кінцевою точкою шляхом категоризації за квартилями. Якість мультиваріативної моделі оцінювали за допомогою ROC-аналізу з визначенням площі під кривою (area under the curve — AUC), а також тесту Хосмера — Лемешоу (Hosmer — Lemeshow) для оцінки калібрування моделі.
З метою перевірки стабільності отриманих результатів проводили аналіз чутливості з побудовою альтернативних моделей, зокрема аналіз у підгрупах та після виключення крайніх показників. Усі статистичні розрахунки виконували з використанням програмного забезпечення Python версії 3.12 із застосуванням бібліотек Pandas, SciPy та Statsmodels. Рівень статистичної значущості встановлювали на рівні p <0,05 при двосторонній перевірці гіпотез.
РЕЗУЛЬТАТИ ДОСЛІДЖЕННЯ
Аналізом охоплено 166 пацієнтів, яким у досліджуваний період були виконані оперативні втручання з резекції легень. ПОП діагностовано у 38 осіб, що становило 22,9% від загальної кількості спостережень. У хворих із ПОП тривалість перебування у стаціонарі була більшою порівняно з пацієнтами без цього ускладнення (13,11±3,85 проти 9,85±3,12 доби відповідно).
Базові демографічні, клінічні та функціональні характеристики досліджуваної популяції наведені в табл. 1. Середній вік пацієнтів становив 58,8±11,2 року. Хворі з ПОП були в середньому старшими порівняно з пацієнтами без цього ускладнення. Середній індекс маси тіла (ІМТ) в обох групах був подібним. Індекс коморбідності Чарлсона був вищим у групі пацієнтів із ПОП.
| Показник | Усі пацієнти (n=166) | ПОП (n=38) | Без ПОП (n=128) |
| Вік, років | 58,8±11,2 | 61,0±11,0 | 57,9±12,4 |
| ІМТ, кг/м² | 26,7±4,1 | 27,0±4,5 | 26,9±5,5 |
| Індекс коморбідності Чарлсона | 7,2±2,8 | 7,4±2,5 | 6,9±2,3 |
| ОФВ1, мл | 2287±843 | 2100±780 | 2350±860 |
| Тривалість наркозу, хв | 137,5±67,3 | 135,9±53,2 | 143,1±61,0 |
| Тривалість однолегеневої вентиляції, хв | 109,8±54,2 | 108,0±49,7 | 115,4±61,0 |
Середня тривалість наркозу та однолегеневої вентиляції не відрізнялася суттєво між групами з ПОП та без неї.
Результати уніваріативного логістичного регресійного аналізу представлені в табл. 2. Вищий індекс коморбідності Чарлсона був асоційований із підвищеним ризиком розвитку ПОП. Наявність метастатичного процесу також була пов’язана зі зростанням імовірності цього ускладнення. Зниження абсолютного показника ОФВ1 свідчило про зворотний зв’язок із ризиком розвитку ПОП.
| Показник | OR | 95% ДІ | p |
| Індекс коморбідності Чарлсона | 1,16 | 1,03–1,31 | 0,02 |
| Наявність метастатичного процесу | 2,21 | 1,06–4,61 | 0,03 |
| ОФВ1 (на 100 мл) | 0,99 | 0,98–1,00 | 0,05 |
Вік, ІМТ, тривалість наркозу та однолегеневої вентиляції не мали статистично значущого зв’язку з розвитком ПОП (p >0,10). Тип післяопераційного знеболення, а також сумарна доза морфіну в післяопераційний період не були асоційовані з частотою розвитку цього ускладнення. У режимі інтраопераційної інфузійної терапії не виявлено статистично значущого зв’язку з ризиком ПОП, хоча при рестриктивному режимі відзначалася тенденція до вищої частоти ускладнення.
До мультиваріативної логістичної регресійної моделі були включені індекс коморбідності Чарлсона, наявність метастатичного процесу та абсолютний показник ОФВ1. Результати аналізу наведені в табл. 3. Незалежними предикторами розвитку ПОП залишалися індекс коморбідності Чарлсона та наявність метастазів. Абсолютний показник ОФВ1 у мультиваріативній моделі свідчить про граничну асоціацію з ризиком розвитку ПОП. Ознак значущої мультиколінеарності між змінними, включеними до регресійної моделі, не виявлено.
| Показник | Скориговане OR | 95% ДІ | p |
| Індекс коморбідності Чарлсона | 1,18 | 1,03–1,35 | 0,02 |
| Наявність метастатичного процесу | 2,45 | 1,12–5,36 | 0,02 |
| ОФВ1 (на 100 мл) | 0,99 | 0,98–1,00 | 0,08 |
Дискримінаційну здатність фінальної мультиваріативної логістичної регресійної моделі оцінювали з використанням ROC-аналізу на основі прогнозованих імовірностей розвитку ПОП. Отримана ROC-крива відображала здатність моделі відрізняти пацієнтів із наявністю цього ускладнення від осіб без нього з урахуванням сукупного впливу включених клінічних факторів. Показник площі під ROC-кривою відповідав задовільному рівню дискримінації, що свідчить про помірну ефективність моделі у класифікації клінічних спостережень (рисунок).
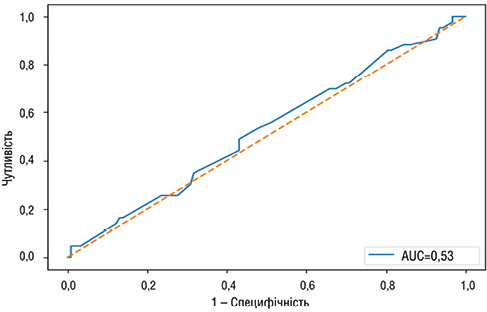
Рисунок. ROC-крива фінальної мультиваріативної логістичної регресійної моделі, побудованої на основі індексу коморбідності Чарлсона та наявності метастатичного процесу, для розрізнення пацієнтів із наявністю та відсутністю ПОП після резекції легень
Важливо підкреслити, що отриманий показник AUC характеризує інтегральний внесок декількох незалежних предикторів, зокрема індексу коморбідності Чарлсона та наявності метастатичного процесу, і не відображає прогностичну значущість окремих змінних. У цьому контексті ROC-аналіз використовувався як інструмент оцінки загальної якості побудованої мультиваріативної моделі, а не як основа для формування індивідуального клінічного прогностичного індексу.
Адекватність калібрування моделі перевіряли за допомогою тесту Хосмера — Лемешоу, який не виявив статистично значущих розбіжностей між спостережуваними та розрахованими ймовірностями розвитку ПОП. Це свідчить про відсутність систематичного зміщення прогнозів моделі в різних підгрупах пацієнтів.
Стійкість отриманих результатів підтверджувалася аналізом чутливості. Виключення крайніх показників безперервних змінних, а також повторний аналіз у підгрупі хворих з анатомічними резекціями легень не зумовлювали суттєвих змін величини коефіцієнтів регресії або напрямку виявлених асоціацій, що свідчить про відсутність домінантного впливу окремих спостережень на результати моделювання.
ДИСКУСІЯ
Отримані результати підтверджують визначальну роль загального соматичного стану пацієнтів у формуванні ризику ПОП після резекцій легень. Індекс коморбідності Чарлсона залишався незалежним предиктором розвитку цього ускладнення як в уніваріативному, так і мультиваріативному аналізі, що узгоджується з даними попередніх досліджень, у яких коморбідність розглядається як інтегральний показник функціональних резервів організму та толерантності до хірургічного стресу [7, 8]. Аналогічні результати наведені в дослідженні [9], де коморбідність була асоційована з підвищеною післяопераційною смертністю та частотою ускладнень у торакальних пацієнтів.
Асоціація між наявністю метастатичного процесу та ризиком розвитку ПОП, ймовірно, відображає системні порушення імунної відповіді та хронічну активацію запальних механізмів, характерні для пацієнтів з прогресуючим онкологічним захворюванням. Імуносупресія, зниження нутритивного та функціонального резерву, а також вплив протипухлинної терапії можуть спричиняти підвищену вразливість до інфекційних ускладнень у післяопераційний період, що пояснює незалежний внесок цього чинника в багатофакторній моделі.
Періопераційні параметри, зокрема тривалість наркозу та однолегеневої вентиляції, у цьому дослідженні не чинили статистично значущого впливу на ризик розвитку ПОП. Ці результати частково відрізняються від окремих публікацій, у яких тривалі оперативні втручання, зокрема понад 180 хв, асоціювалися з підвищеним ризиком легеневих ускладнень [9, 20]. Водночас у представленій вибірці тривалість більшості оперативних втручань не перевищувала 3 год, що могло обмежити варіабельність цього показника. Крім того, всі операції виконувалися з використанням однолегеневої вентиляції, що забезпечувало стандартизований вентиляційний підхід і могло мінімізувати додатковий травматичний вплив на оперовану легеню.
Відсутність статистично значущого впливу тривалості наркозу та однолегеневої вентиляції на ризик розвитку ПОП у цьому дослідженні узгоджується з результатами сучасних проспективних аудитів анестезіологічної практики. Зокрема, у багатоцентровому проспективному дослідженні критичних інцидентів під час анестезії, опублікованому в «BMC Anesthesiology» у 2023 р. [25], виявлено, що більшість інтраопераційних ускладнень має транзиторний характер і рідко трансформується у віддалені післяопераційні наслідки, зокрема інфекційні ускладнення. Автори підкреслюють, що системні характеристики пацієнта та вихідний соматичний стан відіграють значно більшу роль у формуванні післяопераційних ускладнень, ніж окремі технічні або часові параметри анестезіологічного забезпечення.
У цьому контексті результати представленого дослідження додатково підтверджують, що ризик ПОП після резекцій легень визначається переважно сукупністю немодифікованих або умовно модифікованих факторів пацієнта, зокрема коморбідністю та онкологічним статусом, тоді як ізольовані інтраопераційні події або тривалість окремих етапів анестезії чинять обмежений вплив на формування інфекційних ускладнень у віддалений післяопераційний період.
Аналіз режимів інтраопераційної інфузійної терапії виявив тенденцію до вищої частоти ПОП у пацієнтів, яким використовували рестриктивну інфузійну стратегію (<5 мл/кг/год), порівняно з помірним та ліберальним режимами, однак ці відмінності не досягли статистичної значущості. Слід підкреслити, що, на відміну від більшості попередніх досліджень, у яких оцінювали вплив періопераційної інфузійної терапії загалом [23], у цій роботі акцент було зроблено саме на інтраопераційному етапі. У попередніх публікаціях наведено недоліки ліберальної інфузійної стратегії та її вплив на розвиток легеневого набряку й пневмонії [24], однак дані щодо ізольованого впливу інтраопераційних об’ємів інфузії залишаються обмеженими.
З патофізіологічної точки зору, надмірна рестрикція інтраопераційної інфузії може призводити до гіпоперфузії колабованої легені під час однолегеневої вентиляції, порушення мікроциркуляції та дисфункції ендотеліального глікокаліксу, що потенційно сприяє активації запальної відповіді. Отримані результати не дозволяють дійти остаточних висновків щодо переваг тієї чи іншої інфузійної стратегії, однак вказують на доцільність подальшого вивчення підходів із чітким розмежуванням інтра- та післяопераційного етапів інфузійної терапії.
Вплив регіонарних методів післяопераційного знеболення на ризик розвитку ПОП у вищевказаному дослідженні не може бути інтерпретований як достовірний у зв’язку з відсутністю рандомізації. Регіонарні методи використовувалися переважно у пацієнтів з більшим обсягом хірургічного втручання, тоді як у хворих з атиповими резекціями легень вони використовувалися рідше. Такий нерівномірний розподіл міг нівелювати потенційний захисний ефект регіонарної анальгезії. Опосередковано про її можливий позитивний вплив може свідчити відсутність різниці в частоті розвитку ПОП між групами малих та великих резекцій, тоді як у попередніх дослідженнях більший обсяг резекції асоціювався з підвищеним ризиком цього ускладнення [9, 10].
Знижені абсолютні показники ОФВ1 свідчили про асоціацію з підвищеним ризиком ПОП в уніваріативному аналізі, однак у мультиваріативній моделі асоціація не досягла статистичної значущості, але наближалася до порогового рівня (p=0,08). Це може відображати взаємозв’язок між функціональним станом легень, коморбідністю та онкологічним статусом пацієнтів, що зменшує незалежний внесок ОФВ1 після корекції на ці чинники.
Основними обмеженнями дослідження є його ретроспективний дизайн, який обмежує можливість повного контролю потенційних конфаундерів та причинно-наслідкових інтерпретацій, а також відносно невеликий обсяг вибірки, який знижує статистичну потужність для виявлення помірних ефектів окремих періопераційних факторів. Верифікація ПОП ґрунтувалася переважно на рентгенологічних критеріях без систематичного мікробіологічного підтвердження, що могло впливати на точність діагностики. Відсутність рандомізації при використанні регіонарних методів знеболення та їх селективний характер залежно від обсягу оперативного втручання обмежують інтерпретацію отриманих результатів. Крім того, аналіз інтраопераційної інфузійної терапії не враховував післяопераційні об’єми інфузії та кумулятивний баланс рідини, які можуть мати додаткове значення для розвитку легеневих ускладнень.
ВИСНОВКИ
ПОП виникала у 22,9% пацієнтів після резекції легень та була асоційована зі статистично значущим подовженням тривалості госпіталізації. Незалежними факторами ризику її розвитку у представленій когорті були високий індекс коморбідності Чарлсона та наявність метастатичного ураження. Знижений ОФВ1 та рестриктивна інтраопераційна інфузійна терапія супроводжувалися тенденцією до вищої частоти ПОП, однак не мали незалежної прогностичної значущості в мультиваріативному аналізі. Тривалість наркозу, однолегеневої вентиляції, тип післяопераційного знеболення та доза опіоїдів не впливали на ризик розвитку цього ускладнення в межах досліджуваної вибірки. Отримані результати підкреслюють важливість преопераційної оцінки коморбідності та онкологічного статусу пацієнтів і обґрунтовують необхідність подальших проспективних досліджень для уточнення ролі модифікованих періопераційних факторів у профілактиці післяопераційних легеневих ускладнень.
Додаткова інформація. Автори заявляють про відсутність конфлікту інтересів.
Джерела фінансування: відсутні.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
1. Barbetakis, N., & Vassiliadis, M. (2004). Is amiodarone a safe antiarrhythmic to use in supraventricular tachyarrhythmias after lung cancer surgery? BMC Surgery, 4, 7. doi.org/10.1186/1471-2482-4-7.
2. Belda, J., Cavalcanti, M., Ferrer, M., Serra, M., Puig de la Bellacasa, J., Canalis, E., & Torres, A. (2005). Bronchial colonization and postoperative respiratory infections in patients undergoing lung cancer surgery. Chest, 128(3), 1571–1579. doi.org/10.1378/chest.128.3.1571.
3. Bray, F., Ferlay, J., Soerjomataram, I., Siegel, R. L., Torre, L. A., & Jemal, A. (2018). Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide in 185 countries. CA: A Cancer Journal for Clinicians, 68(6), 394–424. doi.org/10.3322/caac.21492.
4. Campos, J. H. (2023). Hypoxia during one-lung ventilation. Open Anesthesia. Retrieved from http://www.openanesthesia.org/keywords/hypoxia-during-one-lung-ventilation.
5. Ergin Özcan, P., & Şentürk, E. (2017). Pneumonia after thoracic surgery. Postoperative Care in Thoracic Surgery, 11, 207–217. doi.org/10.1007/978-3-319-19908-5_14.
6. Finley, C. J., Begum, H. A., Pearce, K., Agzarian, J., Hanna, W. C., Shargall, Y., & Akhtar-Danesh, N. (2022). The effect of major and minor complications after lung surgery on length of stay and readmission. Journal of Patient Experience, 9, 23743735221077524. doi.org/10.1177/23743735221077524.
7. Khoche, S. (2025). Perioperative pulmonary hypertension. Medscape. Retrieved from emedicine.medscape.com/article/2500073-overview.
8. Li, R., Wang, K., Qu, C., Qi, W., Fang, T., Yue, W., & Tian, H. (2021). Effect of ERAS program on lung cancer surgery: systematic review and meta-analysis. Journal of Thoracic Disease, 13(6), 3670–3683. doi.org/10.21037/jtd-21-433.
9. Lijun, Y., Luo, J., Liu, L., Wu, Q., Zhou, R., Li, L., & Zhang, C. (2021). Risk factors for postoperative pneumonia and prognosis in lung cancer patients after surgery. Medicine, 100(13), e25295. doi.org/10.1097/MD.0000000000025295.
10. Лісний, І. І., & Закальська, Х. А. (2024). Реміфентаніл — сучасний анестетик у сучасній анестезіології та інтенсивній терапії. Клінічна онкологія, 14(1), 18–25. doi.org/10.32471/clinicaloncology.2663-466X.53-1.31991 [Lisnyi, I. I., & Zakalska, K. A. (2024). Remifentanil — suchasnyi anestetyk u suchasnii anesteziolohii ta intensyvnii terapii. Clinical Oncology, 14(1), 18–25. Ukrainian].
11. Motono, N., Ishikawa, M., Iwai, S., Iijima, Y., Usuda, K., & Uramoto, H. (2021). Individualization of risk factors for postoperative complications after lung cancer surgery. BMC Surgery, 21, 311. doi.org/10.1186/s12893-021-01305-0.
12. Pei, G., Zhou, S., Han, Y., Liu, Z., & Xu, S. (2014). Risk factors for postoperative complications after lung resection for NSCLC in elderly patients. Journal of Thoracic Disease, 6(9), 1230–1237. doi.org/10.3978/j.issn.2072-1439.2014.07.23.
13. Radu, D. M., Jauréguy, F., Seguin, A., Foulon, C., Destable, M. D., Azorin, J., & Martinod, E. (2007). Postoperative pneumonia after major pulmonary resections: An unsolved problem. Annals of Thoracic Surgery, 84(5), 1669–1673. doi.org/10.1016/j.athoracsur.2007.05.059.
14. Rogers, L. J., Bleetman, D., Messenger, D. E., Joshi, N. A., Wood, L., Rasburn, N. J., & Batchelor, T. J. P. (2018). The impact of enhanced recovery after surgery (ERAS) protocol compliance on morbidity from resection for primary lung cancer. Journal of Thoracic and Cardiovascular Surgery, 155(4), 1843–1852. doi.org/10.1016/j.jtcvs.2017.10.151.
15. Roungeris, L., Devadze, G., Talliou, C., & Griva, P. (2024). Prediction of postoperative complications after major lung resection: A literature review. Anesthesia Research, 1(2), 146–156. doi.org/10.3390/anesthres1020014.
16. Semenkovich, T. R., Frederiksen, C., Hudson, J. L., Subramanian, M., Kollef, M. H., Patterson, G. A., Kreisel, D., … Puri, V. (2019). Postoperative pneumonia prevention in pulmonary resections: A feasibility pilot study. Annals of Thoracic Surgery, 107(1), 262–270. doi.org/10.1016/j.athoracsur.2018.08.008.
17. Sengupta, S. (2015). Post-operative pulmonary complications after thoracotomy. Indian Journal of Anaesthesia, 59(9), 618–626. doi.org/10.4103/0019-5049.165852.
18. Shinohara, S., Kobayashi, K., Kasahara, C., Onitsuka, T., Matsuo, M., Nakagawa, M., & Sugaya, M. (2019). Long-term impact of complications after lung resections in NSCLC. Journal of Thoracic Disease, 11(5), 2050–2057. doi.org/10.21037/jtd.2019.04.91.
19. Simonsen, D. F., Søgaard, M., Bozi, I., Horsburgh, C. R., & Thomsen, R. W. (2015). Risk factors for postoperative pneumonia and its impact on survival. Respiratory Medicine, 109(10), 1340–1346. doi.org/10.1016/j.rmed.2015.07.008.
20. Xu, Y., Qin, Y., Ma, D., & Liu, H. (2022). Impact of segmentectomy versus lobectomy on pulmonary function in NSCLC: A meta-analysis. Journal of Cardiothoracic Surgery, 17, 107. doi.org/10.1186/s13019-022-01853-3.
21. Erdogu, V., Akin, H., Sonmezoglu, Y., Kutluk, A. C., Sezen, C. B., Dogru, M. V., … Metin, M. (2020). Comparison of VATS lobectomy vs open thoracotomy for NSCLC. Sisli Etfal Hospital Medical Bulletin, 54(3), 291–296. doi.org/10.14744/SEMB.2020.60963.
22. Yang, R., Zhou, Y., Gao, S., Du, C., & Wu, Y. (2022). Effects of 24-hour postoperative intravenous fluid on postoperative outcomes after lobectomy: A retrospective observational study. Journal of Thoracic Disease, 14(7), 2602–2610. doi.org/10.21037/jtd-22-707.
23. Pang, Q., Liu, H., Chen, B., & Jiang, Y. (2017). Restrictive and liberal fluid administration in major abdominal surgery. Saudi Medical Journal, 38(2), 123–131. doi.org/10.15537/smj.2017.2.15077.
24. Iwata, H. (2019). Importance of intraoperative fluid management. Journal of Thoracic Disease, 11(15), S2002–S2004. doi.org/10.21037/jtd.2019.06.58.
25. Bielka, K., Kuchyn, I., Frank, F., Sirenko, I., Yurovich, A., Slipukha, D., … Posternak, G. (2023). Critical incidents during anesthesia: prospective audit. BMC Anesthesiology, 23, 206. doi.org/10.1186/s12871-023-02171-4.
Адреса для листування:
Стабровська Ірина Миколаївна
03022, Київ, вул. Здановської Юлії, 33/43
Державне некомерційне підприємство «Національний інститут раку»
E-mail: iryna.stabrovska@unci.org.ua
Correspondence:
Iryna Stabrovska
33/43 Yulii Zdanovskoi str., Kyiv, 03022
Nonprofit Organization National Cancer Institute
E-mail: iryna.stabrovska@unci.org.ua














Leave a comment