Профілактика та лікування фібриляції передсердь у пацієнтів з онкопатологією після торакальних некардіохірургічних операцій
Горкавий Є.О., Головко В.О., Ганоль О.Ю., Єгоров І.В., Науменко А.В., Нечваль В.М., Перконос А.П., Пікульський В.В., Сидоренко К.Д., Балахонов О.І.
Резюме. Фібриляція передсердь (ФП) належить до надшлуночкової тахіаритмії з некоординованою активацією передсердь та їх неефективним скороченням, що підвищує ризик виникнення артеріального тромбозу та розвитку хронічної серцевої недостатності. У рекомендаціях Американського коледжу кардіології, Американської асоціації серця (American College of Cardiology / American Heart Association — АСС / АНА), Американської асоціації торакальних хірургів (American Association for Thoracic Surgery — AATS) та Європейської асоціації кардіоторакальної хірургії (European Association of Cardio-Thoracic Surgery — EACTS) запропоновано шляхи профілактики та лікування ФП антиаритмічними фармакологічними та не фармакологічними засобами у пацієнтів, що потребують торакальної хірургії, у періопераційний період. У Державному некомерційному підприємстві «Національний інститут раку» у відділенні анестезіології та інтенсивної терапії з 2024 р. введено в клінічну практику стандартизований підхід до профілактики і лікування ФП антиаритмічними препаратами (аміодароном та блокаторами бета-адренорецепторів) у визначеної категорії пацієнтів з онкопатологією після торакальних некардіохірургічних операцій.
Одержано 29.01.2026
Прийнято до друку 3.02.2026
DOI: 10.32471/clinicaloncology.2663-466X.35539
ВСТУП
ФП є найчастішою аритмією із всіх порушень ритму, та її поширеність у світі продовжує зростати [6]. Приблизна глобальна поширеність в усьому світі у 2020 р. становила 50 млн зареєстрованих випадків [7]. Кожна 3-тя людина європеоїдної раси віком старше 55 років має ризик захворіти на ФП [17].
Фактори ризику розвитку ФП численні: серцево-судинні захворювання, ожиріння, малорухомий спосіб життя, цукровий діабет, хронічні обструктивні захворювання легень, хронічні хвороби нирок, зловживання алкоголем, чоловіча стать, особи похилого віку та етнічна приналежність до некавказької національності [3, 6, 7, 10, 11, 16, 19].
У пацієнтів з торакальною патологією ФП найчастіше виникає на 2–4-ту добу після операції. У більшості випадків (близько 90%) синусовий ритм відновлюється протягом 4–6 тиж після операції у разі нападу передсердної тахіаритмії. У кардіохірургії та оперативних втручаннях на легенях частота розвитку ФП на 50–200% вища порівняно із загальною хірургією [21]. За результатами досліджень, тривалість перебування пацієнтів після торакальних операцій, ускладнених ФП, становила в середньому 3 доби, та вартість лікування підвищувалася від 30 до 68% [21, 25]. За умови тяжкого перебігу ФП ускладнюється гострою серцевою недостатністю, набряком легень, гострим порушенням мозкового кровообігу, судинними тромбозами.
Рекомендації АСС / АНА, AATS, ESC і EACTS дозволяють знизити частоту виникнення ФП у післяопераційний період у 2–3 рази за даними різних досліджень [23, 26].
МЕХАНІЗМИ ТА РИЗИКИ розвитку ФП у ТОРАКАЛЬНІЙ ХІРУРГІЇ
За даними досліджень, напади ФП після торакальних операцій пов’язані з інтенсивністю хірургічної травми та фізичними характеристиками пацієнтів [1, 9, 21, 25]. У дослідженнях, присвячених механізму виникнення ФП, виявлено наявність патоморфологічного субстрату передсердя (фіброз або дилатація передсердя, волемічне судинне навантаження, ішемія міокарда, хронічна серцева недостатність, перикардит) та пускового механізму (адренергічна або ваговагальна стимуляція) з активацією ектопічних вогнищ та механізму «ріентрі» (патологічної кругової циркуляції збудження) в лівому передсерді, що ініціює ФП (рис. 1) [23, 26]. Остаточно механізм виникнення ФП не з’ясований.
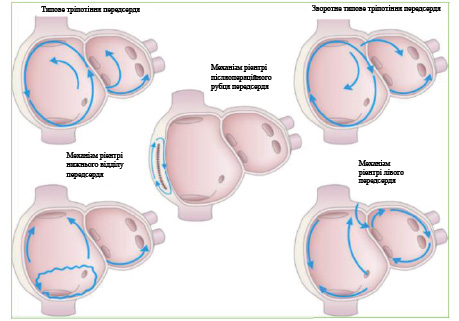
Рис. 1. Ініціація ФП через активацію ектопічних вогнищ та механізму ріентрі (АСС / АНА, 2023) [цит. за 27]
До операцій з низьким ризиком розвитку ФП (<5%) належать торакоскопічні та бронхоскопічні процедури, встановлення стенту трахеї та стравоходу, трахеотомія, дренування плевральної порожнини, медіастиноскопія, торакоскопічна краєва резекція легень.
До операцій із середнім ризиком виникнення ФП (5–15%) належать торакоскопічна симпатектомія та лімфодисекція, сегментектомія, фундопластика та пластика стравохідного кільця, резекція дивертикула стравоходу.
До операцій з високим ризиком виникнення ФП (>15%) належать торакоскопічна або відкрита лобектомія, пульмонектомія, вісцероліз плеври, видалення пухлини переднього середостіння, резекція та реконструктивні операції на трахеї та бронхах, резекція бронхоплевральної фістули, трансплантація легень, фенестрація перикарда, резекція стравоходу [1, 9, 14, 21, 25].
ПЕРЕДОПЕРАЦІЙНА ПІДГОТОВКА ПАЦІЄНТІВ З ВИСОКИМ РИЗИКОМ РОЗВИТКУ ФП ПІСЛЯ ТОРАКАЛЬНИХ НЕКАРДІОХІРУРГІЧНИХ ОПЕРАЦІЙ
Передопераційне стандартне обстеження включає консультацію кардіолога, електро-, ехокардіографію серця з метою визначення патології ритму та структурних змін цього органа, а також виявлення функціональної спроможності лівого шлуночка. За наявності у пацієнта ФП оцінка проводиться з урахуванням ризику можливого ускладнення гострого ішемічного інсульту (ГІІ) відповідно до міжнародної класифікації CHA2DS2-VASc: Cardiac failure — серцева недостатність, Hypertension — артеріальна гіпертензія, Age ≥75 — вік ≥75 років, Diabetes — цукровий діабет, Stroke — інсульт, Vascular disease — ІХС, захворювання периферичних судин, Age 65–74 — вік 65–74 роки, Sex category (female) — жіноча стать. CHA2DS2-VASc ≥2 — підвищений або високий ризик ГІІ, CHA2DS2-VASc ≤1 — мінімальний або відсутній ризик ГІІ у післяопераційний період у пацієнтів з ФП (таблиця) [15].
| Критерій | Показник |
| Серцева недостатність | 1 |
| Артеріальна гіпертензія | 1 |
| Вік ≥75 років | 2 |
| Цукровий діабет | 1 |
| Інсульт | 2 |
| Судинне захворювання | 1 |
| Вік 65–74 роки | 1 |
| Стать | 1 |
| Шкала | Ризик (%) |
| 0 | 0,0 |
| 1 | 1,3 |
| 2 | 2,2 |
| 3 | 3,2 |
| 4 | 4,0 |
| 5 | 6,7 |
| 6 | 9,8 |
| 7 | 9,6 |
| 8 | 6,7 |
| 9 | 15,2 |
АНТИАРИТМІЧНА ПРОФІЛАКТИКА У ПАЦІЄНТІВ ПІСЛЯ ТОРАКАЛЬНИХ ОПЕРАЦІЙ
Прийом блокаторів бета-адренорецепторів перед операцією є ефективним антиаритмічним засобом для профілактики ФП. Рекомендується продовжувати у пацієнтів після торакальних операцій, щоб запобігти синдрому відміни після операції (клас рекомендації — 1, сильна; рівень доказовості — А, високий [2, 5, 8, 12, 20].
Застосування аміодарону у пацієнтів після торакальної хірургії в післяопераційний період у 2–3 рази зменшувало кількість ФП порівняно з плацебо (клас рекомендації — 2А, помірна; рівень доказовості — А, високий) [4, 8, 23, 26].
Дилтіазем може бути призначений пацієнтам, що потребують торакальної хірургії, зі збереженою функцією лівого шлуночка, якщо ті не приймали блокатори бета-адренорецепторів перед операцією. Препарат протипоказаний за наявності додаткових шляхів провідності (наприклад, синдром Вольфа — Паркінсона — Вайта) (клас рекомендації — 2А, помірна; рівень доказовості — В, помірний) [2, 8].
Показано внутрішньовенне введення магнію сульфату після торакальних операцій за наявності гіпомагніємії (клас рекомендації — 2В, помірна; рівень доказовості — С, слабкий) [8, 18].
ПРАКТИЧНІ РЕКОМЕНДАЦІЇ ЩОДО ПРОФІЛАКТИКИ ФП ПІСЛЯ ТОРАКАЛЬНИХ ОПЕРАЦІЙ
1. Продовжити блокатори бета-адренорецепторів до, в день та після операції.
2. Аміодарон 300 мг в/в інфузія (навантажувальна доза), потім перорально 600 мг 2 р/добу протягом 5 діб. За результатами рандомізованого плацебо-контрольованого дослідження, ФП після операції виникла у 9% пацієнтів, що отримували аміодарон за схемою, наведеною вище, порівняно з 32% у групі плацебо. Без значних побічних ефектів [8, 24].
3. Аміодарон 1050 мг в/в інфузія / 24 год, потім перорально 400 мг 2 р/добу протягом 5 діб. За результатами рандомізованого плацебо-контрольованого дослідження, ФП відмічалася після операції у 14% пацієнтів, що отримали аміодарон за схемою, наведеною вище, порівняно з 32% плацебо. Без значних побічних ефектів [8, 26].
4. Дилтіазем 240 мг/добу перорально (скоротливість лівого шлуночка збережена, відсутність додаткових шляхів провідності) [2, 8].
5. Магнію сульфат 80 мг/кг маси тіла в/в інфузія (навантажувальна доза) і 8 мг/кг/год протягом 48 год (при гіпомагніємії). За результатами проспективного рандомізованого плацебо-контрольованого дослідження, ФП зафіксована після операції у 13% пацієнтів, що отримали магнію сульфат за схемою, наведеною вище, порівняно з 44% плацебо (p <0,05) [8, 13].
ЛІКУВАННЯ ФП ПІСЛЯ ТОРАКАЛЬНИХ ОПЕРАЦІй
Блокатори бета-адренорецепторів та аміодарон у терапевтичній дозі ефективні для лікування ФП за умови стабільної гемодинаміки. У разі артеріальної гіпотензії пацієнту в ургентному порядку проводиться кардіоверсія за життєвими показаннями. За наявності клінічних ознак хронічної серцевої недостатності, погіршення функції лівого шлуночка та збереження тахіаритмії може бути рекомендовано внутрішньовенне введення дигоксину як препарату другої лінії (клас рекомендації — 2В, помірна; рівень доказовості — В, помірний) [8, 22].
З 2024 р. в Національному інституті раку у відділенні анестезіології та інтенсивної терапії введено в клінічну практику стандартизований підхід до профілактики і лікування ФП антиаритмічними препаратами аміодарон та блокатори бета-адренорецепторів у визначеної категорії пацієнтів з онкопатологією після радикальних торакальних некардіохірургічних операцій (рис. 2).
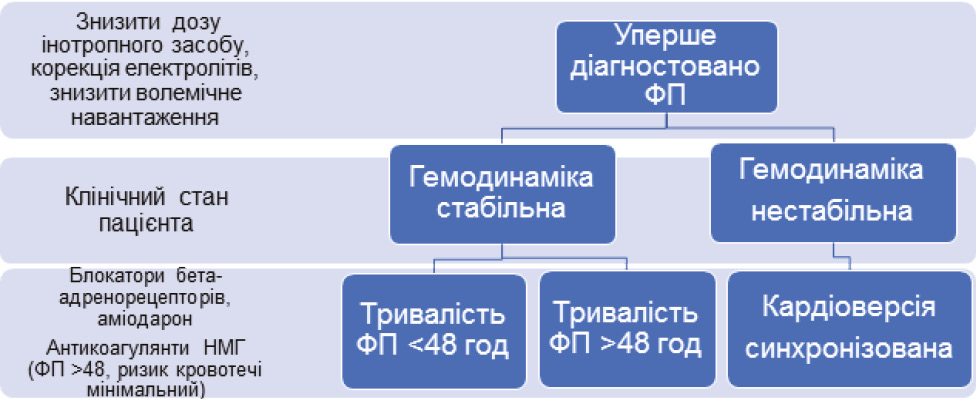
Рис. 2. Алгоритм лікування ФП
Примітка: НМГ — низькомолекулярний гепарин.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
1. Akoum, N., Daccarett, M., McGann, C., Segerson, N., Vergara, G., Kuppahally, S., … Marrouche, N. (2011). Atrial fibrosis helps select the appropriate patient and strategy in catheter ablation of atrial fibrillation: a DE-MRI guided approach. Journal of Cardiovascular Electrophysiology, 22(1), 16–22. doi: 10.1111/j.1540-8167.2010.01876.x.
2. Amar, D., Roistacher, N., Rusch, V. W., Leung, D. H. Y., Ginsburg, I., Zhang, H., … Ginsberg, R. J. (2000). Effects of diltiazem prophylaxis on the incidence and clinical outcome of atrial arrhythmias after thoracic surgery. Journal of Thoracic and Cardiovascular Surgery, 120(4), 790–798. doi: 10.1067/mtc.2000.109538.
3. Aune, D., Feng, T., Schlesinger, S., Janszky, I., Norat, T., & Riboli, E. (2018). Diabetes mellitus, blood glucose and the risk of atrial fibrillation: a systematic review and metaanalysis of cohort studies. Journal of diabetes and its complications, 32(5), 501–511. doi: 10.1016/j.jdiacomp.2018.02.004.
4. Barbetakis, N., & Vassiliadis, M. (2004). Is amiodarone a safe antiarrhythmic to use in supraventricular tachyarrhythmias after lung cancer surgery? BMC Surgery, 4, 7. doi: 10.1186/1471-2482-4-7.
5. Bayliff, C. D., Massel, D. R., Inculet, R. I., Malthaner, R. A., Quinton, S. D., Powell, F. S., & Kennedy, R. S. (1999). Propranolol for the prevention of postoperative arrhythmias in general thoracic surgery. Annals of Thoracic Surgery, 67(1), 182–186. doi: 10.1016/s0003-4975(98)01226-0.
6. Benjamin, E. J., Muntner, P., Alonso, A., Bittencourt, M. S., Callaway, C. W., Carson, A. P., … Virani, S. S. (2019). Heart disease and stroke statistics 2019 update: a report from the American Heart Association. Circulation, 139(10), e56–e528. doi: 10.1161/CIR.0000000000000659.
7. Chugh, S. S., Havmoeller, R., Narayanan, K., Singh, D., Rienstra, M., Benjamin, E. J., … Murray, C. J. (2014). Worldwide epidemiology of atrial fibrillation: a Global Burden of Disease 2010 study. Circulation, 129(8), 837–847. doi: 10.1161/CIRCULATIONAHA.113.005119.
8. Frendl, G., Sodickson, A. C., Chung, M. K., Waldo, A. L., Gersh, B. J., Tisdale, J. E., … Adler, D. (2014). 2014 AATS guidelines for the prevention and management of perioperative atrial fibrillation and flutter for thoracic surgical procedures. Executive summary. Journal of Thoracic and Cardiovascular Surgery, 148(3), 772–791. doi: 10.1016/j.jtcvs.2014.06.037.
9. Hardy, J., Liu, X., Cheng, K., Ireland, P., Panizales, C., Sugarbaker, D., & Frendl, G. (2012). Risk factors for atrial fibrillation following extrapleural pneumonectomy, the effect of prophylactic beta blockade. American Journal of Respiratory and Critical Care Medicine, 185, A5831.
10. Heeringa, J., van der Kuip, D. A., Hofman, A., Kors, J. A., van Herpen, G., Stricker, B. H., … Witteman, J. C. (2006). Prevalence, incidence and lifetime risk of atrial fibrillation: the Rotterdam Study. European Heart Journal, 27(8), 949–953. doi: 10.1093/eurheartj/ehi825.
11. Hobbelt, A. H., Siland, J. E., Geelhoed, B., Van Der Harst, P., Hillege, H. L., Van Gelder, I. C., & Rienstra, M. (2017). Clinical, biomarker, and genetic predictors of specific types of atrial fibrillation in a community-based cohort: data of the PREVEND study. Europace, 19(2), 226–232. doi: 10.1093/europace/euw016.
12. Jakobsen, C. J., Bille, S., Ahlburg, P., Rybro, L., Hjortholm, K., & Andresen, E. B. (1997). Perioperative metoprolol reduces the frequency of atrial fibrillation after thoracotomy for lung resection. Journal of Cardiothoracic and Vascular Anesthesia, 11(6), 746–751. doi: 10.1016/s1053-0770(97)90169-5.
13. Khalil, M. A., Al-Agaty, A. E., Ali, W. G., & Abdel Azeem, M. S. (2013). A comparative study between amiodarone and magnesium sulfate as antiarrhythmic agents for prophylaxis against atrial fibrillation following lobectomy. Journal of Anesthesia, 27(1), 56–61. doi: 10.1007/s00540-012-1478-3.
14. Lee, G., Wu, H., Kalman, J. M., Esmore, D., Williams, T., Snell, G., & Kistler, P. M. (2010). Atrial fibrillation following lung transplantation: double but not single lung transplant is associated with long-term freedom from paroxysmal atrial fibrillation. European Heart Journal, 31(22), 2774–2782. doi: 10.1093/eurheartj/ehq224.
15. Lip, G. Y., Nieuwlaat, R., Pisters, R., Lane, D. A., & Crijns, H. J. (2010). Refining clinical risk stratification for predicting stroke and thromboembolism in atrial fibrillation using a novel risk factor-based approach: the euro heart survey on atrial fibrillation. Chest, 137(2), 263–272. doi: 10.1378/chest.09-1584.
16. Lloyd-Jones, D. M., Wang, T. J., Leip, E. P., Larson, M. G., Levy, D., Vasan, R. S., … Benjamin, E. J. (2004). Lifetime risk for development of atrial fibrillation: the Framingham Heart Study. Circulation, 110(9), 1042–1046. doi: 10.1161/01.CIR.0000140263.20897.42.
17. Magnussen, C., Niiranen, T. J., Ojeda, F. M., Gianfagna, F., Blankenberg, S., Njolstad, I., … Schnabel, R. B. (2017). Sex differences and similarities in atrial fibrillation epidemiology, risk factors, and mortality in community cohorts: results from the BiomarCaRE Consortium (Biomarker for Cardiovascular Risk Assessment in Europe). Circulation, 136(17), 1588–1597. doi: 10.1161/CIRCULATIONAHA.117.028981.
18. Merritt, R. E., & Shrager, J. B. (2012). Prophylaxis and management of atrial fibrillation after general thoracic surgery. Thoracic Surgery Clinics, 22(1), 13–23. doi: 10.1016/j.thorsurg.2011.08.016.
19. Nalliah, C. J., Sanders, P., & Kalman, J. M. (2018). The impact of diet and lifestyle on atrial fibrillation. Current Cardiology Reports, 20(12), 137. doi: 10.1007/s11886-018-1082-8.
20. Nattel, S., Rangno, R. E., & Van Loon, G. (1979). Mechanism of propranolol withdrawal phenomena. Circulation, 59(6), 1158–1164. doi: 10.1161/01.cir.59.6.1158.
21. Onaitis, M., D’Amico, T., Zhao, Y., & Harpole, D. (2010). Risk factors for atrial fibrillation after lung cancer surgery: analysis of the Society of Thoracic Surgeons general thoracic surgery database. Annals of Thoracic Surgery, 90(2), 368–374. doi: 10.1016/j.athoracsur.2010.03.100.
22. Rena, O., Papalia, E., Oliaro, A., Casadio, C., Ruffini, E., Filosso, P. L., … Maggi, G. (2001). Supraventricular arrhythmias after resection surgery of the lung. European Journal of Cardio-Thoracic Surgery, 20(4), 688–693. doi: 10.1016/s1010-7940(01)00890-9.
23. Riber, L. P., Christensen, T. D., & Jensen, H. K. (2012). Amiodarone significantly decreases atrial fibrillation in patients undergoing surgery for lung cancer. Annals of Thoracic Surgery, 94(2), 339–344. doi: 10.1016/j.athoracsur.2011.12.096.
24. Riber, L. P., Larsen, T. B., & Christensen, T. D. (2014). Postoperative Atrial Fibrillation Prophylaxis After Lung Surgery: Systematic Review and Meta-Analysis. Annals of Thoracic Surgery, 98(6), 1989–1997. doi: 10.1016/j.athoracsur.2014.06.069.
25. Roselli, E. E., Murthy, S. C., Rice, T. W., Houghtaling, P. L., Pierce, C. D., Karchmer, D. P., & Blackstone, E. H. (2005). Atrial fibrillation complicating lung cancer resection. Journal of Thoracic and Cardiovascular Surgery, 130(2), 438–444. doi: 10.1016/j.jtcvs.2005.02.010.
26. Tisdale, J. E., Wroblewski, H. A., & Wall, D. S. (2009). A randomized trial evaluating amiodarone for prevention of atrial fibrillation after pulmonary resection. Annals of Thoracic Surgery, 88(3), 886–893. doi: 10.1016/j.athoracsur.2009.04.074.
27. Wellens, H. J. (2002). Contemporary management of atrial flutter. Circulation, 106(6), 649–52. doi: 10.1161/01.cir.0000027683.00417.9a.
Адреса для листування:
Горкавий Євген Олександрович
03022, Київ, вул. Здановської Юлії, 33/43
Державне некомерційне підприємство «Національний інститут раку»
E-mail: ygorkavyy@gmail.com
Correspondence:
Yevgen Gorkavyi
33/43 Yulii Zdanovskoi str., Kyiv, 03022
Nonprofit Organization National Cancer Institute
E-mail: ygorkavyy@gmail.com.














Leave a comment