Реконструктивні хірургічні втручання грудної стінки — шанс уникнути інвалідизації
Борисюк Б.О., Борисюк Ю.В., Ганул В.А., Совенко В.М., Величко В.В.
Резюме. Проведено ретроспективний аналіз клінічних випадків 83 пацієнтів із первинними пухлинами грудної стінки, ребер і грудини, а також із метастатичним ураженням грудної стінки, які отримали хірургічне лікування із закриттям дефектів грудної стінки як частину комплексного лікування у клініці Державного некомерційного підприємства «Національний інститут раку» (ДНП «НІР») у період з 2021 до 2025 рр. У зазначений період виконано 45 комбінованих оперативних втручань із реконструкцією та заміщенням дефектів грудної стінки. У клінічній практиці успішно використано різні методики реконструкції грудини, ребер і ключиці із використанням кісткових аутотрансплантатів, м’язово-шкірних клаптів та синтетичних матеріалів, зокрема поліпропіленової сітки, титанових пластин, фторопластових протезів, а також тривимірних (3D) друкованих імплантатів, виготовлених із титану та поліефірефіркетону (PEEK). У результаті дослідження оптимізовано підходи до вибору реконструктивних матеріалів для заміщення дефектів грудної стінки.
Одержано 20.02.2026
Прийнято до друку 24.02.2026
DOI: 10.32471/clinicaloncology.2663-466X.35550
ВСТУП
Пухлини грудної стінки можуть бути доброякісними або злоякісними та розподіляються на первинні, що походять із кісткової, хрящової, м’язової або м’якотканинних структур, і вторинні, які виникають унаслідок інвазії пухлин суміжних органів у грудну стінку або метастатичного ураження. Найчастіше вторинні пухлини грудної стінки відмічаються при раку грудної залози, м’яких тканин і легень. За даними наукової літератури, близько 50% усіх пухлин грудної стінки є злоякісними [1, 2].
Доброякісні пухлини грудної стінки можуть уражувати ребра, грудину та призводять до патологічних переломів та виникнення больового синдрому. Хірургічна резекція із відновленням каркасності та закриттям післяопераційного дефекту є стандартом лікування доброякісних пухлин грудної стінки [3].
Злоякісні пухлини грудної стінки часто інфільтрують магістральні судини середостіння, нервові сплетення, легені та перикард, що зумовлює необхідність ретельної передопераційної діагностики з використанням комп’ютерної (КТ), магнітно-резонансної томографії (МРТ), 3D-реконструкції КТ, а також високого рівня хірургічної техніки та анестезіологічного забезпечення. КТ є найбільш інформативним методом візуалізації пухлин грудної стінки. МРТ має переваги над КТ, особливо в оцінці стану м’яких тканин і поширеності пухлинного процесу на нервові структури. Позитронно-емісійна томографія (ПЕТ) використовується в окремих випадках для стадіювання захворювання, оцінки відповіді на лікування та виявлення рецидиву [4, 5].
Лікування злоякісних новоутворень передбачає мультидисциплінарний підхід із застосуванням неоад’ювантної поліхімієтерапії або внутрішньоартеріальної хімієтерапії чи променевої терапії [6].
Радикальна резекція місцево-поширених пухлин грудини, ребер і ключиці часто супроводжується формуванням значних дефектів грудної стінки, що потребують пластики та реконструкції. Наступним важливим завданням є відновлення каркасної функції грудної клітки, герметичності плевральної порожнини й адекватної дихальної функції та досягнення досконалого косметичного результату. Дефекти грудної стінки, які виникають після резекції ≥3 ребер передньобокових відділів, резекції або тотального видалення грудини, а також дефекти площею понад 70 см² у бічних або задніх відділах грудної стінки потребують реконструкції з метою запобігання респіраторній дисфункції та пошкодженню внутрішніх органів. Вибір сучасних протезних матеріалів і оптимальний періопераційний догляд є ключовими факторами покращення результатів лікування та довгострокової виживаності пацієнтів [7].
Для закриття дефектів грудної стінки хірурги використовують власні тканини пацієнта, зокрема різні типи клаптів: торако-епігастральний фасціошкірний клапоть, великий грудний м’яз, клапоть вертикального прямого м’яза живота (VRAM), краніально ніжковий клапоть поперечного прямого м’яза живота (TRAM), найширший м’яз спини, а також вільні клапті. Серед синтетичних матеріалів використовуються сітки із політетрафторетилену, біосинтетичні сітки та безклітинні дермальні матриці [5, 7, 8].
Титанові та нікелідтитанові пластини є перспективними матеріалами для жорсткої реконструкції грудини та ребер. PEEK, використаний у вигляді індивідуальних 3D-друкованих імплантатів, цінується провідними торакальними хірургами світу за свої біомеханічні властивості, близькі до кісткової тканини, а також вважається одним з найперспективніших матеріалів для закриття жорстких дефектів грудної стінки [5, 7, 8].
МАТЕРІАЛИ І МЕТОДИ дослідження
У відділенні пухлин легень та середостіння ДНП «НІР» у період з 2021 до 2025 рр. прооперовано 83 пацієнтів із доброякісними та злоякісними пухлинами грудної стінки. Серед пролікованих осіб виявлено такі гістологічні типи новоутворень: хондросаркома — 28 випадків (33,7%), ліпосаркома — 6 (7,2%), примітивна нейроектодермальна пухлина — 6 (7,2%), рабдоміосаркома — 4 (4,8%), ангіосаркома — 2 (2,4%), десмоїдна пухлина грудини — 4 (4,8%), фібросаркома — 4 (4,8%), рак легень з інвазією в грудну стінку — 3 (3,6%), саркома Юїнга — 2 (2,4%), герміногенні пухлини гемітораксу з інвазією в грудну стінку — 1 (1,2%), мезотеліома плеври з інвазією в грудну стінку — 1 (1,2%), хондробластома — 1 (1,2%), міксофібросаркома — 1 (1,2%), гемангіома — 1 (1,2%), нейрофіброма — 2 (2,4%), параосальна саркома — 1 (1,2%), рак шкіри з інвазією в грудну стінку — 1 (1,2%), шваннома — 1 (1,2%), гістіоцитома — 1 (1,2%), нейросаркома — 1 (1,2%), парагангліома — 1 (1,2%), гігантоклітинна пухлина — 1 (1,2%). Крім того, у 10 пацієнтів (12%) діагностовано метастатичне ураження грудної стінки при раку грудної залози, яєчників, передміхурової залози, нирки, колоректальному раку та раку щитоподібної залози (табл. 1).
| Морфологічні варіанти пухлин | Кількість пацієнтів |
| Хондросаркома | 28 |
| Ліпосаркома | 6 |
| Примітивна нейроектодермальна пухлина | 6 |
| Рабдоміосаркома | 4 |
| Ангіосаркома | 2 |
| Десмоїдна пухлина грудини | 4 |
| Фібросаркома | 4 |
| Рак легень з інвазією в грудну стінку | 3 |
| Саркома Юїнга | 2 |
| Герміногенні пухлини гемітораксу з інвазією в грудну стінку | 1 |
| Мезотеліома плеври з інвазією в грудну стінку | 1 |
| Хондробластома | 1 |
| Міксофібросаркома | 1 |
| Гемангіома | 1 |
| Нейрофіброма | 2 |
| Параосальна саркома | 1 |
| Рак шкіри з інвазією в грудну стінку | 1 |
| Шваннома | 1 |
| Гістіоцитома | 1 |
| Нейросаркома | 1 |
| Парагангліома | 1 |
| Гігантоклітинна пухлина | 1 |
| Метастази раку грудної залози, яєчників, передміхурової залози, нирки, колоректального раку, раку щитоподібної залози в грудну стінку | 10 |
| Усього | 83 |
Діагностичний алгоритм у пацієнтів із пухлинами грудної стінки включав проведення КТ з внутрішньовенним контрастуванням. За показаннями виконували 3D-реконструкцію магістральних судин середостіння та нервових сплетень, а також ангіографію судин пухлини з метою планування внутрішньоартеріальної хімієтерапії. Усім пацієнтам проведено біопсію пухлини з подальшим гістологічним та імуногістохімічним дослідженням. МРТ та остеосцинтиграфію використовували у частини пацієнтів для стадіювання захворювання, визначення поширеності пухлинного процесу та оцінки можливої інвазії в нервові структури хребта і плечового сплетення.
Мультидисциплінарний підхід до лікування злоякісних новоутворень передбачав використання неоад’ювантної поліхімієтерапії або внутрішньоартеріальної хімієтерапії чи променевої терапії відповідно до гістологічного типу пухлини та стадії захворювання. Водночас хірургічне втручання залишалось основним методом лікування пухлин грудної стінки та інколи єдиним ефективним методом у випадках резистентності новоутворення до хімієтерапії чи променевої терапії, а також при пухлинах, ускладнених розпадом і кровотечею. Радикальне хірургічне втручання сприяло найкращим показникам безрецидивної виживаності та якості життя пацієнтів.
Основним завданням онкохірургічного лікування було радикальне видалення пухлини з негативними краями резекції (R0) із дотриманням адекватного онкологічного відступу від пухлинної тканини, принципів м’язово-фасціальної футлярності та виконання резекції єдиним блоком. На етапі передопераційного планування хірург оцінював обсяг ураження грудини, ребер, ключиць і м’яких тканин грудної стінки за даними КТ та 3D-реконструкції з визначенням потенційних меж резекції та очікуваного розміру дефекту грудної стінки. Обсяг резекції залежав від гістологічного типу пухлини, її біологічної агресивності, а також первинного, метастатичного або рецидивного характеру процесу.
У ретроспективний аналіз включено випадки пацієнтів, що супроводжувалися формуванням значних дефектів грудної стінки, які потребували пластики та реконструкції. Наступним важливим етапом хірургічного лікування було відновлення каркасної функції грудної клітки, герметичності плевральної порожнини, адекватної дихальної функції, досягнення належного косметичного результату. Вибір матеріалу для реконструкції грудної стінки був індивідуалізованим і залежав від розміру дефекту, його локалізації, гістологічного типу пухлини.
У відділенні пухлин легень та середостіння ДНП «НІР» успішно виконуються складні та комбіновані оперативні втручання у пацієнтів, які раніше отримували лише паліативне лікування, зокрема при гігантських пухлинах грудної стінки з ураженням грудини, ребер, поширенням на магістральні судини середостіння, нервові сплетення, інвазією в перикард і легені, із використанням сучасних методів реконструкції дефектів грудної стінки.
Серед 83 прооперованих пацієнтів виконано такі обсяги резекції грудної стінки: резекція ручки та тіла грудини — у 10 випадках (12%), комбінована резекція грудини та ребер — у 16 (19,3%), резекція 1–3 ребер — у 16 (19,3%), резекція 4–7 ребер — у 15 (18,1%), резекція 8–12 ребер — у 17 (20,5%). Рецидивні пухлини грудної стінки, що потребували повторної реконструкції, відзначено у 9 хворих (10,8%) (табл. 2).
| Обсяги резекції грудної стінки | Кількість пацієнтів |
| Резекція ручки, тіла грудини | 10 |
| Комбінована резекція грудини та ребер | 16 |
| Резекція 1–3 ребер | 16 |
| Резекція 4–7 ребер | 15 |
| Резекція 8–12 ребер | 17 |
| Рецидивні пухлини грудної стінки, що потребували повторної пластики грудної стінки | 9 |
| Усього | 83 |
У період 2021–2025 рр. у відділенні виконано 45 (54,2%) комбінованих оперативних втручань із резекцією грудини, ребер, діафрагми, перикарда, хребців і магістральних судин середостіння із заміщенням дефектів грудної стінки як аутотрансплантатами, так і синтетичними матеріалами.
Для пластики невеликих дефектів грудної стінки ми використовували м’язові клапті найширшого м’яза спини та великого грудного м’яза. Дефекти передньо- та задньобокових відділів грудної стінки заміщували шляхом переміщення суміжного ребра в комбінації з м’язовими клаптями або із використанням поліпропіленової сітки. Відновлення каркасної функції бокової грудної стінки після резекції ≥3 ребер виконували з використанням поліпропіленової сітки, а для реконструкції після резекції 7 ребер та субтотальної резекції грудини використовували нікелідтитанові пластини в комбінації із поліпропіленовою сіткою.
Наведено клінічний випадок успішного ендопротезування ручки грудини зі встановленням індивідуально виготовлених пластикового та титанових імплантатів.
Пацієнтка, 39 років, з діагнозом раку яєчників T3cN1M0, стадія IIIC. Після проведення комплексного лікування зафіксовано прогресування захворювання у вигляді метастатичного ураження ручки грудини. Хворій проведено 6 курсів системної терапії та дистанційну променеву терапію. Незважаючи на проведене лікування, відмічено подальше прогресування через збільшення розмірів метастазу ручки грудини з її патологічним переломом.
За даними КТ органів грудної клітки візуалізовано пухлинне ураження ручки грудини з внутрішньогрудним компонентом праворуч та поширенням на 2-ге ребро справа (рис. 1).
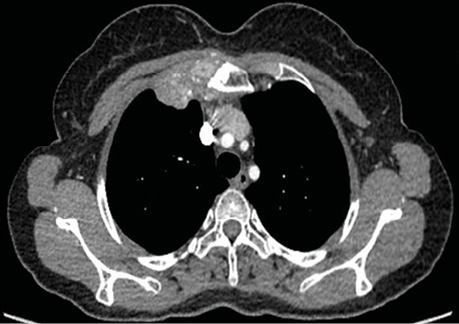
Рис. 1. КТ органів грудної клітки
3D-реконструкція КТ до оперативного втручання підтвердила деструкцію ручки грудини пухлинним процесом (рис. 2).
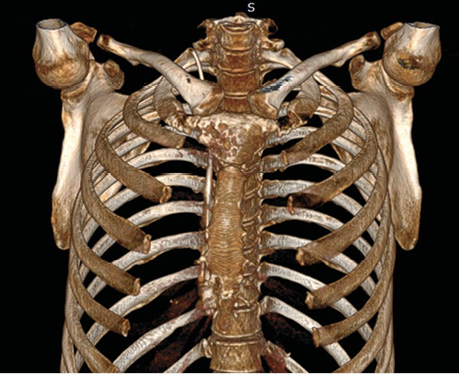
Рис. 2. 3D-реконструкція КТ
Пацієнтці виконано радикальне хірургічне лікування. Оперативний доступ — поперечна стернотомія на рівні 2-го міжребер’я. На 1-му етапі проведено мобілізацію структур переднього середостіння від ураженої ручки грудини та інтраторакального компонента пухлини. Ручку грудини видалено єдиним блоком разом із пухлиною (рис. 3).
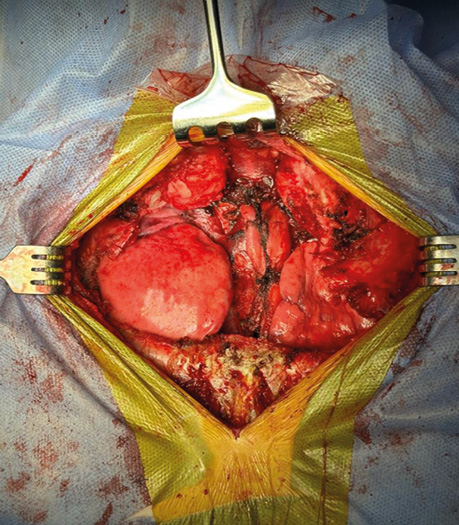
Рис. 3. Фото грудної стінки після радикального видалення пухлини
Інтраопераційний етап моделювання 3D-імплантату представлено на рис. 4.
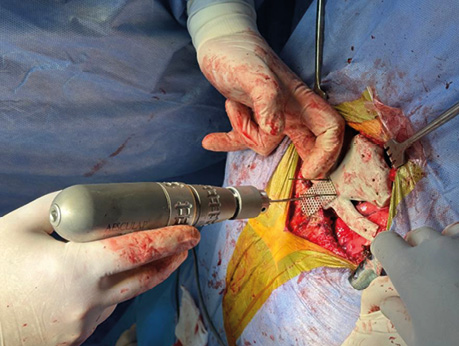
Рис. 4. Інтраопераційний етап моделювання
Ендопротезована ручка грудини з фрагментами других ребер справа і зліва, які фіксовані до тіла грудини титановими пластинами. Пластиковий імплантат ручки грудини додатково зафіксований до других ребер справа і зліва титановими пластинами, а також до правої та лівої ключиць за допомогою хірургічного сталевого дроту (Surgical Steel) (рис. 5).
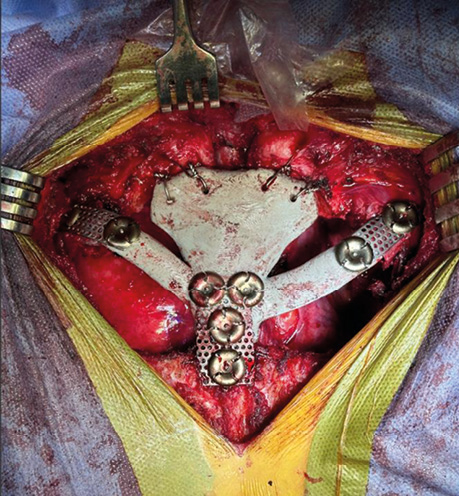
Рис. 5. Ендопротезована ручка грудини
Післяопераційну 3D-реконструкцію КТ перед випискою пацієнтки наведено на рис. 6.
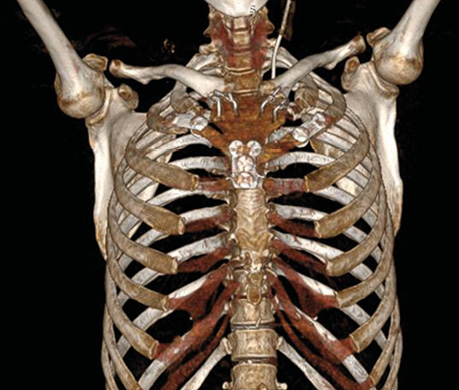
Рис. 6. Післяопераційна 3D-реконструкція КТ
РЕЗУЛЬТАТИ
Проведено ретроспективний аналіз результатів хірургічного лікування 83 пацієнтів із пухлинами грудної стінки, пролікованих у ДНП «НІР», яким виконували реконструкцію дефектів грудної стінки з використанням як аутотрансплантатів (м’язових клаптів, вільних TRAM-клаптів), так і синтетичних матеріалів, зокрема поліпропіленової сітки, індивідуально виготовлених 3D-імплантатів із титану та PEEK, а також нікелідтитанових пластин.
У клінічній практиці найчастіше використовували поліпропіленову сітку для закриття невеликих дефектів передньо- та задньобокових відділів грудної стінки, а також для реконструкції дефектів після резекції ручки та тіла грудини. Поліпропіленова сітка забезпечувала достатню стабільність при невеликих дефектах і дозволяла ефективно відновлювати цілісність грудної стінки.
Титанові та нікелідтитанові пластини успішно використали для жорсткої стабілізації, особливо при комбінованій реконструкції грудини та ребер. Використання цих матеріалів сприяло відновленню каркасної функції грудної клітки; водночас відзначено підвищений ризик ускладнень, зокрема переломів пластин, порушення загоєння післяопераційних ран та інфекційних ускладнень, що зумовлює необхідність зваженого та індивідуального підходу до вибору матеріалу для реконструкції.
У практиці відділення отримали успішний досвід реконструкції дефектів грудної стінки тривимірними друкованими імплантатами з титану та PEEK, які забезпечували точну анатомічну відповідність та надійну механічну стабільність, особливо поєднано з м’язово-шкірними клаптями, сприяли належним функціональним результатам та ефективному захисту органів грудної порожнини при великих дефектах грудної стінки, зумовлювали низьку частоту інфекційних ускладнень та забезпечували хороший косметичний результат.
Таким чином, вибір методу та матеріалу для реконструкції дефектів грудної стінки повинен бути індивідуалізованим та ґрунтуватися на розмірах і локалізації дефекту, гістологічному типі пухлини. Використання сучасних реконструктивних технологій, включно з 3D-друкованими імплантатами, дозволяє поліпшити функціональні результати лікування та якість життя пацієнтів.
ВИСНОВКИ
1. Сучасні реконструктивні можливості торакальної онкохірургії суттєво розширюють показання до оперативного лікування місцево-поширених пухлин грудної стінки, зокрема у пацієнтів із гігантськими новоутвореннями та пухлинами, що залучають грудину, ребра, легені і перикард, які раніше отримували виключно паліативне лікування.
2. У ДНП «НІР» на сьогодні накопичено успішний клінічний досвід закриття дефектів грудної стінки із використанням як аутотрансплантатів (м’язових клаптів, вільних TRAM-клаптів), так і синтетичних матеріалів, зокрема поліпропіленової сітки, та унікальні випадки використання 3D-імплантатів індивідуального друку із титану та PEEK, а також нікелідтитанових пластин.
3. Вибір матеріалу для відновлення каркасної функції грудної стінки є індивідуалізованим і залежить від розмірів та локалізації дефекту, а також від клінічного досвіду та практики використання протезних матеріалів онкохірургом.
4. Радикальне видалення пухлин грудної стінки R0 у комбінації з адекватною реконструкцією дефекту забезпечує найкращі результати безрецидивної виживаності та підвищення якості життя пацієнтів.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
1. Roos, E., van Coevorden, F., Verhoef, C., Wouters, M. W., Kroon, H. M., Hogendoorn, P. C. W., & van Houdt, W. J. (2016). Prognosis of primary and recurrent chondrosarcoma of the rib. Annals of Surgical Oncology, 23(3), 811–817. doi: 10.1245/s10434-015-4932-2.
2. Gao, H., Zhou, Y., Wang, Z., Zhao, R., & Qian, S. (2019). Clinical features and prognostic analysis of patients with chest wall chondrosarcoma. Medicine (Baltimore), 98(36), e17025. doi: 10.1097/MD.0000000000017025.
3. Widhe, B., & Bauer, H. (2011). Diagnostic difficulties and delays with chest wall chondrosarcoma: a Swedish population based Scandinavian Sarcoma Group study of 106 patients. Acta Oncologica, 50(3), 435–440. doi: 10.3109/0284186X.2010.486797.
4. Poulos, C. M., & Servais, E. L. (2025). Precision Medicine in Thoracic Surgery: Chest Wall, Pleural, and Mediastinal Malignancies. Thoracic Surgery Clinics, 35, 461–468. doi: 10.1016/j.thorsurg.2025.07.001.
5. Oreglio, C., Grimaldi, C., Gonfiotti, A., Fusi, G., Severi, E., Piccolo, R. L., … Facchini, F. (2025). Exploring the Role of Bioprosthesis for Chest Wall Reconstruction in Pediatric Oncology. Pediatric Blood & Cancer, 72, e32058. doi: 10.1002/pbc.32058.
6. Lin, C. W., Ho, T. Y., Yeh, C. W., Chen, H.-T., Chiang, I.-P., & Fong, Y.-C. (2021). Innovative chest wall reconstruction with a locking plate and cement spacer after radical resection of chondrosarcoma in the sternum: a case report. World Journal of Clinical Cases, 9(10), 2302–2311. doi: 10.12998/wjcc.v9.i10.2302.
7. Gonfiotti, A., Salvicchi, A., & Voltolini, L. (2022). Chest-Wall Tumors and Surgical Techniques: State-of-the-Art and Our Institutional Experience. Journal of Clinical Medicine, 11, 5516. doi: 10.3390/jcm11195516.
8. Petrella, F., Lo Iacono, G., Casiraghi, M., Gherzi, L., Prisciandaro, E., Garusi, C., & Spaggiari, L. (2020). Chest wall resection and reconstruction by composite prosthesis for locally recurrent breast carcinoma. Journal of Thoracic Disease, 12, 39–41. doi: 10.21037/jtd.2019.07.92.
Адреса для листування:
Борисюк Юрій Віталійович
03022, Київ, вул. Здановської Юлії, 33/43
Державне некомерційне підприємство «Національний інститут раку»
E-mail: dr.yurii.borysiuk@gmail.com
Correspondence:
Yurii Borysiuk
33/43 Yulii Zdanovskoi str., Kyiv, 03022
Nonprofit Organization National Cancer Institute
E-mail: dr.yurii.borysiuk@gmail.com














Leave a comment