Роль методов диссекции в резекционной хирургии печени
Бойко В.В. , Скорый Д.И. , Тищенко А.М. , Козлова Т.В.
Резюме. Применение разработанного тактического подхода у пациентов с первичным и метастатическим раком позволило уменьшить не только объем интраоперационной кровопотери с 995 до 563 мл, но и необходимость в трансфузии эритроцитарной массы с 72,2 до 56,8%. Общее количество осложнений уменьшилось более чем в 1,5 раза — с 37,7 до 21,3%. Ультразвуковая и водоструйная диссекции являются оптимальными для выполнения резекции печени. Применение методики «Clamp crushing» целесообразно лишь в сочетании с «Pringle maneuver».

Введение
Хирургическая гепатология является быстроразвивающимся направлением абдоминальной хирургии. Существенным вкладом в ее развитие стал прогресс в оказании анестезиологических пособий и реанимационных мероприятий, понимании хирургической анатомии печении и разработке новых технологий для диссекции печеночной паренхимы [1].
В настоящий момент предложено большое количество методик и аппаратов для диссекции, основанных на различных физических принципах. Большинство из них обладают свойством селективности, то есть позволяют разрушать печеночные клетки, оставляя при этом неповрежденными сосудистые и секреторные элементы печени, что в ходе резекции дает возможность их клипировать, коагулировать или лигировать, в зависимости от диаметра [2–5]. Тем не менее вопрос выбора того или иного метода диссекции продолжает решаться субъективно оперирующим хирургом.
Целью данного исследования явилось определение оптимальных методов диссекции для пациентов с первичным и метастатическим раком печени.
Материалы и методы
Дизайн исследования. За период 2007–2012 гг. в клинике ГУ «Институт общей и неотложной медицины НАМН Украины» выполнено 200 резекций печени у пациентов с очаговой ее патологией. Все пациенты условно разделены на 2 группы: основную и группу сравнения (рис. 1).
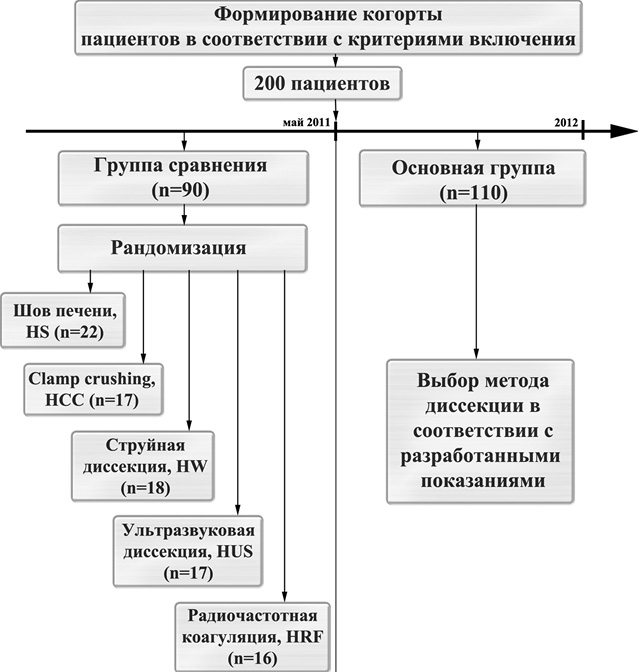
Группу сравнения составили 90 пациентов, рандомизированных для выполнения резекции печени с использованием одного из 5 методов диссекции ее паренхимы: рассечения скальпелем с предварительным наложением блоковидных швов, методики «Clamp crushing», струйной, ультразвуковой диссекции и радиочастотной (РЧ) коагуляции. В соответствии с методиками диссекции группа сравнения разделена на 5 подгрупп.
Каждый пациент группы сравнения, у которого планировали резекцию печени, за сутки до оперативного вмешательства рандомизирован с использованием запечатанных конвертов, где указана методика диссекции печеночной паренхимы (по 17 конвертов для каждого метода диссекции). В случае нерезектабельности конверт вновь запечатывали и возвращали в общую пачку, при выполненной резекции — удаляли. В связи с технической неисправностью РЧ коагулятора в одном случае оперирующий хирург заменил данный метод диссекции на водоструйный. Данная группа больных находились на лечении с 2007 по 2011 г. включительно. При этом в подгруппу пациентов, которым выполняли рассечение скальпелем с предварительным наложением блоковидных швов, добавлены 5 пациентов, оперированных до 2007 г., когда традиционно применяли лишь эту методику.
Основную группу составили 110 пациентов, у которых применены методики «Clamp crushing», струйной, ультразвуковой диссекции и рассечения паренхимы скальпелем с предварительным наложением блоковидных швов, но с учетом разработанных показаний на основе анализа результатов лечения пациентов группы сравнения. Данная группа больных находилась на лечении с мая 2011 г. по сентябрь 2012 г.
Предоперационное обследование, техника выполнения оперативных вмешательств, послеоперационная терапия не отличались в исследуемых группах. Афферентную васкулярную эксклюзию печени применяли лишь у пациентов группы «Clamp crushing». Резекцию у пациентов с диффузной патологией печени проводили с учетом критериев M. Makuuchi [6]. Исследуемые группы сопоставимы по характеру основной и сопутствующей патологии.
Хирургическая техника. При проведении каждой операции мы придерживались определенных условий. Анатомические резекции выполняли по стандартной методике с предварительной селективной деваскуляризацией удаляемого участка печени. Все резекции проведены с учетом принципов малообъемной инфузионной терапии при низких цифрах центрального венозного давления (0–50 мм. водн. ст.). Классификация резекций печени представлена согласно номенклатуре Международной гепатопанкреатобилиарной ассоциации Brisbane 2000 г.
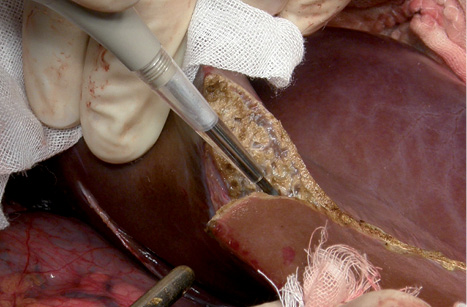
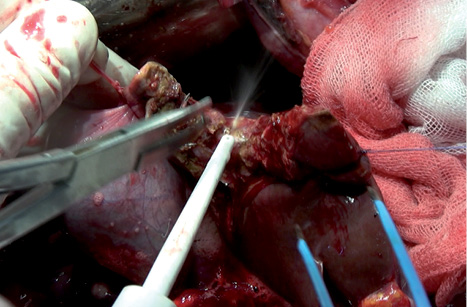
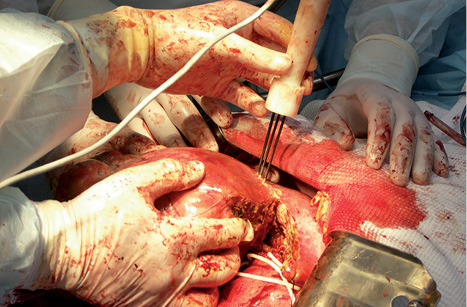
Ультразвуковым диссектором-аспиратором «Sonoca 300» («Soring», Германия) производили ультразвуковую диссекцию. В ходе операции использовали выгнутый макроинструмент, который работает в режиме «резания» (рис. 2). Водоструйную диссекцию (рис. 3) осуществляли аппаратом «Hydrojet» («Erbe», Германия). РЧ коагуляцию выполняли с помощью аппарата ЭХВЧ-150 «Фотек» (ООО «Фотек», Россия). При этом использовали трехигольчатый электрод и биполярный зажим (рис. 4, 5). Режимы работы аппаратов устанавливали, исходя из технической документации фирмы-производителя для операций на печени.
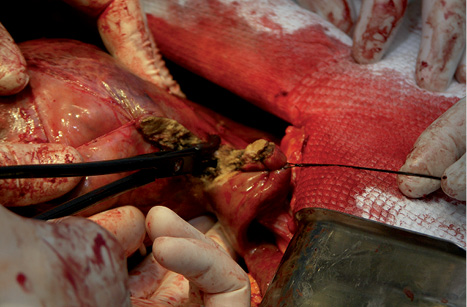
Инструментальную диссекцию проводили по традиционной методике «Clamp crushing» с использованием «мягкого» зажима типа Бильрот (рис. 6). Разделение паренхимы скальпелем выполняли после предварительного ее прошивания блоковидными швами, непосредственно по краю резекции, на всю толщину нитью «Викрил» (рис. 7).
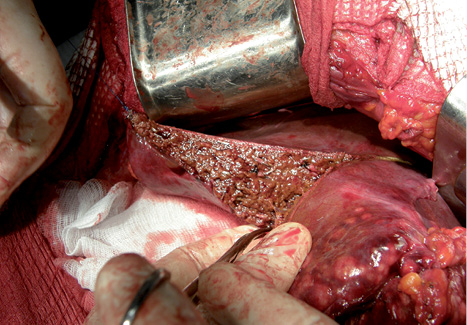
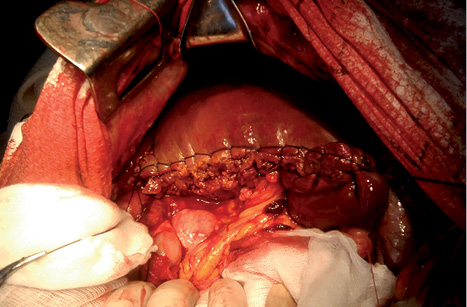
При выполнении селективной диссекции, вне зависимости от используемых аппаратов, в плоскости резекции разрушалась паренхима печени, при этом сосуды и протоки диаметром >1 мм оставались неповрежденными. Это давало возможность их дополнительно обрабатывать, для чего трубчатые структуры диаметром <1 мм коагулировали, от 1 до 3 мм — клипировали и >3 мм — прошивали атравматической нитью, размер которой выбирали в зависимости от их диаметра.
Критерии оценки. Основными количественными показателями, характеризующими эффективность того или иного метода диссекции, регистрируемыми в ходе оперативного вмешательства, были: объем кровопотери на этапе диссекции, время диссекции, площадь резекционной поверхности. Анестезиолог проводил оценку объема кровопотери, которая в каждом случае состояла из количества крови, накопленной в емкости для сбора (за вычетом раствора для диссекции), и объемом в использованном материале (перевязочный материал). Мы принимали равенство единицы массы и объема крови. Показатель объема кровопотери регистрировали до этапа диссекции, на его протяжении и после окончания операции.
Для возможности сравнения эффективности диссекции рассчитаны следующие показатели. Скорость диссекции печеночной паренхимы — отношение площади резекционной поверхности ко времени резекции (см²/мин), удельная кровопотеря — отношение объема кровопотери на этапе резекции к площади резекционной поверхности (мл/см).
Показателем для выполнения трансфузии эритроцитарной массы считали снижение уровня гемоглобина <70 г/л. Оценивали также осложнения, которые развивались в послеоперационный период. Сроки наблюдения за больными составили от 3 мес до 5 лет.
Статистическую обработку полученных результатов проводили методом вариационной статистики с помощью компьютерной программы Stat Plus 2009. Достоверность полученных данных не ниже 0,95.
Результаты и их обсуждение
Результаты рандомизированного исследования и их обсуждение. Основные показатели эффективности различных методов диссекции представлены в табл. 1. Как видно из данных (см. табл. 1), из всех анализируемых методов диссекции наибольшей скоростью обладает методика рассечения паренхимы скальпелем с предварительным наложением блоковидных швов — 4,2±0,06 см²/мин. Методы РЧ коагуляции и «Clamp crushing» уступают по данному показателю, который составляет соответственно 4,0±0,02 и 3,6±0,03 см²/мин. Различия между показателями статистически достоверны (р<0,05). Ультразвуковая и струйная методики обладают наименьшей скоростью диссекции, которая составляет соответственно 2,2±0,04 и 2,3±0,03 см²/мин. Причем различия между показателями статистически недостоверны (р>0,05).
Таблица 1. Сравнительная оценка эффективности применения различных способов диссекции печеночной паренхимы
| Показатель | Шов печени | РЧ коагуляция | «Clamp crushing» | Ультразвуковая | Струйная |
|---|---|---|---|---|---|
| Средняя скорость диссекции, см²/мин | 4,2±0,06 | 4,0±0,02 | 3,6±0,03 | 2,2±0,04 | 2,3±0,03 |
| Удельная кровопотеря, мл/см² | 7,5±0,24 | 5,9±0,11 | 6,8±0,1 | 3,4±0,08 | 3,6±0,11 |
| Средний объем кровопотери на этапе диссекции, мл | 605,6±46,8 | 510,8±29,7 | 575,3±55,9 | 237,1±23,3 | 303,9±26,4 |
| % пациентов, которым не проводили трансфузию эритроцитарной массы | 31,8 | 6,3 | 17,6 | 35,3 | 44,4 |
Показатель удельной кровопотери на этапе диссекции был максимальным при применении метода рассечения паренхимы печени скальпелем с предварительным наложением блоковидных швов и составил 7,5±0,24 мл/мин. Следующими в сторону уменьшения удельной кровопотери были методики «Clamp crushing» и РЧ коагуляция, показатели которых составили соответственно 6,8±0,1 и 5,9±0,11 мл/см². Причем различие между тремя вышеуказанными показателями достоверны (р<0,05). Ультразвуковая и струйные методики сопряжены с наименьшей удельной кровопотерей, которая составляет соответственно 3,4±0,63 и 3,6±0,96 мл/см². Причем различия между показателями статистически недостоверны (р>0,05).
Из всех исследуемых подгрупп наибольшим процентом пациентов, которым не проводили трансфузию эритроцитарной массы в интра- и послеоперационный период, были подгруппы, где применяли методики ультразвуковой и струйной диссекции. Данные показатели составили 35,3 и 44,4% соответственно. В группе пациентов, у которых проводили рассечение паренхимы скальпелем с предварительным наложением блоковидных швов, данный показатель составил 31,8%. При максимальных показателях удельной и средней кровопотери на этапе диссекции в данной подгруппе этот факт объясняется наибольшим количеством пациентов, которым выполняли атипичные (краевые) резекции печени.
Что же касается результатов хирургического лечения пациентов с объемными образованиями печени с применением различных методов диссекции печеночной паренхимы, то наибольшим процентом пациентов, у которых возникли осложнения в послеоперационный период, характеризовалась подгруппа, где применяли рассечение паренхимы скальпелем с предварительным наложением блоковидных швов. Этот показатель составил 54,5%. Несколько меньше осложнений возникло в подгруппе, где проводили РЧ коагуляцию, данный показатель составил 50%. Наименьшее количество осложнений возникло в подгруппах ультразвуковой и струйной диссекции, где процент пациентов с осложнениями был равен 23,5 и 22,2% соответственно. Методика «Clamp crushing» заняла промежуточное положение, данный показатель составил 29,4%.
В структуре осложнений желчеистечение имело место лишь в подгруппах пациентов, у которых применен блоковидный шов печени (22,7%) и РЧ коагуляция (31,3%). В отличие от остальных методик, они не сопровождаются селективным выделением и обработкой трубчатых структур (артериальные, портальные, венозные сосуды и желчные протоки), а герметизация достигается сдавлением паренхимы швами или «завариванием» их просвета с помощью РЧ коагулятора. Как показали наши морфологические исследования, применение этих методов диссекции неминуемо сопровождается ишемическими изменениями в зоне резекционной поверхности, что и является пусковым моментом для последующей разгерметизации билиарного дерева или сосудистой системы печени. В подтверждение этому единственное кровотечение из резекционной поверхности имело место в подгруппе, у которой использованы блоковидные швы на печень (4,5%).
Проведенный комплексный анализ позволил сформировать концепцию применения методов диссекции у пациентов основной группы. При выполнении плановой резекции печени приоритет нужно отдавать ультразвуковой или струйной диссекции печеночной паренхимы, которая, несмотря на низкую скорость диссекции, обладает минимальной кровопотерей, количеством послеоперационных осложнений. Методика «Clamp crushing» нуждается в сочетании с одним из методов афферентной васкулярной эксклюзии печени и не должна применяться у пациентов с маргинальным объемом резекции.
Методики рассечения паренхимы скальпелем с предварительным наложением блоковидных швов и РЧ коагуляции могут быть применены лишь при выполнении экономных резекций печени у пациентов неонкологического профиля.
Результаты лечения пациентов онкологического профиля и их обсуждение. 55,5% пациентов основной группы и 58,9% группы сравнения оперированы по поводу первичного или метастатического рака печени. Структура онкологической патологии исследуемых групп представлена в табл. 2.
Таблица 2. Характер онкологической патологии в исследуемых группах
| Характер основного заболевания | Основная группа | Группа сравнения |
|---|---|---|
| Гепатоцеллюлярная карцинома | 16 (14,6%) | 13 (14,4%) |
| Холангиоцеллюлярная карцинома | 10 (9,1%) | 6 (6,7%) |
| Цистаденокарцинома | – | 1 (1,1%) |
Метастатический рак печени:
|
35 (31,8%) 21 (19,1%) 12 (10,9%) 2 (1,8%) |
32 (35,5%) 18 (20%) 11 (1,2%) 3 (3,3%) |
| Лимфосаркома | – | 1 (1,1%) |
| Всего | 61 (55,5%) | 53 (58,9%) |
Поскольку течение послеоперационного периода, частота и тяжесть возможных осложнений в значительной мере зависят от объема резекции, мы представили распределение пациентов исследуемых групп в зависимости от выполненного объема резекции печени на подгруппы (табл. 3).
Таблица 3. Объем резекций печени в исследуемых группах
| Объем резекции | Основная группа | Группа сравнения |
|---|---|---|
| Резекция 1 сегмента | 10 | 9 |
| Удаление 2 сегментов | 10 | 11 |
| Удаление 3 сегментов | 11 | 9 |
| Гемигепатэктомия | 15 | 11 |
| Расширенная гемигепатэктомия | 7 | 5 |
| Неанатомическая резекция | 8 | 8 |
| Всего | 61 | 53 |
Из представленных данных (см. табл. 3) видно, что группы сопоставимы по характеру и объему выполненных оперативных вмешательств.
Применение разработанного тактического подхода в выборе метода диссекции позволило существенно уменьшить объем общей кровопотери во время операции. Медиана данного показателя в группе сравнения составила 995 мл (135–3500 мл), а в основной — 563 мл (128–999 мл). Различия между показателями статистически достоверны (р=0,009).
Безусловно, это отразилось и на количестве пациентов, у которых не проводили трансфузию эритроцитарной массы в интра- и послеоперационный период. Данный показатель в группе сравнения составил 27,8%, а в основной увеличился практически вдвое, достигнув значения 43,2%.
Как видно из вышеизложенного, применение разработанного тактического подхода позволило уменьшить не только объем интраоперационной кровопотери, но необходимость в трансфузии эритроцитарной массы. Эти показатели являются одними из основных критериев, влияющих на количество послеоперационных осложнений и отдаленные результаты лечения пациентов с первичным и метастатическим раком печени.
После резекций печени, независимо от ее объема, различного рода осложнения отмечали как в основной группе, так и в группе сравнения. Все виды осложнений в послеоперационный период мы условно разделили на 2 группы: специфические (характерные именно для резекции печени) и общехирургические (табл. 4).
Таблица 4. Характер послеоперационных осложнений в основной группе и группе сравнения
| Осложнения | Основная группа | Группа сравнения |
|---|---|---|
| Специфические | 18,0% | 27,8% |
| Общехирургические | 3,3% | 8,9% |
| Всего | 21,3% | 37,7% |
Общее количество осложнений уменьшилось более чем в 1,5 раза — с 37,7 до 21,3%, как за счет уменьшения специфических осложнений, так и общехирургических. Данный факт мы объясняем, с одной стороны, снижением травматичности диссекции, а с другой — достоверным уменьшением объема интраоперационной кровопотери.
В структуре осложнений количество желчеистечений уменьшилось более чем в 3 раза, в связи с чем в основной группе удалось избежать такого осложнения, как билома и поддиафрагмальный абсцесс. В этой же группе мы не выявили кровотечения из резекционной поверхности в послеоперационный период, для лечения которого в группе сравнения потребовалась срочная релапаротомия. Печеночная недостаточность имела место в основной группе у 3 (4,9%) пациентов, что было практически в 2 раза ниже, чем в группе сравнения, где данный показатель составил 9,4%. Причем у всех пациентов основной группы на фоне консервативных мероприятий явления печеночной недостаточности были купированы.
Вышеуказанные осложнения, по нашему мнению, характеризуют качество обработки резекционной поверхности печени. Методики наложения блоковидных швов и тотальной коагуляции с «завариванием» трубчатых структур приводят к ишемическим изменениям в зоне диссекции, что в дальнейшем и отражается на разгерметизации билиарного дерева. Кроме того, дополнительная ишемия приводит к уменьшению объема остаточной паренхимы, что также может послужить дополнительным фактором для развития печеночной недостаточности при выполнении резекции большого объема.
Реактивный правосторонний плеврит мы рассматривали как неотъемлемую реакцию на мобилизацию печени, однако снижение частоты данного осложнения с 16,9% в группе сравнения до 8,1% в основной группе свидетельствует о влиянии метода диссекции на развитие данного осложнения.
Послеоперационная летальность в группе сравнения составила 7,5%, в основной группе — 3,1%.
Учитывая то, что длительность наблюдения 50% пациентов основной группы составляет не более 6 мес, мы не представляем в данной статье сравнение отдаленных результатов лечения в исследуемых группах.
Выводы
При выполнении плановой резекции печени у пациентов с первичным и метастатическим раком печени целесообразно применение ультразвуковой, струйной диссекции или методики «Clamp crushing».
Применение методики «Clamp crushing» является эффективным лишь в сочетании с одним из методов афферентной васкулярной эксклюзии печени.
У пациентов с маргинальным объемом резекции допустимыми являются лишь методики струйной или ультразвуковой диссекции.
Применение методов рассечения паренхимы скальпелем с предварительным наложением блоковидных швов и РЧ коагуляции у пациентов с первичным и метастатическим раком печени является нецелесообразным ввиду большой травматичности, высокого риска как интра-, так и послеоперационных осложнений и, соответственно, худшего прогноза отдаленных результатов лечения.
Список использованной литературы
1. Скорый Д.И. (2011) Каким способом выполнять диссекцию печеночной паренхимы? Оценка эффективности и травматичности четырех техник в семи рандомизированных исследованиях. Укр. журн. хір., 4(13): 260–265.
2. Arita J., Hasegawa K., Kokudo N. et al. (2005) Randomized clinical trial of the effect of a saline-linked radiofrequency coagulator on blood loss during hepatic resection. Br. J. Surg., 92: 954–959.
3. Delis S., Bakoyiannis A., Tassopoulos N. (2009) Clamp–crush technique vs. radiofrequency-assisted liver resection for primary and metastatic liver neoplasms. HPB, 11: 339–344.
4. Koo BN., Kil HK., Choi JS. et al. (2005) Hepatic resection by the Cavitron ultrasonic surgical aspirator increases the incidence and severity of venous air embolism. Anesth. Anal., 101: 966–970.
5. Smyrniotis V., Arkadopoulos N., Kostopanagiotou G. et al. (2005) Sharp liver transection vs. clamp crushing technique in liver resections: a prospective study. Surgery, 137: 306–311.
6. Makuuchi M., Kosuge T., Takayama T. et al. (1993)Surgery for small liver cancers. Semin. Surg. Oncol., 9: 298–304.
Роль методів дисекції в резекційній хірургії печінки
Резюме. Застосування розробленого тактичного підходу в пацієнтів з первинним і метастатичним раком дозволило зменшити не лише обсяг інтраопераційної крововтрати з 995 до 563 мл, а й необхідність трансфузії еритроцитарної маси з 72,2 до 56,8%. Загальна кількість ускладнень зменшилася більш ніж в 1,5 разу — з 37,7 до 21,3%. Ультразвукова та водоструминна дисекції є оптимальними для проведення резекції печінки. Застосування методики «Сlamp crushing» є доцільним лише в поєднанні з «Pringle maneuver».
Ключові слова: резекція печінки, дисекція печінки, первинний рак печінки, метастатичний рак печінки.
Liver transection methods. Efficient for liver resection
Summary. New tactical approach in patients with primary and metastatic cancer has reduced blood loss from 995 to 563 ml, and transfusion of red blood cells from 72,2 to 56,8%. The total number of complications has decreased by more than 1.5 times — from 37,7 to 21,3%. The ultrasonic and Hydrojet were the most efficient devices. Clamp crush technique should be used only with Pringle maneuver.
Key words: liver resection, liver transection, liver cancer, metastatic liver cancer.














Leave a comment