Необоротна електропорація як альтернативний метод лікування в онкології: клінічне застосування, сучасні можливості методу та майбутні перспективи (огляд медичної літератури)
Мовчан В.І., Стаховський Е.О., Войленко О.А., Вітрук Ю.В., Стаховський О.Е., Кононенко О.А., Васильонок Я.В.
Резюме. Необоротна електропорація (НОЕ; англ. irreversible electroporation — IRE) — новітня абляційна методика, що полягає в застосуванні імпульсного електричного поля з метою локального впливу на пухлинні клітини, їх деструкції без пошкодження позаклітинного матриксу. Основним механізмом дії є утворення нанопор у зовнішньому біліпідному шарі клітин та перешкоджання відновленню його нормальної структури, що, своєю чергою, запускає подальший каскад реакцій та в кінцевому результаті зумовлює загибель клітин. Станом на сьогодні існує велика кількість досліджень з використання НОЕ як у режимі монотерапії, так і в комбінації з іншими перспективними методиками. Усе спрямовано на досягнення якнайкращих онкологічних та функціональних результатів, забезпечення належної якості життя пацієнта. Ця робота є продовженням статті «Необоротна електропорація як альтернативний метод лікування в онкології: біофізичні та молекулярні механізми, технічні аспекти та сучасні можливості методу (огляд наукової літератури)» авторів В.І. Мовчан, Е.О. Стаховський, О.А. Войленко, Ю.В. Вітрук, О.Е. Стаховський, О.А. Кононенко та О.В. Романенко (2025) [1], де висвітлено підґрунтя методу НОЕ. У цій статті на основі огляду профільної літератури наведено приклади практичного використання НОЕ для лікування злоякісних новоутворень, проаналізовано та представлено результати декількох фундаментальних клінічних досліджень. Акцент зроблено на лікування пацієнтів переважно з пухлинами нирок, передміхурової залози та печінки. Окрема увага приділяється перспективним напрямкам лікування, як-от електрохімієтерапія, електролітична НОЕ.
Одержано 26.02.2026
Прийнято до друку 9.03.2026
DOI: 10.32471/clinicaloncology.2663-466X.35701
ВСТУП
Фокус сучасної онкології все частіше зміщується в бік органозберігальних та мінімально інвазивних методів лікування, що дозволяють ефективно контролювати пухлинний процес із мінімальним впливом на якість життя пацієнтів. Традиційні методи абляції, зокрема радіочастотна (Radiofrequency Ablation — RFA) та мікрохвильова абляція (Microwave Ablation — MWA), хоча й широко використовуються, мають низку обмежень, пов’язаних із термічним пошкодженням навколишніх структур.
НОЕ належить до методів нетермічної абляції, що базується на використанні високовольтних електричних імпульсів, які утворюються між парами електродів, розміщених навколо пухлини [1]. Перевага НОЕ над методами термічної абляції полягає в максимальній селективності. При її проведенні не відбувається пошкодження або процедура проходить з мінімальним пошкодженням прилеглих до пухлини структур (судин, нервів, проток), що дозволяє працювати у випадку складнодоступних локалізацій пухлин. Ця перевага є ключовою, вона дозволяє розширити сферу використання фокальної терапії та забезпечити кращий функціональний результат.
Такий метод фокальної терапії, як променева терапія, а також хірургічні методики доволі часто знижують якість життя пацієнтів, маючи високі рівні ускладнень. НОЕ проявила себе в якості безпечного малоінвазивного органозберігального методу лікування осіб з локалізованими пухлинами як у разі первинної терапії, так і терапії резидуальних і рецидивних пухлин, та зі значно нижчими рівнями післяопераційних ускладнень.
У статті наведено клінічні результати використання НОЕ при пухлинах нирок [2, 3], передміхурової залози [4, 5] та печінки [6, 7], проаналізовано функціональні та онкологічні показники, частоту ускладнень, рецидивування та виживаність. Окремо розглянуто перспективні напрямки:
- електролітичну НОЕ (Е-НОЕ; англ. E-IRE) для розширення зони абляції [8];
- електрохімієтерапію як синергію оборотної електропорації з цитостатиками [9];
- комбінування НОE з радіотерапією з потенційним посиленням системної імунної відповіді [10].
Отже, НОЕ постає інноваційним та потенційно ключовим методом персоналізованої онкотерапії, який здатний у майбутньому доповнити або частково замінити традиційні абляційні та хірургічні втручання.
КЛІНІЧНЕ ВИКОРИСТАННЯ МЕТОДИКИ НОЕ В ОНКОЛОГІЇ
Клінічні ніші, де НОЕ має перевагу
Аденокарцинома передміхурової залози
НОЕ ефективно використовується при лікуванні раку передміхурової залози, забезпечуючи належний онкологічний результат та майже не змінюючи якість життя пацієнтів, часто зберігаючи нормальну статеву функцію та функцію утримання сечі, які переважно порушуються іншими методами лікування. Клінічні дослідження свідчать про безпеку та доцільність НОЕ при раку передміхурової залози з низьким рівнем побічних явищ.
У проведеному ретроспективному аналізі даних 45 історій хвороб пацієнтів, яким у період 2018–2022 рр. виконано фокальну терапію раку передміхурової залози з використанням НОЕ [4]. Встановлено, що метод зумовив хороші онкологічні результати як у випадку первинної терапії (N-38), так і у вигляді терапії порятунку після неефективної дистанційної променевої терапії або брахітерапії та андроген-деприваційної терапії (АДТ) (N-7) (рис. 1).
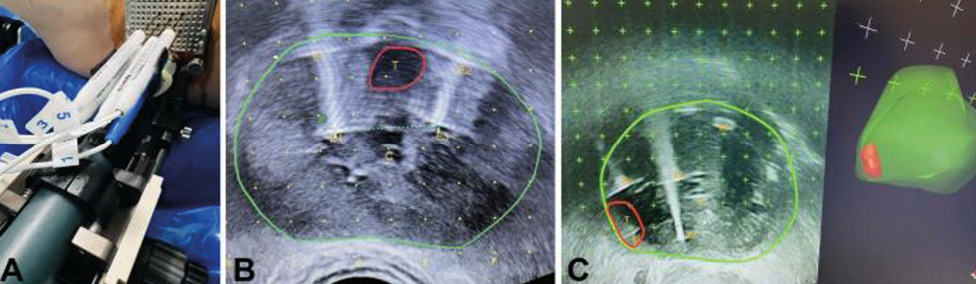
Рис. 1. Проведення процедури НОЕ (NanoKnife): a) — електроди, введені через сітку для промежинної біопсії, паралельно до ультразвукового датчика; b) — пацієнт з групи первинного лікування. Ультразвукове поперечне зображення, зеленим кольором позначено контур передміхурової залози, червоним — ділянку ураження. T — пухлина; E — електрод (1–4); C — катетер. Пухлина оточена безпечним краєм; c) — пацієнт з групи терапії порятунку після невдалої брахітерапії. Справа ураження (червоне) і передміхурова залоза (зелена) в 3D-вигляді (Bio-Jet, Fusion system, BK ultrasound). Поперечний вигляд; T — пухлина; E — електрод (1–4); BS — насінини для брахітерапії. Ураження знаходиться справа постеролатерально в Mid-сегменті передміхурової залози. Електроди оточують ураження, з урахуванням безпечного краю [цит. за 2]
У групі первинного лікування середній рівень простатоспецифічного антигену (ПСА) через 6 міс після лікування становив 3,4 нг/мл (0,8–16,3) порівняно із середнім показником до лікування 5,6 нг/мл (1,5–25), що свідчить про зниження на 39%. При контрольній мультипараметричній МРТ (мпМРТ) (рис. 2) через 6 міс після лікування у 84% пацієнтів (25/38) не було ознак хвороби при порівнянні результатів мпМРТ (Prostate Imaging Reporting and Data System — PI-RADS) = 2, тоді як у 12% виявлено нові підозрілі вогнища ураження поза межами зони абляції (PI-RADS >3), а у 4% зберігалося ураження в межах зони абляції. Контроль промежинної біопсії проведено через 1 рік після лікування (раніше, якщо на МРТ були ознаки залишкової хвороби) 13 пацієнтам. У 69% не виявлено ознак захворювання, у 31% (N-4) діагностовано клінічно значущий рак передміхурової залози за межами зон абляції (ISUP >2), клінічно значущих уражень у межах зони абляції не зафіксовано у жодного хворого. Загалом впродовж 1 року після лікування 2 пацієнти пройшли повторну НОЕ, а 1 — радикальну простатектомію, отже, 97% пацієнтів перебували під активним спостереженням. Через 2 роки із 13 пацієнтів двом проведено радикальну простатектомію, 4 пройшли повторну НОЕ і загалом 84% (11/13) залишалися під АС.
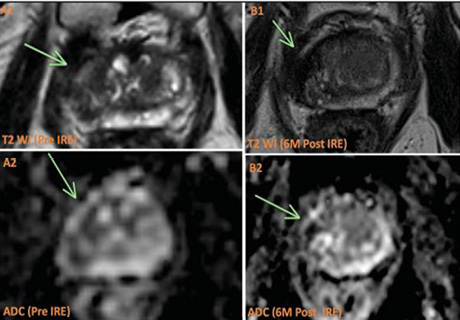
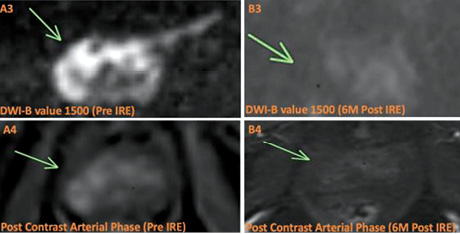
Рис. 2. МРТ передміхурової залози до та після лікування за допомогою НОЕ. Пацієнт віком 75 років із нещодавно діагностованою злоякісною пухлиною, ISUP 2, у периферійній зоні (PZ) справа, що охоплює верхівку та середню частину цієї залози. (a) МРТ до лікування. У PZ на Т2-WI видно низьку інтенсивність сигналу (стрілка) (a1), що відповідає обмеженому низькому сигналу ADC (a2) та високому сигналу на DWI (a3). Це корелювало з артеріальним підсиленням (a4). (b) МРТ через 6 міс після лікування. Відмічається підвищення низького сигналу на Т2-WI у зоні лікування, що є наслідком очікуваної атрофії (b1), з неоднорідним сигналом на ADC (b2) та відсутністю обмеження на DWI (b3). Крім того, підсилення більше не виявляється (b4) [цит. за 2]
Примітки: ISUP — ступінь агресивності раку передміхурової залози за класифікацією Міжнародного товариства урологічної патології (International Society of Urological Pathology); Т2-WI — Т2-зважені зображення; DWI — дифузійно-зважені зображення.
У групі терапії порятунку медіана ПСА через 6 міс становила 22 нг/дл (4–34) (заявлені одиниці вимірювання нг/дл, при переведенні величин до стандартних одиниць виміру, показник відповідатиме 2,2 нг/мл (0,4–3,4)). Показник ПСА до лікування становив 11,9 нг/мл (4–28). 71% хворих (5/7) пройшли мпМРТ через 6 міс. 60% не мали ознак захворювання (PI-RADS 2), а 40% мали вогнища ураження поза межами ділянки абляції (PI-RADS >3). На мпМРТ не зафіксовано вогнищ ураження в межах обробленої ділянки. При спостереженні через 1 рік 3 пацієнти з групи отримували гормональну терапію (1 через поширення ураження на сім’яний пухирець та 2 через спалах COVID-19 і неможливість продовжувати спостереження), а 4 особи (57%) перебували під активним спостереженням та не отримували гормональну терапію.
Загальна виживаність в обох групах протягом усього періоду спостереження становила 100%.
У післяопераційний період уретральний катетер залишався в середньому на 5 (5–7) днів, жоден з пацієнтів не був госпіталізований на ніч і ніхто не потребував повторної госпіталізації. Не зафіксовано ускладнень за шкалою Clavien – Dindo >1. Не встановлено випадків нетримання сечі (усі пацієнти мали повне утримання відразу після видалення катетера, з повним контролем, як і до операції), і не зафіксовано жодних фістул. Незначне зниження сексуальної функції (ерекції) виявлено у 2/38 пацієнтів у первинній групі, що перевищувало їхній базовий рівень (5,2%), ефективно проліковано за допомогою інгібіторів фосфодіестерази 5-го типу, еякуляція залишилася без змін.
У більш ранньому мультицентровому дослідженні з визначення безпеки, функціональних та онкологічних результатів НОЕ для абляції раку передміхурової залози, проведеному у 2015–2020 рр. [5], отримано хороші функціональні та задовільні онкологічні результати й низький рівень ускладнень, проте автори наголошують на важливості якісних методів променевої діагностики та контролі промежинної біопсії через 12–18 міс після лікування з метою отримання більш достовірних статистичних даних.
Дослідження охоплювало 411 пацієнтів, середній вік становив 67,3±7,4 року, середній час спостереження — 24 міс (15–36). Популяція дослідження складалася з пацієнтів з гістологічно підтвердженим раком передміхурової залози, з них ISUP 1 мали 126 осіб (30,7%), ISUP 2 — 193 (47,1), ISUP 3 — 58 (14,1), ISUP 4 — 12 (2,9), ISUP 5 — 17 (4,1). Усім пацієнтам до лікування виконано мпМРТ. Середній об’єм передміхурової залози, згідно з даними МРТ, становив 44,3±21,2 см3, пухлина сT1c наявна у 182 хворих (46,8%), сТ2а — 101 (26,0), сТ2b — 37 (9,5), сТ2с — 65 (16,7), сТ3а — 3 (0,8), сТ3b 1 (0,3). Середній рівень ПСА — 6,3 нг/мл (4,4–9,0).
Для того щоб відобразити реальні дані, у протоколі дослідження не було конкретних критеріїв виключення.
Первинним результатом була частота рецидивів раку передміхурової залози через 1 рік. Пацієнтам запропоновано провести біопсію передміхурової залози через 1 рік після НОЕ.
Вторинні результати включали функціональні результати, виміряні за допомогою опитувальників «Міжнародна система сумарної оцінки захворювань передміхурової залози» (International Prostate Symptom Score — IPSS) та «Міжнародний індекс еректильної функції» (International Index of Erectile Function, 5th version — IIEF-5), а також профіль безпеки НОЕ, який оцінювали за пов’язаними з лікуванням ускладненнями.
Серйозним недоліком дослідження були втрати великої кількості пацієнтів для подальшого спостереження. Усього 28,2% пацієнтів (116/411) проведено контроль біопсії передміхурової залози, з них клінічно значущий рак передміхурової залози встановлено у 24,1% (28/116), клінічно незначущий — у 35,3% (41/116). Важливим висновком цього дослідження стало те, що частота рецидивів не була пов’язана зі ступенем ISUP на початковому етапі, що свідчить про те, що розширення показань до НОЕ може бути безпечним.
Також у цьому дослідженні вказується на значне підвищення рівня ПСА в перші 24 год після терапії НОЕ і його подальше різке зниження на 96,2% протягом наступних 3 міс. Через рік рівень ПСА у пацієнтів з позитивним результатом біопсії був достовірно вищим, ніж у пацієнтів з негативним (5,2 нг/мл проти 2,7 нг/мл, р <0,01) (рис. 3).
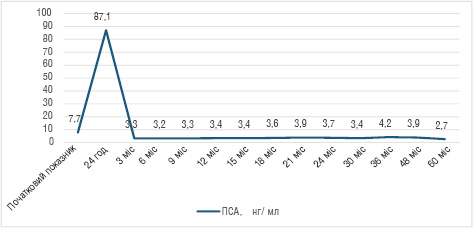
Рис. 3. Зміна показників ПСА — до лікування, 24 год після лікування та при кожному контролі протягом періоду спостереження [цит. за 3]
При 3-місячному спостереженні показник за шкалою IPSS значно підвищився з 7,1 до 8,2 (p=0,015) порівняно з базовим рівнем. Через 6 міс він знизився до 6,1 і досяг ще нижчого показника, ніж вихідний рівень (p=0,017). Після цього рівень IPSS залишався стабільним протягом спостереження.
Показник IIEF-5 знизився через 3 міс з 16,0 до 12,1 (p <0,001). Хоча рівень IIEF-5 був статистично нижчим у кожній точці спостереження, ніж базовий рівень, він залишався на однаковому рівні (табл. 1).
| Показник | Період спостереження, міс | ||||||
| 3 | 6 | 9 | 12 | 18 | 24 | 30 | |
| IPSS | |||||||
| n, парні показники | 215 | 160 | 123 | 117 | 72 | 63 | 42 |
| Початковий показник | 7,1±5,8 | 7,1±5,9 | 7,7±5,9 | 7,4±6,0 | 7,7±6,4 | 8,5±6,7 | 8,6±6,3 |
| Період спостереження | 8,2±5,9 | 6,1±5,5 | 7,2±6,5 | 6,4±5,0 | 7,8±6,4 | 8,1±5,6 | 8,7±8,2 |
| 95% довірчий інтервал (ДІ) | 1,1 | −1,0 | −0,5 | −1,1 | 0,2 | −0,3 | 0,1 |
| Зміна | 0,2—1,9 | −0,2 — −1,8 | −1,5 — 0,6 | −0,04 — −2,1 | −1,2 — 1,5 | −2,0 — 1,2 | −2,2 — 2,5 |
| Показник р | 0,015 | 0,017 | 0,41 | 0,04 | 0,82 | 0,65 | 0,90 |
| IIEF-5 | |||||||
| n, парні показники | 139 | 124 | 95 | 89 | 55 | 36 | 28 |
| Початковий показник | 16,0±8,6 | 15,7±8,6 | 14,9±8,6 | 15,3±8,6 | 14,4±8,6 | 16,0±9,0 | 156,0±9,1 |
| Період спостереження | 12,1±8,7 | 11,5±8,4 | 11,5±8,3 | 11,2±8,5 | 10,8±8,5 | 12,3±9,0 | 10,9±9,1 |
| 95% ДІ | −3,8 | −4,2 | −3,4 | −4,0 | −3,7 | −3,8 | −4,1 |
| Зміна | −4,9 — −2,7 | −5,4 — −3,1 | −4,7 — −2,0 | −5,5 — −2,6 | −5,6 — −1,7 | −6,9 — −0,6 | −7,6 — −0,5 |
| Показник р | <0,001 | <0,001 | <0,001 | <0,001 | <0,001 | 0,02 | 0,03 |
Спостерігалося помірне, але значне зниження сексуальної функції. Серед пацієнтів, які мали потенцію до лікування, 76% не мали жодних змін у потенції через 12 міс, 17% мали ерекцію, достатню для певної сексуальної активності, а 7% не мали ерекції, достатньої для будь-якої сексуальної активності.
Згідно з профілем безпеки, методика продемонструвала чудові показники. Протягом 12 міс після процедури загальний показник кількості ускладнень складав всього 2,6%. Частота ускладнень була найвищою на 3-му місяці після НОЕ і становила 1,8% у всій групі та знизилася до менш ніж 1% вже через 6 міс і залишалася такою ж до 48 міс після процедури. Серйозні ускладнення (≥3 ступеня) були рідкісними.
Найпоширенішими ускладненнями були підвищення рівня лейкоцитів у сечі (23,9%), епідидиміт (4,6%), тривала макрогематурія (3,7%), затримка сечі (2,8%), інфекції сечовивідних шляхів (1,8%).
Порівнюючи онкологічні результати, в європейському дослідженні значуща частота раку передміхурової залози становила 22,5% через 12 міс після НОЕ. Частота рецидивів у межах поля зору становила 9,8%.
Для інших видів фокальної терапії описано значну частоту рецидивів раку передміхурової залози в зоні лікування з медіаною 14,7% для високоінтенсивного сфокусованого ультразвуку (High-Intensity Focused Ultrasound — HIFU), 10% — для фотодинамічної терапії, 15% — для кріоабляції, 17% — для вогнищевої лазерної абляції, 20% — для радіочастотної абляції та 60% — для емболізації передміхурової артерії. Частота ускладнень для НОЕ становила 8,5%.
В одному дослідженні, в яке залучено 229 пацієнтів з медіаною спостереження 60 міс, безрецидивна виживаність становила 91% протягом 3 років та 84% протягом 5 років. Виживаність без метастазів становила 99,6%, а специфічна та загальна виживаність при раку передміхурової залози — 100%.
Нирково-клітинна карцинома
Використання НОЕ для лікування раку нирки проявило свою ефективність порівняно з іншими методами інвазивних втручань як у класичних, так і у складних випадках локалізацій пухлин, за наявності множинних пухлин нирок та при ураженнях єдиної нирки. Результати окремих клінічних досліджень вказують на те, що метод є безпечним, зумовлює прийнятний рівень ускладнень, хороші показники онкологічної та загальної виживаності й дозволяє зберегти оптимальну функцію нирок. Активне використання цієї методики в майбутньому дозволить вберегти багатьох пацієнтів від нефректомії та потреби гострого / хронічного гемодіалізу.
В одному з найбільш ранніх клінічних досліджень, яке проводилося на базі Університетської лікарні Сент-Джеймса, Беккет-стріт, Лідс LS9 7TF, Велика Британія [2], з 2015 до 2020 р., вибірка пацієнтів становила 26, загалом проліковано 30 пухлин за допомогою НОЕ. Ключовим повідомленням, яке автори хотіли донести, було те, що «необоротну електропорацію слід розглядати лише тоді, коли хірургічне втручання або термічна абляція під контролем зображення не є варіантом при невеликих розмірах пухлини». Тому критеріями включення були нирково-клітинна карцинома (НКК) cTa (<4 см) і відстань до життєво важливих структур, наприклад, сечоводу, товстої кишки, інших органів і судинних ніжок <1 мм. Одним із критеріїв виключення була наявність НКК cT1a, яку можна безпечно лікувати за допомогою класичних методів термічної абляції.
Середній розмір пухлини становив 2,5 см (1–4), а середній бал нефрометрії за шкалою R.E.N.A.L. — 6. За гістологічною будовою, визначеною за допомогою біопсії до лікування, НКК включала світлоклітинний (n=19; 63%), папілярний (n=5; 16%), еозинофільний (n=2; 7%) і хромофобний типи (n=2; 7%). Без гістологічного підтвердження були пацієнти з хворобою фон Гіппеля — Ліндау (n=2; 7%). Середня мінімальна відстань до життєво важливих структур становила 0,2 мм (±0,31), а до структур, що знаходилися в безпосередній близькості, належали товста кишка (n=11), сечовід (n=11) та судинна ніжка нирки (n=7). Середній інтрапроцедурний час НОЕ становив 72 хв (±24,2). Після лікування НОE всі пацієнти перебували під нічним спостереженням, середнім терміном перебуванням у лікарні було 2 доби. Середній відсоток зміни швидкості клубочкової фільтрації (ШКФ) після НОЕ — 13% (±16,3) серед усіх пацієнтів.
Початкового технічного успіху досягнуто після першої НОЕ у 22 з 30 пухлин (73%) при першій та подальших візуалізаціях.
7 з 8 випадків із залишковою хворобою були успішно проліковані за допомогою рятівної кріоабляції в середньому протягом 3 міс від першої НОЕ, досягнувши загального технічного успіху в 97%. 1 пацієнт не отримав подальшого лікування, оскільки помер від інсульту через 4 міс після НОЕ.
У решти 22 хворих зареєстровано загалом 7 ускладнень із загальною частотою 24%. Серед них були Clavien — Dindo I (n=6) та III ступенів (n=1). В одного пацієнта одразу після НОЕ розвинулася самообмежувальна перинефральна гематома, що було відмічено на комп’ютерній томографії (КТ) відразу після лікування. У 5 пацієнтів розвинулося >25% зниження ШКФ у найближчий період після НОЕ, що потребувало тривалішої госпіталізації та моніторингу функції нирок без необхідності гострого або хронічного гемодіалізу. Згодом у 3 пацієнтів ШКФ відновилася до вихідного рівня через 3–6 міс після процедури. Серйозне ускладнення (Clavien — Dindo III) відмічено в одного хворого, у якого розвинулася стриктура сечоводу, що потребувала тривалого стентування.
Після виконання статистичного аналізу не зафіксовано статистично достовірних даних щодо залежності первинного технічного успіху чи розвитку ускладнень від будь-яких факторів. Єдиним статистично достовірним результатом була залежність >25% зниження ШКФ від оцінки за шкалою R.E.N.A.L.
Контроль згідно з протоколом включає візуалізацію через 1 і 3 міс після лікування за допомогою МРТ і через 6 і 12 міс після терапії за допомогою КТ або МРТ (рис. 4) для пацієнтів з нирковою недостатністю або алергією на йодний контраст. Після цього всім пацієнтам щорічно проводиться КТ 3 зон для оцінки стану грудної клітки, черевної порожнини та малого таза протягом наступних 10 років.
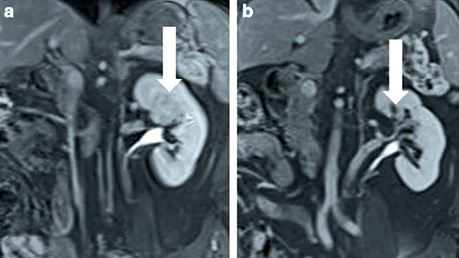
Рис. 4. МРТ, екскреторна фаза на 12 хв після контрастного підсилення візуалізувала центрально розташовану пухлину розміром 3,5 см, біопсійно підтверджений еозинофільний нирково-клітинний рак (НКР) G1 (вертикальна стрілка) до НОЕ (а) і повне зникнення пухлини (вертикальна стрілка) через 12 міс після НОE (b) [цит. за 4]
Середній період спостереження становив 37 міс (12–62). У цій когорті НОЕ не втрачено жодного пацієнта для подальшого спостереження, а також не зафіксовано випадків 30-денної смертності після лікування. Однак зареєстровано 3 випадки смерті: серцева подія (n=1), метастатичний НКР (n=1) і геморагічний інсульт (n=1). Серед них у 2 пацієнтів розвинувся локальний рецидив захворювання в зоні абляції через 16 і 24 міс відповідно.
2- та 3-річна виживаність без метастазів у пацієнтів, які отримували НОЕ, становила 87% (95% ДІ 65%; 96%). Показники 2- та 3-річної канцерспецифічної (cancer-specific survival — CSS) та загальної виживаності у пацієнтів, які отримували НОЕ, становили 96% (95% ДІ 73%; 99%) та 89% (95% ДІ 70%; 96%).
Дослідження, проведене Z. Wang та співавт. (2024) [3], наводить результати успішного лікування пацієнтів з пухлинними ураженнями єдиної нирки. Нефронозберігальна хірургія широко визнана як найкращий метод лікування солітарних пухлин нирок. Однак важливо зазначити, що хірургічна резекція може зашкодити ефективним нефронам нирок, особливо у випадку єдиної нирки. Вчені заявляють, що час інтраопераційної ішемії є одним з незалежних факторів, що впливає на функцію нирок пацієнтів після операції. Порівняно з хірургічною резекцією абляція дозволяє уникнути ішемії і післяопераційної реперфузійної травми, процедура проходить з мінімальною крововтратою. Перевагою НОЕ над іншими методами абляції є відсутність теплового пошкодження, тому метод абляції за допомогою НОЕ обраний з метою максимального збереження ефективної функції єдиної нирки.
Згідно з проведеним ретроспективним аналізом, з лютого 2017 до вересня 2020 р. 8 пацієнтам виконано КТ-керовану НОЕ з приводу 9 вогнищ ураження. Усім пацієнтам з набутою єдиною ниркою раніше було виконано контрлатеральну нефректомію через НКР. В усіх пацієнтів підтверджено наявність НКР за допомогою біопсії, і всі вони перебували в клінічній стадії T1aN0M0.
4 пацієнти (50,0%) мали різні ступені хронічної хвороби нирок до НОЕ, 6 (75,0%) — артеріальну гіпертензію, а 1 пацієнт мав хворобу фон Гіппеля — Ліндау. Середній діаметр пухлини у 8 пацієнтів становив 2,01±0,57 см (1,3–3,0). Середній бал за шкалою R.E.N.A.L. становив 6,67±1,58 (4–9), а середній бал за класифікацією PADUA становив 9,00±1,49 (6–11).
Автори повідомили, що технічного успіху в результаті лікування досягнуто у всіх 8 пацієнтів. Усі вони вижили і регулярно перебували під спостереженням (100,0%). Середній час спостереження становив 29,25±11,66 міс (14–48). Середня тривалість післяопераційного ліжко-дня становила 2,875±0,991 (2–4). У жодного з пацієнтів не розвинулося ускладнень за Clavien — Dindo ≥3 ступеня. Усі пацієнти мали післяопераційний біль за шкалою ≤2 балів. У 1 хворого після НОЕ виникла невелика самообмежувальна гематома навколо нирки, а у 2 осіб — транзиторна гематурія. Усі ускладнення усунуто протягом декількох днів виключно консервативним лікуванням.
Візуалізаційний контроль проводився в стандартні терміни за допомогою КТ / МРТ із внутрішньовенним підсиленням (рис. 5).
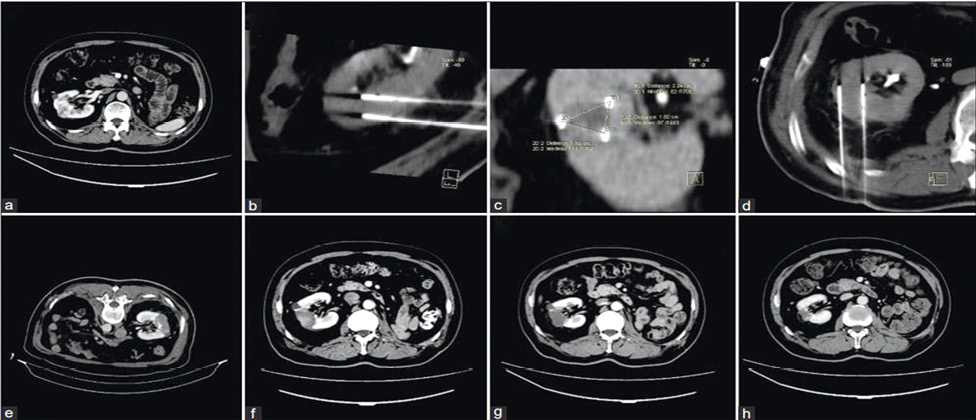
Рис. 5. На передопераційному КТ-зображенні виявлено пухлину в середньому сегменті правої нирки (а). Електроди були введені ззаду, а для точного позиціонування голок електродів використано зображення 3D-реконструкції (b–d). Повторні КТ-зображення одразу після НОЕ та через 1, 3, 12 міс не виявили жодного підсилення в ділянці абляції (e–h) [цит. за 5]
У одного пацієнта відмічалося підшкірне метастазування в голковий тракт, яке було видалено хірургічним шляхом під місцевим знеболенням (рис. 6). Ще в одного хворого через 6 міс після НОЕ виявлено часткове підсилення початкової зони абляції, що було розцінено як рецидив, з приводу чого виконано повторну НОЕ. Після цього не зафіксовано жодних ознак рецидиву на наступних візуалізаційних дослідженнях у жодного з пацієнтів.
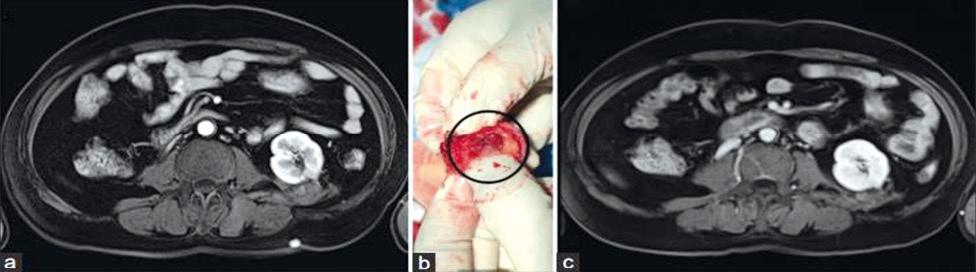
Рис. 6. Метастаз голкового тракту виявлено через 3 міс після НОЕ (а). Підшкірну резекцію виконано під місцевою анестезією (b). Повторне МРТ-підсилення через 6 міс після резекції свідчить про повне видалення метастазу без рецидиву (с) [цит. за 5]
Функція нирок оцінювалася, порівнюючи показник ШКФ, креатиніну в сироватці крові та гемоглобіну до лікування та під час останнього контролю (табл. 2). Результати не мали суттєвої різниці. Ба більше, порівняно з показниками функції нирок до операції в усіх пацієнтів не виникло достовірного підвищення рівня креатиніну в сироватці крові та достовірного зниження ШКФ.
| Візуальна аналогова шкала (1 год після НОЕ) | Сироватковий креатинін до операції, мкмоль/л |
Сироватковий креатинін визначений при останньому спостереженні, мкмоль/л |
Розрахункова ШКФ до операції, мл/хв/1,73 м2 | Розрахункова ШКФ визначена при останньому спостереженні | Рівень гемоглобіну до операції, г/л |
Рівень гемоглобіну, визначений при останньому спостереженні, г/л | Середній показник |
||
| сироваткового креатиніну | розрахункової ШКФ | рівня гемоглобіну | |||||||
| 0 | 69 | 83 | 96,035 | 86,057 | 118 | 112 | 14 | −9,978 | −6 |
| 0 | 58 | 71 | 105,337 | 96,936 | 123 | 131 | 13 | −8,401 | 8 |
| 2 | 136 | 147 | 48,72 | 44,348 | 119 | 117 | 11 | −4,372 | −2 |
| 0 | 84 | 79 | 72,545 | 78,133 | 133 | 110 | −5 | 5,588 | −23 |
| 1 | 93 | 102 | 54,576 | 48,809 | 129 | 141 | 9 | −5,767 | 12 |
| 0 | 74 | 69 | 67,536 | 73,497 | 109 | 118 | −5 | 5,961 | 9 |
| 0 | 142 | 131 | 36,609 | 40,358 | 147 | 135 | −11 | 3,749 | −12 |
| 0 | 116 | 152 | 53,52 | 38,601 | 119 | 119 | 36 | −14,919 | 0 |
До недоліків цього дослідження, загальних для переважної більшості, можна віднести малу вибірку пацієнтів, відсутність контрольної групи, контрольного гістологічного підтвердження та обмежений період спостереження.
Гепатоцелюлярна карцинома та вторинні вогнища печінки
Абляція за допомогою НОЕ використовується як метод лікування злоякісних пухлин печінки, розташованих поблизу великих кровоносних судин та/або жовчних проток, де методи термоабляції пов’язані з ризиком ускладнень та ефектом нагрівання.
У дослідженні, опублікованому авторами з Маямі, Флорида [6], проаналізовано еволюцію НОЕ, а також її безпеку та ефективність у контексті інших абляційних методів лікування злоякісних новоутворень печінки. Згідно з описом цього дослідження, зазвичай доставляється 90 високовольтних (1500–3000 В) імпульсів постійного струму (25–45 А) між парою монополярних або одним біполярним електродом (зі зміною лікувальних настанов кількість імпульсів для успішного лікування між парою монополярних електродів була зменшена з 90 до 70). Напруга встановлюється залежно від відстані між кожною парою електродів, з метою генерувати принаймні 1000 В між електродами. Генератор запрограмований на зупинку подачі енергії та перезарядку, якщо сила струму перевищує 48 А. Електроди розміщуються перкутанно під контролем візуалізації (КТ або ультразвукового дослідження) з максимальною відстанню між електродами 2,2 см (рис. 7).
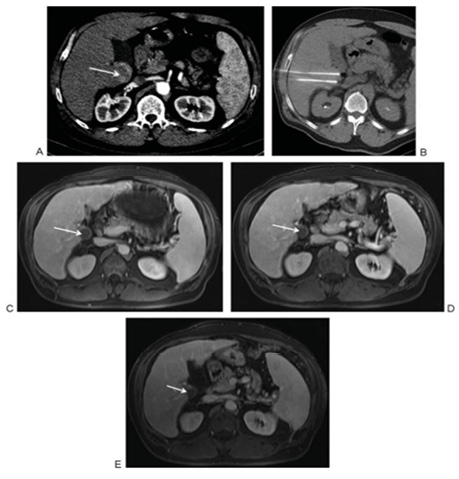
Рис. 7. Процедура НОЕ у пацієнта з біопсійно підтвердженою гепатоцелюлярною карциномою: a) — контрастно підсилене аксіальне КТ-сканування, що проявляє ураження каудальної частки печінки до процедури НОЕ (стрілка); b) — аксіальне КТ-сканування під час процедури НОЕ, що візуалізує 2 монополярні електроди в ураженій частці печінки; c–e) — магнітно-резонансне сканування через 6, 11 та 14 міс після процедури НОЕ, що свідчить про відсутність залишкової або рецидивної пухлини (стрілка) [цит. за 6]
У систематичному огляді, опублікованому в журналі Cancers (2023) [7], проаналізовано інформацію про використання НОЕ у пацієнтів з метастазами колоректального раку в печінку та наведено дані про результати, пов’язані з процедурою та перебігом хвороби. Пошук виявив 647 унікальних статей, після відсіву залишилося 8. Вони були оцінені на ризик упередженості за методологічним індексом для нерандомізованих досліджень (критерії MINORS) та описані відповідно до настанови «Синтез без метааналізу» (Synthesis Without Meta-analysis — SWiM).
Лікування метастазів у печінку від колоректального раку методом НОЕ отримали 180 пацієнтів. Медіанний поперечний діаметр пухлин, оброблених НОЕ, становив <3 см. У 94 (52%) випадках пухлини були розташовані поруч із великими судинами печінкового притоку / відтоку або порожнистою веною. Процедуру проводили під загальною анестезією із синхронізацією із серцевим циклом та використанням КТ або ультразвуку для локалізації ураження. Відстань між електродами при всіх абляціях була <3,2 см. Серед 180 осіб зафіксовано 2 (1,1%) летальні випадки, пов’язані з процедурою. Виявлено 1 (0,5%) післяопераційну кровотечу, що потребувала лапаротомії, 1 (0,5%) витік жовчі, 5 (2,8%) випадків післяпроцедурних стриктур жовчних проток і жодного випадку печінкової недостатності після НОЕ.
Цей систематичний огляд свідчить, що метод НОЕ при метастазах колоректального раку в печінку можна виконати з низьким рівнем ускладнень та смертності, пов’язаних із процедурою. Потрібні додаткові проспективні дослідження, щоб оцінити роль НОЕ серед методів лікування пацієнтів з метастазами в печінку від колоректального раку.
Автори також вказують, що для оцінки ролі НОЕ у лікуванні пацієнтів із метастазами в печінку від колоректального раку необхідні подальші ретельні дослідження з належним описом поширеності захворювання та попередніх методів лікування.
ПЕРСПЕКТИВНІ НАПРЯМКИ КОМПЛЕКСНОЇ ТЕРАПІЇ
Упродовж останніх років НОЕ активно модифікується з метою підвищення ефективності абляції, зменшення кількості резидуальних та рецидивних пухлин і посилення імунної відповіді. Найперспективнішими напрямками терапії вважаються електролітична НОЕ (E-IRE), електрохімієтерапія, а також поєднання НОЕ з променевою терапією (Radiation Therapy and IRreversible Electroporation — RTIRE).
Електролітична НОЕ
Огляди останніх клінічних досліджень з лікування раку за допомогою НОE свідчать, що відсоток успішного лікування знижується зі збільшенням розміру пухлини. Однією з важливих причин рецидиву пухлини in situ може бути неповна абляція після лікування за допомогою НОE.
Загалом зона електропорації (включно із оборотною та необоротною) залежить від локального електричного поля в тканині-мішені. Електричні імпульси, що подаються парою голкових електродів, можуть генерувати електричне поле між самою парою електродів і навколо них у тканині. Величина електричного поля зменшується з віддаленням від електродів [8, 11].
Стандартна НОЕ створює зону оборотної електропорації на периферії, де клітини потенційно відновлюють свою структуру. Щоб збільшити площу абляції запропоновано електролітичне посилення — подачу низькочастотного постійного струму між імпульсами, що сприяє:
- електрофоретичному переміщенню іонів електролізу в зону оборотної електропорації;
- переходу зони оборотної електропорації в необоротну;
- поступовому збільшенню площі некрозу без підвищення напруги.
Експерименти на моделях (зокрема тканинах картоплі та тварин) допомогли виявити, що зона ураження при E-НОE зростає до 30–40% порівняно зі стандартним протоколом при однакових імпульсах.
Електрохімієтерапія
Електрохімієтерапія поєднує оборотну електропорацію з введенням хімієтерапевтичних засобів (цисплатину, блеоміцину), які після електропорації легко проникають у клітини [9]. У варіації з оборотною електропорацією:
- цитостатики вводяться безпосередньо перед подачею імпульсів;
- зона абляції значно розширюється через цитотоксичний ефект у зоні оборотної електропорації;
- встановлено підвищену інфільтрацію Т-клітин у ділянці абляції та зменшення ангіогенезу.
Цей підхід відкриває перспективу лікування більших уражень при збереженні низької енергії імпульсів.
RTIRE
Ідея комбінованого підходу полягає в тому, що НОЕ підвищує оксигенацію пухлини та проникність клітинної мембрани, тим самим сенсибілізуючи клітини до дії іонізуючого випромінювання.
У дослідженні M. Diven та співавт. (2024) у пацієнтів з раком передміхурової залози виявлено, що комбінація НОЕ зі стереотаксичною променевою терапією тіла (Stereotactic body radiation therapy — SBRT) [10]:
- знижує необхідну дозу опромінення на 30–40%;
- посилює контроль над вторинними пухлинами;
- не підвищує частоту токсичних ускладнень ≥II ступеня.
Проведення НОЕ до радіотерапії дозволяє посилити абскопальний ефект імунної відповіді подібно до ефекту вакцинації пухлиною in situ.
Висновки. На тлі постійного пошуку методів, здатних забезпечити локальний контроль пухлинного процесу без значного пошкодження навколишніх тканин, НОЕ привертає особливу увагу як технологія з принципово іншим механізмом впливу. На відміну від більшості абляційних методик, її дія не пов’язана з термічним пошкодженням, що дозволяє зберігати структурну цілісність особливо важливих навколишніх елементів навіть у межах зони втручання.
Отримані результати вказують на значну користь методу в ситуаціях, де стандартні підходи пов’язані з високим ризиком втрати функції органа або значною операційною травмою. Тому поєднання вибірковості впливу НОЕ з відносно низьким рівнем системної токсичності визначає інтерес до цього методу як до потенційного інструменту органозберігального лікування.
Використання НОЕ при раку нирки та передміхурової залози дозволяє досягати онкологічного контролю, зіставного з хірургічним лікуванням, за значно меншого впливу на функціональні результати, зокрема забезпечення континенції, збереження статевої функції, ефективної паренхіми та органа в цілому. У пацієнтів з локалізованими формами пухлин НОЕ сприяє високій технічній успішності (>90%), низькому рівню ускладнень та належній переносимості.
Проте більшість наявних на сьогодні протоколів клінічних досліджень мають короткі терміни спостереження, що не дозволяє однозначно оцінити довгострокові онкологічні результати та обмежує можливість широкого впровадження методу у стандарти лікування. Сюди ж можна додати гетерогенність популяцій, переважно малі вибірки пацієнтів, відсутність уніфікованих критеріїв відбору пацієнтів, контрольних груп, єдиного алгоритму контролю якості проведеного втручання. Це ускладнює формування чітких клінічних рекомендацій і визначає необхідність подальшої стандартизації методики та накопичення доказової бази.
Важливим є також те, що ефективність методу значною мірою визначається технічними аспектами виконання процедури, включно з точністю позиціонування електродів та плануванням зони впливу. Це підкреслює залежність результатів не лише від біології пухлини, а й рівня технологічного забезпечення та досвіду оператора.
У зв’язку з цим НОЕ на цьому етапі доцільно розглядати як компонент клінічних досліджень або опцію для індивідуалізованого лікування в окремої когорти ретельно відібраних пацієнтів на базі спеціалізованих центрів.
Окремої уваги заслуговує питання доступності технології. З огляду на високу вартість оригінального обладнання перспективним напрямком буде розробка вітчизняних аналогових апаратів для забезпечення НОЕ. Це може сприяти ширшому впровадженню методики на теренах України, однак потребує ретельної технічної валідації, стандартизації параметрів впливу та підтвердження безпечності й ефективності порівняно з наявними системами.
Окремим напрямком подальшого розвитку є вивчення ролі НОЕ у послідовних та комбінованих схемах лікування, зокрема у якості доповнення до системної терапії. Такий підхід може змінити уявлення про локальні методи впливу, трансформуючи їх із ізольованих втручань у частину комплексного онкологічного менеджменту.
Тому найближчими викликами є:
- стандартизація показань;
- розширення доступу до технології;
- проведення багатоцентрових клінічних досліджень;
- поєднання з хіміє-, імуно- та променевою терапією.
З урахуванням наявних клінічних результатів і технологічних перспектив НОЕ може посісти важливе місце в сучасній онкології як інструмент персоналізованого лікування, особливо в межах органозберігальних стратегій та комбінованих терапевтичних підходів.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
1. Мовчан, В. І., Стаховський, Е. О., Войленко, О. А., Вітрук, Ю. В., Стаховський, О. Е., Кононенко, О. А., & Романенко, О. В. (2025). Необоротна електропорація як альтернативний метод лікування в онкології: біофізичні та молекулярні механізми, технічні аспекти та сучасні можливості методу (огляд наукової літератури). Клінічна онкологія, 3(59), 185–191. doi.org/10.32471/clinicaloncology.2663-466X.34868. [Movchan, V. I., Stakhovskyi, E. O., Voilenko, O. A., Vitruk, Y. V., Stakhovskyi, O. E., Kononenko, O. A., & Romanenko, O. V. (2025). Neoborotna elektroporatsiya yak alʹternatyvnyy metod likuvannya v onkolohiyi: biofizychni ta molekulyarni mekhanizmy, tekhnichni aspekty ta suchasni mozhlyvosti metodu (ohlyad naukovoyi literatury). Clinical Oncology, 3(59), 185–191. Ukrainian].
2. Wah, T. M., Lenton, J., Smith, J., Bassett, P., Jagdev, S., Ralph, C., … Cartledge, J. (2021). Irreversible electroporation (IRE) in renal cell carcinoma (RCC): a mid-term clinical experience. European Radiology, 31, 7491–7499. doi.org/10.1007/s00330-021-07846-5.
3. Wang, Z., Huang, W., Liu, J., Liu, Q., Wang, Q., Wu, Z., … Wang, Z. (2024). Percutaneous irreversible electroporation of renal cell carcinomas in an acquired solitary kidney: A primary study. Journal of Cancer Research and Therapeutics, 20(7), 1997–2003. doi.org/10.4103/jcrt.jcrt_16_24.
4. Gielchinsky, I., & Lev-Cohain, N. (2023). Focal irreversible electroporation for localized prostate cancer — oncological and safety outcomes using mpMRI and transperineal biopsy follow-up. Research and Reports in Urology, 15, 27–35. doi.org/10.2147/RRU.S393243.
5. Zhang, K., Stricker, P., Löhr, M., Stehling, M., Suberville, M., Cussenot, O., … de la Rosette, J. (2024). A multi-center international study to evaluate the safety, functional and oncological outcomes of irreversible electroporation for the ablation of prostate cancer. Prostate Cancer and Prostatic Diseases, 27, 525–530. doi.org/10.1038/s41391-023-00783-y.
6. Narayanan, G., Froud, T., Suthar, R., & Barbery, K. (2013). Irreversible electroporation of hepatic malignancy. Seminars in Interventional Radiology, 30(1), 67–73. doi.org/10.1055/s-0033-1333655.
7. Spiers, H. V. M., Lancellotti, F., de Liguori Carino, N., Pandanaboyana, S., Frampton, A. E., Jegatheeswaran, S., … Siriwardena, A. K. (2023). Irreversible Electroporation for Liver Metastases from Colorectal Cancer: A Systematic Review. Cancers, 15(9), 2428. doi.org/10.3390/cancers15092428.
8. Lv, Y., Liu, H., Feng, Z., Zhang, J., Chen, G., & Yao, C. (2022). The enlargement of ablation area by electrolytic irreversible electroporation (E-IRE) using pulsed field with bias DC field. Annals of Biomedical Engineering, 50(12), 1964–1973. doi.org/10.1007/s10439-022-03017-9.
9. Lindelauf, K. H. K., Baragona, M., Lemainque, T., Maessen, R. T. H., & Ritter, A. (2024). Electrochemotherapy and Calcium Electroporation on Hepatocellular Carcinoma Cells: An In-Vitro Investigation. Cardiovasc Intervent Radiol, 47, 1384–1391 (2024). doi.org/10.1007/s00270-024-03847-1.
10. Diven, M., Ballman, K., Marciscano, A., Barbieri, C., Piscopo, J., Wang, S., … McClure, T. (2024). Radiation therapy and IRreversible electroporation for intermediate risk prostate cancer (RTIRE). BMC Urology, 24, 151. doi.org/10.1186/s12894-024-01506-8.
11. Xu, C., & Zhang, Y. (2021). Multi Physical Field Simulation of Irreversible Electroporation. Journal of Physics: Conference Series, 1861, 012058. doi: 10.1007/978-3-319-55113-5_3.
Адреса для листування:
Мовчан Валентина Іванівна
03022, Київ, вул. Здановської Юлії, 33/43
Державне некомерційне підприємство «Національний інститут раку»
E-mail: valyalimma@gmail.com
Correspondence:
Valentyna Movchan
33/43 Yulii Zdanovskoi str., Kyiv, 03022
Nonprofit Organization National Cancer Institute
E-mail: valyalimma@gmail.com














Leave a comment