Хірургічне видалення пухлинних тромбів нижньої порожнистої вени без штучного кровообігу: що робити, якщо piggyback-мобілізація печінки неможлива?
Резюме. У статті представлено результати анатомічного дослідження можливості виконання нового хірургічного маневру — формування поперечного тунелю під вічками головних печінкових вен при видаленні пухлинних тромбів нижньої порожнистої вени. Параметри цього хірургічного підходу порівнювали з результатами рiggyback-мобілізації печінки. Результати нашої роботи продемонстрували можливість формування поперечного тунелю під вічками головних печінкових вен у 80% пацієнтів. Такий маневр має подібний з рiggyback-мобілізацією печінки ступінь ризику. Для визначення його ефективності необхідно подальше клінічне дослідження.
Резюме. В статье представлены результаты анатомического исследования возможности выполнения нового хирургического маневра — формирования поперечного тоннеля под устьями главных печеночных вен при удалении опухолевых тромбов нижней полой вены. Параметры данного хирургического подхода сравнивали с результатами рiggyback-мобилизации печени. Результаты нашей работы продемонстрировали возможность формирования поперечного тоннеля под устьями главных печеночных вен у 80% пациентов. Такой маневр имеет сходную с рiggyback-мобилизацией печени степень риска. Для определения его эффективности необходимо дальнейшее клиническое исследование.
Введение
Отчетливые недостатки удаления высоких опухолевых тромбов с помощью баллонных катетеров или технологий искусственного кровообращения привели к разработке альтернативных методов, позволяющих полностью контролировать подпеченочный, ретропеченочный и интраперикардиальный отделы нижней полой вены (НПВ) [1, 2]. Наиболее важным аспектом этого подхода является возможность наружного пальцевого смещения верхушки тромба ниже диафрагмы [3, 4]. Однако при слабом развитии кавальных коллатералей наложение зажима на НПВ выше устьев главных печеночных вен может привести к серьезным гемодинамическим сдвигам. Поэтому основной задачей хирурга в данной ситуации является дальнейшее смещение тромба вниз и наложение зажима на НПВ ниже устьев главных печеночных вен [5, 6] (рис. 1). Этот маневр позволяет сохранить печеночный кровоток, на который приходится около 25% притока крови к НПВ. Основным условием осуществления данного этапа операции является проведение мобилизации печени в классическом и piggyback вариантах [2].
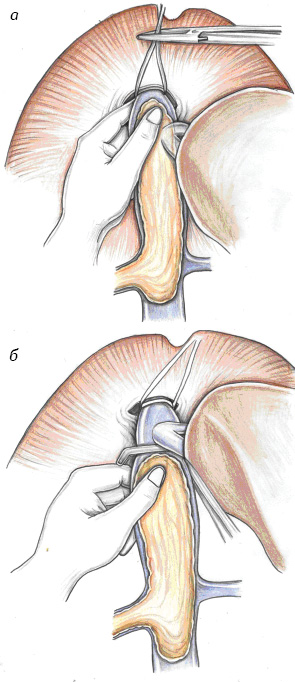
При классическом варианте печень мобилизуют en bloc с НПВ. Это требует лигирования и пересечения правых поясничных, адренальных и нижнедиафрагмальных вен и полного отделения ретропеченочного отдела НПВ от задней брюшной стенки. Вариант piggyback характеризуется максимальным отделением передней поверхности НПВ от печени (сохраняются только главные печеночные вены) путем пересечения малых печеночных вен, дренирующих хвостатую долю. Тщательно мобилизуются конечные участки и устья главных печеночных вен.
Для облегчения мобилизации ретропеченочного отдела НПВ J. Belghiti и соавторы предложили маневр, заключающийся в приподнимании печени (liver-hanging maneuver) [7]. Его осуществляют путем проведения ленты между передней поверхностью НПВ и задней поверхностью печеночной паренхимы [8]. Приподнимание печени с помощью ленты обеспечивает лучший обзор всей надпеченочной области и значительно упрощает выполнение манипуляций на печеночных венах и интраперикардиальной части НПВ, особенно в случаях выраженной гепатомегалии.
Но необходимо учитывать, что из-за проблем, связанных с венозной анатомией, piggyback-мобилизация печени возможна лишь в 80–92% случаев [2]. Главные печеночные вены и вены хвостатой доли печени в ряде наблюдений имеют очень короткую внепеченочную часть, весьма тонкие стенки и вариабельную локализацию. К тому же у некоторых пациентов обнаруживают несколько десятков вен, открывающихся в ретропеченочном отделе НПВ. Все вышеперечисленное предрасполагает к их травматизации, что в свою очередь может привести к массивному кровотечению. Ятрогенное повреждение коротких печеночных вен — наиболее неприятное осложнение этой процедуры, которое возникает примерно у 4–6% пациентов [8].
С нашей точки зрения, выполнение piggyback-мобилизации печени требуется далеко не всегда. Это прежде всего касается ситуаций, когда печень охватывает ретропеченочный отдел полой вены менее чем на ½ длины ее окружности. При этом для низведения тромба вниз вполне достаточно выполнить мобилизацию печени в классическом варианте и освободить заднюю поверхность полой вены. Учитывая геометрические особенности ретропеченочной НПВ и главных печеночных вен, а также данные визуальных исследований, мы предположили, что непосредственно под устьями главных печеночных вен существует аваскулярная зона шириной около 1,0 см, через которую может быть проведен сосудистый зажим без выполнения piggyback-мобилизации печени (рис. 2). Таким образом, рука хирурга, заведенная выше верхушки тромба и охватывающая полую вену сзади и сбоку, а не циркулярно, может легко сместить тромб ниже устьев главных печеночных вен. При этом зажим над верхушкой тромба может быть проведен через поперечный тоннель непосредственно под устьями главных печеночных вен (рис. 3).
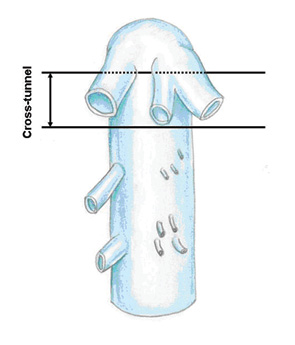
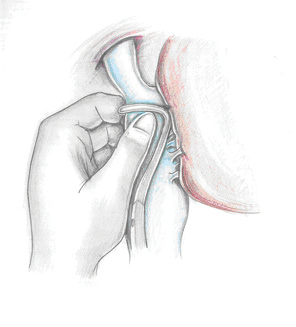
Для подтверждения этого предположения мы провели анатомическое исследование ретропеченочного отдела НПВ в плане оценки выполнимости и рискованности двух вариантов хирургических подходов к данному сегменту НПВ: piggyback-мобилизации печени и формирования поперечного тоннеля под устьями главных печеночных вен.
Объект и методы исследования
Материалом анатомического исследования служили 35 трупов (время после смерти не более 48 ч). Аутопсию выполняли с июня по сентябрь 2012 г. на базе патологоанатомических отделений больницы № 8 и КУОЗ «Областной клинический центр урологии и нефрологии им. В.И. Шаповала». Возраст умерших (18 мужчин и 17 женщин) варьировал от 42 до 85 лет и составлял в среднем 69,3 года, их средний рост не превышал 168 см, а масса тела — 82 кг.
Для изучения особенностей ретропеченочной НПВ и ее притоков использовали следующую методику. После изъятия органокомплекса острым и тупым путем выделяли заднюю поверхность НПВ на всем протяжении. Затем переворачивали органокомплекс вентральной стороной кверху и выполняли мобилизацию печени по классической методике (пересечение серповидной, треугольных и коронарных связок), что позволяло выделить супрагепатический поддиафрагмальный отдел НПВ с устьями главных печеночных вен. Вслед за этим пытались тупым путем создать поперечный тоннель шириной около 1,0 см непосредственно ниже устьев главных печеночных вен без проведения piggyback-мобилизации печени. При этом оценивали возможное повреждение печени и сосудов.
После этого полую вену продольно вскрывали от бифуркации до ретропеченочного сегмента НПВ. Разрез проводили по левой боковой поверхности вены в направлении на 9 часов условного циферблата для максимального сохранения целостности задней стенки НПВ. На уровне ретропеченочного отдела НПВ рассекали продольно по средней линии. После завершения разреза заднюю стенку НПВ отворачивали наружу, что давало возможность исследовать устья основных притоков НПВ, расположенных как по передней, так и по задней поверхности сосуда. Изучалась длина и диаметр каждого сегмента НПВ, а также размеры устья каждого из венозных притоков.
Для топографической фиксации устьев печеночных вен ретропеченочный сегмент НПВ условно разделяли на 12 участков, которые наносили на специальную диаграмму. Главные печеночные вены характеризовали как верхнюю правую, среднюю и левую. Другие, более мелкие венозные сосуды, дренирующиеся в области задней поверхности печени (дорзальные печеночные вены), классифицировали в соответствии c L. De Cecchis и соавторами [9]. При диаметре устья более 4 мм выделяли правую нижнюю и правую среднюю печеночную вену [10]. Отдельно рассматривали вены хвостатой доли печени и другие мелкие венозные притоки. Учитывая локализацию, размеры и количество венозных устьев, изучали возможность и риск выполнения piggyback-мобилизации печени. Все этапы анатомического исследования были сфотографированы.
Возможность выполнения piggyback-мобилизации печени и формирования тоннеля под устьями главных печеночных вен оценивали с помощью шкалы: легко (100 баллов), сложно (50 баллов), невозможно (0 баллов). В отношении риска вмешательство рассматривали как безопасное (100 баллов), рискованное (50 баллов), приведшее к травме сосудов или паренхимы печени (0 баллов).
Результаты и их обсуждение
Основные результаты исследования представлены в табл. 1–3. Средняя длина ретропеченочного отдела НПВ составляла 85,8 мм (70–130 мм), диаметр — 31,1 мм (25–40 мм). Ретропеченочная НПВ была полностью окружена печенью в 1 (2,9%) случае, на ½ длины окружности — в 17 (48,5%), на ⅔ — в 16 (45,7%) и на ⅓ — только в 1 (2,9%) наблюдении.
Таблица 1. Показатели выполнимости piggyback-мобилизации печени и формирования тоннеля под устьями главных печеночных вен
| Выполнимость | Легко | Сложно | Невозможно | Средний балл |
| Piggyback-мобилизация | 7 (20%) | 24 (68,6%) | 4 (11,4%) | 54,3 |
| Формирование тоннеля под главными печеночными венами | 11 (31,4%) | 17 (48,6%) | 7 (20%) | 55,7 |
Таблица 2. Показатели риска piggyback-мобилизации печени и формирования тоннеля под устьями главных печеночных вен
| Безопасность | Безопасно | Рискованно | Травма | Средний балл |
| Piggyback-мобилизация | 1 (2,9%) | 29 (82,8%) | 5 (14,3%) | 44,3 |
| Формирование тоннеля под главными печеночными венами | 0 | 25 (71,4%) | 10 (28,6%) | 35,7 |
Таблица 3. Показатели сочетания параметров выполнимости и безопасности piggyback-мобилизации печени и формирования тоннеля под устьями главных печеночных вен
| Piggyback-мобилизация | Формирование тоннеля под главными печеночными венами | |
| Легко + безопасно | 1 (2,9%) | 0 |
| Легко + рискованно | 6 (17,1%) | 11 (31,5%) |
| Легко + травма | 0 | 0 |
| Сложно + безопасно | 0 | 0 |
| Сложно + рискованно | 22 (62,9%) | 14 (40%) |
| Сложно + травма | 2 (5,7%) | 3(8,5%) |
| Невозможно + рискованно | 1 (2,9) | 0 |
| Невозможно + травма | 3 (8,5%) | 7 (20%) |
| Всего | 35 (100%) | 35 (100%) |
Количество устьев всех видов печеночных вен варьировало от 4 до 16 и составляло в среднем 7,6. Среднее количество устьев дорзальных вен печени диаметром3 мм — 2,5 (0–5).
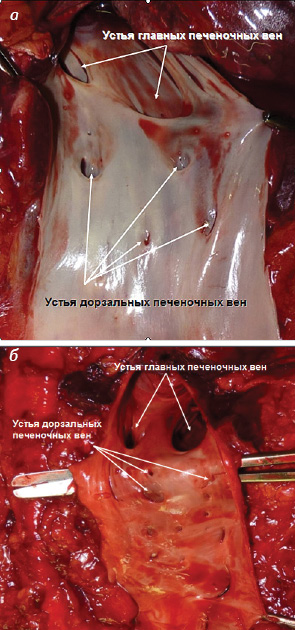
Рiggyback-мобилизация печени признана невозможной в 4 (11,4%) случаях, у 24 (68,6%) пациентов ее выполнение было сложным. В отношении тоннеля под устьями главных печеночных вен нужно отметить, что его формирование было невозможным в 7 (20%) случаях. Тем не менее у 11 (31,4%) больных создание тоннеля признано легким (рис. 4).
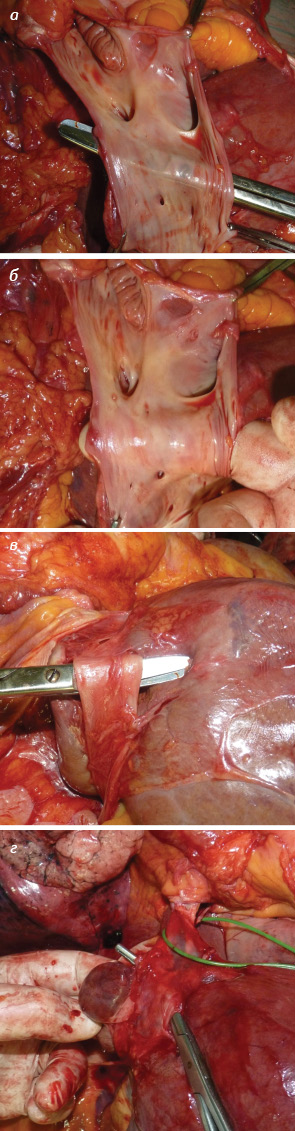
Повреждение паренхимы печени, печеночных вен или НПВ отмечено в 14,3% случаев при использовании рiggyback-мобилизации печени, тогда как формирование тоннеля под устьями печеночных вен приводило к подобным проблемам у 28,6% пациентов (рис. 5).
Риск тем не менее был несколько выше при piggyback-мобилизации печени (82,8% против 71,4%). Сочетание параметров «легко + рискованно» чаще отмечено при формировании тоннеля (31,5% по сравнению с 17,1%), тогда как «сложно + рискованно» — гораздо чаще при выполнении рiggyback-мобилизации печени (62,9% по сравнению с 40,0%). Интересно, что невозможность как рiggyback-мобилизации, так и формирования тоннеля зафиксирована только у 1 пациента. Выполнимость рiggyback-мобилизации не коррелировала с возможностью создания тоннеля.
Результаты данного исследования продемонстрировали, что выполнение piggyback-мобилизации печени является возможным примерно в 90% случаев, тогда как формирование тоннеля под устьями главных печеночных вен — в 80%. Интересно, что оба варианта доступа к ретропеченочной части НПВ были невыполнимы только у 1 (2,9%) пациента. Поэтому мы считаем, что какие-либо проблемы с проведением одного из доступов могут быть компенсированы использованием второго подхода.
Оба доступа продемонстрировали достаточно высокие показатели риска (82,8 и 71,4%). Однако сочетание параметров «легко + рискованно» в большем проценте случаев отмечали при формировании тоннеля, тогда как параметры «сложно + рискованно» гораздо чаще констатировали при выполнении piggyback-мобилизации печени. Безусловно, одним из недостатков нашего исследования был определенный субъективизм оценки результатов, несмотря на то что мы попытались унифицировать этот показатель за счет создания шкалы выполнимости и риска этапов операции. Наиболее весомым фактором, влияющим на оценку этих параметров, является опыт печеночной хирургии и знание анатомии хирургом, который выполняет удаление опухолевого тромба.
Наша работа представляет собой моделирование доступа к ретропеченочному отделу НПВ путем создания тоннеля под устьями главных печеночных вен во время анатомического исследования. Для более детальной и объективной оценки этого подхода необходимо дальнейшее клиническое исследование. Несомненно, интраоперационная ультрасонография печени может значительно облегчить формирование тоннеля под устьями главных печеночных вен и снизить уровень риска.
Заключение
Результаты нашего анатомического исследования продемонстрировали возможность выполнения нового маневра во время венокавотромбэктомии путем создания поперечного тоннеля под устьями главных печеночных вен у 80% пациентов. Данный подход имеет сходную степень риска с рiggyback-мобилизацией печени. Для определения эффективности этого подхода необходимо дальнейшее клиническое исследование.
Список использованной литературы
1. Давыдов М.И., Матвеев В.Б. (2005) Хирургическое лечение больных раком почки с опухолевым тромбозом почечной и нижней полой вены. Онкоурология, 2: 8–15.
2. Переверзев А.С. (1997) Хирургия опухолей почки и верхних мочевых путей. Lora Medpharm, Харьков, 392 с.
3. Vaidya A., Ciancio G., Soloway M. (2003) Surgical techniques for treating a renal neoplasm invading the inferior vena cava. J. Urol., 169(2): 435–444.
4. Щукин Д.В., Илюхин Ю.А. (2007) Хирургия опухолевых тромбов нижней полой вены при раке почки. Белгород, 196 с.
5. Ciancio G., Hawke C., Soloway M. (2000) The use of liver transplant technique to aid in the surgical management of urological tumor. J. Urol., 164: 655–672.
6. Ciancio G., Vaidya A., Savoie M., Soloway M. (2002) Management of renal cell carcinoma with level 111 thrombus in the inferior vena cava. J. Urol., 168: 1374–1377.
7. Belghiti J., Guevara O.A., Noun R. et al. (2001) Liver hanging maneuver: a safe approach to right hepatectomy without liver mobilization. J. Am. Coll. Surg., 193: 109.
8. Ettorre G.M., Vennarecci G., Santoro R. et al. (2003) Modified liver hanging maneuver during orthotopic liver transplantation with inferior vena cava preservation. Transplantation, 75(2): 247–249.
9. De Cecchis L., Hribernik M., Ravnik D., Gadzijev E.M. (2000) Anatomical variations in the pattern of
the right hepatic veins: possibilities for type classification. J. Anat., 197, Pt. 3: 487–493.
10. Birincioglu I., Topaloglu S., Turan N. et al. (2011) Detailed dissection of hepato-caval junction and suprarenal inferior vena cava. Hepatogastroenterology, 58(106): 311–317.














Leave a comment