Лікування постпневмонектомічних бронхіальних нориць у торакальній онкохірургії: огляд літератури та власний досвід
Резюме. У статті наведено огляд сучасних методів лікування та профілактики бронхіальних нориць, які виникли після пульмонектомії з лімфодисекцією, виконаної з приводу раку легені. Описано раніше застосовувані методи оперативного лікування та консервативні методи терапії пацієнтів із цим ускладненням. Проведено порівняльний аналіз ефективності консервативних та сучасних оперативних методик лікування цієї категорії хворих. Наведено алгоритм терапії пацієнтів із постпневмонектомічною бронхіальною норицею залежно від боку оперативного втручання, строків виникнення ускладнення та загальносоматичного стану пацієнтів.
Резюме. В статье приведен обзор современных методов лечения и профилактики бронхиальных свищей, возникших после пульмонэктомии с лимфодиссекцией, выполненной по поводу рака легкого. Описаны ранее применяемые способы оперативного лечения и консервативные методы терапии пациентов с этим осложнением. Проведен сравнительный анализ эффективности консервативных и современных оперативных методов лечения этой категории больных. Приведен алгоритм терапии при постпневмонэктомических бронхиальных свищах в зависимости от стороны проведения операции, сроков возникновения осложнения и общесоматического состояния пациентов.
 Хирургический метод лечения пациентов с немелкоклеточным раком легкого является основным при І и ІІ стадии заболевания и одним из ключевых этапов комбинированной терапии при ІІІ (преимущественно ІІІа) стадии патологического процесса.
Хирургический метод лечения пациентов с немелкоклеточным раком легкого является основным при І и ІІ стадии заболевания и одним из ключевых этапов комбинированной терапии при ІІІ (преимущественно ІІІа) стадии патологического процесса.
Удельный вес пневмонэктомий составляет около 50–60% всех радикальных операций, выполняемых при раке легкого (Ганул В.Л., 2008) [7]. В настоящее время стандартными радикальными операциями у больных раком легкого являются лоб- и пневмонэктомии с лимфодиссекцией до D2. Подобные операции почти в полтора раза улучшают отдаленные онкологические результаты лечения [1]. Для правого легкого в этот объем входят: пульмональные, бронхопульмональные, правые корневые, правые трахеобронхиальные, бифуркационные, правые паратрахеальные, претрахеальные, параэзофагеальные лимфоузлы и лимфоузлы правой легочной связки; для левого легкого — левые пульмональные, левые бронхопульмональные, параэзофагеальные, бифуркационные, субаортальные, левые трахеобронхиальные, претрахеальные лимфоузлы, лимфоузлы левой легочной связки, а также аортального окна.
Частота развития постпневмонэктомического бронхиального свища без лимфодиссекции составляет около 1% [11], с лимфодиссекцией, по данным разных авторов, — от 0 до 20%[11, 14, 16]. При этом некоторые авторы не всегда указывают объем выполненной лимфодиссекции. За последние два десятилетия не отмечено особой тенденции к снижению данного показателя. Причем слева бронхиальный свищ возникает в 5 раз реже, чем справа [14]. Отдельные авторы подчеркивают значительную роль бифуркационной лимфодиссекции в развитии ишемических поражений трахеобронхиальной стенки, поскольку именно при бифуркационной диссекции возможно поражение бронхиальных артерий (питающих в том числе зону культи главного бронха). Именно ишемия является главной причиной развития постпневмонэктомического бронхиального свища. В меньшей степени, но все-таки имеют значение неоадъювантные химиотерапия и лучевая терапия, длительность интубации трахеи, хирургическая инфекция, рост опухоли по линии резекции бронха, стадия рака легкого, сопутствующие заболевания (хронические обструктивные болезни легких и сахарный диабет), объем интраоперационной кровопотери, метод обработки культи главного бронха. Касаемо последнего пункта, наиболее надежными являются методы ручной бескультевой обработки и обработки культи главного бронха при помощи одноразового линейного сшивающего аппарата. Менее надежной считают обработку культи главного бронха с помощью многоразовых сшивающих аппаратов типа УО-40 и УО-60. Частота развития свищей в зависимости от метода обработки культи может отличаться примерно в 5 раз [11, 10]. Хронический бронхит курильщика также может вносить лепту в развитие постпневмонэктомического бронхиального свища, хотя это скорее способствующий фактор, чем истинная причина. Онкохирург всегда балансирует между достаточным онкологическим радикализмом выполненной операции и потенциальной возможностью развития бронхиального свища. Возникший постпневмонэктомический бронхиальный свищ представляет собой серьезную проблему и порой сводит на нет все старания хирурга. Летальность при консервативном лечении по поводу постпневмонэктомического бронхиального свища, по данным, например P.H. Hollaus и соавторов (1997) [17], составляет около 67%. Впечатляющая цифра, не так ли?
Диагностика
Постпневмонэктомический бронхиальный свищ редко проявляет себя раньше 7-х суток после операции, чаще всего манифестирует на 7–11-е сутки, но бывает и намного позже — 15–21-е сутки. Заподозрить свищ следует, если в период кажущегося полного выздоровления резко повышается температура тела до 38–39 °С и более, усиливается или появляется кашель — сначала сухой, затем с выделением большого количества мокроты, начинает промокать повязка послеоперационной раны серозным отделяемым — сначала немного, затем обильно (при свищах, возникших на 7–12-е сутки), часто развивается эмфизема грудной клетки, шеи, лица, иногда — живота, мошонки (у мужчин). Выполнение диагностической плевральной пункции остаточной плевральной полости, как правило, подтверждает диагноз, хотя и в этом могут быть определенные трудности. Например, при свищах, возникших позже 11-х суток, остаточная плевральная полость делится на автономные части большими свертками фибрина, и поэтому при пункции одной из таких частей хирург получает определенное количество экссудата и не получает воздух, поскольку часть остаточной плевральной полости изолирована от свища. В таких случаях нужно сделать еще одну пункцию. К примеру, если первая пункция выполнена во II–III межреберье по среднеключичной линии, то вторую пункцию следует проводить возле угла лопатки. Как правило, будет получен воздух и не будет «удерживаться герметизм», что подтверждает диагноз. На этом этапе выполняют дренирование остаточной плевральной полости и налаживание системы пассивной аспирации по Бюлау, за считанные часы состояние больного резко улучшается. Компьютерная томография (КТ) органов грудной полости (ОГП) и/или фибробронхоскопия, произведенные после установления дренажа, полностью подтверждают диагноз. В этот период (1–2-е сутки после установления диагноза) решается дальнейшая судьба пациента.
Выбор лечения. Консервативное лечение
Выбор терапии при развившемся осложнении имеет огромное значение. При отсутствии оперативного лечения летальность, по данным некоторых авторов, составляет 67%. Причиной летального исхода являются:
- нарушение механики дыхания;
- контаминация контралатерального легкого;
- плеврогенный хрониосепсис.
Обобщая результаты консервативного лечения, удалось выявить, что при применении фибринового клея смогли добиться выздоровления 20,0% пациентов, при использовании лазера, прижигания свища химическими компонентами или подслизистого введения склерозирующих веществ выздоравливают 33–58% больных с уровнем летальности 26–66%. Общая смертность в пяти лучших сериях наблюдений эндоскопического лечения свищей составляла 39,6%. Из 85 больных с постпневмонэктомическими бронхиальными свищами и ассоциированными с ними эмпиемами остаточной плевральной полости авторам удалось вылечить только 30,1% [14].
Следует отметить, что такое лечение растягивается на достаточно долгое время (при успешном его проведении) — 2,5–3 мес. Автор данной статьи с помощью эндоскопического прижигания постпневмонэктомического бронхиального свища 50% раствором трихлоруксусной кислоты полностью вылечил 3 таких пациентов (у 5 больных метод оказался неэффективен). Процедуры производили через гибкий бронхоскоп 1 раз в 3–4 дня, на одно прижигание расходовали 0,4–0,8 мл 50% раствора трихлоруксусной кислоты. Параллельно с эндоскопическим лечением налаживали систему проточного промывания остаточной плевральной полости антисептиками — раствор декаметоксина чередовали с 2–3% водным раствором борной кислоты в объеме 200–600 мл ежесуточно.
Необходимо отметить, что при такой терапии после закрытия бронхиального свища проточное промывание остаточной плевральной полости проводят еще 2–3 нед для полного разрешения эмпиемы (которая сохраняется еще несколько недель после эндоскопической ликвидации бронхиального свища). В состав комплексного лечения входит неспецифическая иммунотерапия полиоксидонием (№ 10), внутриполостное введение бактериофага (обычно синегнойного, так как конечным возбудителем эмпиемы является, как правило, синегнойная палочка). Бактериофаг вводят внутриплеврально через верхний дренаж — широкий подключичный катетер, установленный в плевральную полость во II межреберье по среднеключичной линии. Интервал между введением растворов антисептиков и бактериофага (внутриплеврально) составляет не менее 8 ч. Конечно, всем больным выполняют бактериальный посев в процессе лечения. Возбудитель эмпиемы — чаще всего полирезистентная синегнойная палочка, поэтому роль антибиотиков в лечении данного контингента пациентов скромна. Кроме того, при таком методе терапии, после полного закрытия бронхиального свища, следует примерно 1 раз в 2 нед проводить замену нижней дренажной трубки на новую по тому же «каналу», так как даже в самой дренажной трубке и вокруг нее «гнездится» инфекция, а для полной ликвидации эмпиемы этот прием является необходимым. Следует подчеркнуть, что в лечении склерозирующими препаратами имеет значение размер бронхиального свища. Если свищ составляет 1–4 мм, можно надеяться на успех терапии, если больше — излечение пациента с помощью данного метода маловероятно [12] (хотя автору статьи с помощью эндоскопических прижиганий 50% трихлоруксусной кислотой удалось полностью излечить больного со свищом размерами 10×3 мм, но это скорее исключение из общего правила). Естественно, если бронхиальный свищ полный или занимает ½–¾ культи бронха, описанные методы мало- или неперспективны. Установление трахеобронхиального стента или бронхоблокирующего клапана многие авторы вообще не рассматривают как заслуживающий внимания метод лечения при постпневмонэктомическом бронхиальном свище. Таким образом, эндоскопическим технологиям необходимо дальнейшее развитие и улучшение, поскольку в настоящее время они не составляют достойной альтернативы хирургическому лечению.
Хирургическое лечение
Для хирургического лечения пациентов с постпневмонэктомическим бронхиальным свищом принципиальное значение имеет время от момента возникновения усложнения: ранний (первые 2 сут, то есть до развития эмпиемы плевры) или поздний (когда уже есть эмпиема плевры) бронхиальный свищ. Прежде чем перейти к современным методам хирургии при постпневмонэктомическом бронхиальном свище, кратко остановлюсь на более ранних.
При первичной несостоятельности культи главного бронха (в первые 2 сут, до развития эмпиемы плевры) планировали выполнить реторакотомию и повторное ушивание культи бронха с обязательной ее плевризацией (либо вместо плеврального лоскута использовать перикардиальный, межреберный лоскут или жировой подвесок перикарда). Однако некоторые авторы справедливо относят применение таких лоскутов для укрепления культи бронха к категории хирургического самообмана. Механическая непрочность, гиповаскулярность лишают их пластических свойств — перикард прочный, но слишком тонкий [13, 14]. Вышеуказанные операции, применяемые до развития эмпиемы плевры, малоэффективны (рецидив свища составляет около 75% случаев). Если диагностирована вторичная несостоятельность культи главного бронха, ушивание ее в условиях острой эмпиемы бесперспективно. В таких случаях предлагали срочно проводить дренирование остаточной плевральной полости, при недостаточной эффективности которого показано открытое дренирование плевральной полости — торакостомия. Оперативное закрытие бронхиального свища осуществляли только после тщательной санации остаточной плевральной полости и улучшения общего состояния больного.
Операции, применяемые для лечения при хронических постпневмонэктомических бронхиальных свищах
Реампутации и окклюзии культи главного бронха при постпневмонэктомическом бронхиальном свище возможны при достаточной длине культи (1,5–2,0 см). Разработаны и используются 3 доступа к культе бронха:
- трансплевральный доступ на стороне пневмонэктомии, то есть через полость эмпиемы;
- трансстернальный доступ — через средостение или перикард;
- задний контралатеральный доступ к культе левого главного бронха через правую плевральную полость.
Операции из всех вышеперечисленных подходов направлены на ликвидацию свища (его ререзекцию и реушивание), герметизацию плевральной полости эмпиемы и создание условий для ее ликвидации (используют дополнительно торакомиопластику) — по методу Л.К. Богуша, Б.С. Бабашева — Ч. Нуркабаева или без него (метод И.С. Колесникова). Например, операции, проводимые через средостение (М.И. Перельман, Т.Б. Богуславская) заключаются в пересечении и удалении культи главного бронха с зашиванием отверстия в трахее. После таких операций, как правило, происходит уменьшение размера остаточной плевральной полости, состояние больных улучшается, снижается гнойная интоксикация, создаются благоприятные условия для ликвидации полости эмпиемы методом пункции, дренирования, а при необходимости — торакопластикой и мышечной пластикой. В тех случаях, когда культя бронха очень короткая или полностью отсутствует, предлагалось выполнять циркулярную резекцию бифуркации трахеи с наложением анастомоза трахеи с главным бронхом единственного легкого [5]. Выполнение подобной операции в такой ситуации опасно ввиду высокого риска несостоятельности анастомоза, наложенного в условиях воспаления, и в случае неуспеха подобного вмешательства последствия будут более серьезными, нежели образование постпневмонэктомического бронхиального свища. Операции, выполненные по поводу постпневмонэктомического бронхиального свища с хронической эмпиемой плевры, являются сложными и травматическими хирургическими вмешательствами. Успех их проведения во многом зависит от совершенства техники и индивидуального опыта хирурга, а также от высококвалифицированного анестезиологического и реаниматологического обеспечения. Рецидивы бронхиального свища и послеоперационная летальность высоки.
Современные методы хирургического лечения
В настоящее время с учетом крайне недостаточной эффективности консервативных методов лечения при постпневмонэктомических бронхиальных свищах агрессивная хирургическая тактика является наиболее оправданной. Простое повторное ушивание свища или ререзекция культи бронха абсолютно бесполезны. Единственной возможностью надежно ликвидировать свищ культи бронха является пластика культи. В большинстве случаев рекомендуется применение оментопластики, в исключительных случаях — диафрагмопластики. Операцию выполняют в день манифестации свища, максимум — на следующий день. Сначала через лапаротомный доступ мобилизуют большой сальник на правых желудочно-сальниковых сосудах (для надежного кровоснабжения лоскута) вне зависимости от стороны свища (их длины, как правило, хватает). Затем выполняют реторакотомию в положении больного на боку. Плевральную полость санируют, производят ререзекцию и реушивание культи (иногда при наличии длинной культи свищ оставляют открытым — см. ниже). Очень важным является способ фиксации большого сальника к культе бронха: практиковавшаяся ранее фиксация сальника лигатурами культи бронха, а также узловыми швами к соседним структурам средостения (так называемый узловой способ фиксации) приводила к большому количеству рецидивов (около 75%). При данном способе фиксации нивелируются все полезные свойства большого сальника.
С 2000 г. начали разрабатывать и применять технологии фиксации пластического материала П-образными швами, тампонаду культи бронха биологическим тампоном из большого сальника, муфтообразную фиксацию — все эти способы объединяют понятием «плотной» фиксации, поскольку пластический материал призван автономно обеспечивать герметичность плевральной полости, независимо от состоятельности культи бронха. Эффективность данного способа составляет около 90%. Примечательно, что применение технологий «плотной» фиксации сальникового лоскута не сказывалось на частоте несостоятельности культи бронха: понятия «бронхиальный свищ» и «несостоятельность культи» перестали быть синонимами. Поскольку сальниковый лоскут при его «плотной» фиксации способен автономно обеспечивать герметичность плевральной полости, во многих случаях расхождение краев культи бронха не реализовывалось в свищ. У 17 из 30 пациентов, у которых была выполнена оментопластика культи главного бронха по поводу острого бронхиального свища, эндоскопическим методом выявлено повторное расхождение культи бронха, но рецидив свища был только у 3 из них. Таким образом, в 14 из 30 наблюдений большой сальник автономно обеспечивал герметичность плевральной полости, а все 14 случаев несостоятельности культи бронха выявлены только эндоскопически в виде дефектов культи бронха, плотно прикрытых сальником (культю бронха у всех больных обрабатывали вручную по методике А.Х. Трахтенберга) [14]. Несостоятельность культи бронха — явление преимущественно биологическое, и его вряд ли можно быстро устранить, используя биологические лоскуты. Однако бронхиальный свищ — в большей степени «механическое» понятие, поэтому решить проблему свища оказалось проще и эффективнее, чем несостоятельности культи бронха. Кроме того, сальниковый лоскут является донором продуктивного воспаления и неоваскулогенеза, что имеет большое значение при дальнейшем гранулировании свища.
Итак, основными способами «плотной» фиксации большого сальника к культе бронха являются:
1. Фиксация большого сальника к культе бронха с помощью пяти П-образных швов:
- нижнего шва через парааортальную фасцию;
- верхнего шва через парааортальную фасцию;
- верхнего шва через боковую стену трахеи;
- переднего шва через переднюю стенку бифуркации трахеи;
- нижнего шва через медиальную стенку левого главного бронха.
2. Тампонада культи бронха «биологическим тампоном» из большого сальника с фиксацией к культе бронха П-образным швом и непрерывным атравматичным швом к краю культи бронха.
Ограничение метода состоит в том, что он применим только при наличии относительно длинной (не менее 1,5 см) культи бронха.
3. Тампонада культи бронха с использованием армирующего шва.
Такой метод можно применять, когда свищ полный и культя бронха практически отсутствует. Некротизированные края трахеобронхиального дефекта экономно иссекают, отступая от краев дефекта приблизительно на 1–1,5 см, через все слои стенки трахеи и от противоположного главного бронха проводят П-образный армирующий шов нитью «Polysorb 0-1» или «PDS0-1». Под этот шов протягивают достаточно мощную прядь сальника, после чего до легкого натяжения шов завязывают. Прядь сальника фиксируют в виде петли за армирующий шов и подшивают непрерывным атравматичным швом к краям дефекта.
4. Плотная муфтообразная фиксация сальника к культе бронха.
Трахея и противоположный главный бронх циркулярно мобилизуют на достаточном протяжении и окутывают прядью сальника, образовавшей плотную герметичную муфту вокруг трахеи, противоположного бронха и культи бронха, производят фиксацию П-образным швом [14].
Летальность пациентов, перенесших оментопластику острого бронхиального свища, довольно высока — около 26,7%, но количество смертей больных, леченных консервативно, намного больше — около 67,0%. Однако такой показатель отмечали у авторов методики в период ее разработки, в настоящее время он значительно снизился.
Таким образом, при условии правильной мобилизации и фиксации большого сальника такой метод является высокоэффективным в хирургическом лечении по поводу острого постпневмонэктомического бронхиального свища.
В случае, когда по разным причинам постпневмонэктомический бронхиальный свищ запущен, то есть после 2 сут с момента возникновения, сочетается с эмпиемой плевры и гнойной интоксикацией, единственным рациональным методом терапии является открытое дренирование остаточной плевральной полости — торакостомия (предварительно остаточную плевральную полость дренируют с помощью трубчатого дренажа, налаживают систему пассивной аспирации по Бюлау, состояние больного стабилизируется в течение 1–2 дней).
Торакостомия (проводят в положение больного лежа на спине, наркоз — общий) заключается в резекции III–V ребра на протяжении примерно 12 см. Свободные края кожи и плевры сшивают, образуя «окно», достаточное для мануального и визуального контроля всех отделов санируемой плевральной полости, после чего тампонируют 2–3 большими салфетками, пропитанными 1% раствором повидон-йода или йодопирона. В дальнейшем применяют ежедневные перевязки с 2–3, а по уменьшении остаточной плевральной полости — 1 салфеткой, пропитанной, например, 1% раствором повидон-йода. В течение 4–5 нед остаточную плевральную полость санируют. Тампонада остаточной плевральной полости салфетками надежно защищает противоположное легкое от аспирации патологического содержимого полости. Кроме того, прикрывают «шунт» воздуха — он вновь возникает только на короткий период во время перевязки. После этой операции состояние больного значительно улучшается, ежедневная открытая санация остаточной плевральной полости быстро приводит к ее очищению и началу гранулирования, незамедлительно исчезают симптомы гнойной интоксикации, нормализуется состояние пациента, эмпиема остаточной плевральной полости ликвидируется, угроза сепсиса исчезает, риск пневмонии противоположного легкого сводится к минимуму. После санации плевральной полости путем торакостомии и последующих перевязок возникает вопрос: что делать дальше? Варианты следующие.
1. Если свищ спонтанно гранулирует (закрывается), плевральная полость уменьшается в объеме и обеспечивается санирование, можно выполнить простое ушивание торакостомы, а если есть сомнения в полной санации остаточной плевральной полости, предпочтительнее дальнейшее консервативное лечение — применение перевязок в течение длительного времени (торакостома как бы «зарастает» изнутри); либо возможно применение торакопластики.
2. Чаще всего требуется отсроченная операция по коррекции свища и плевральной полости — оментоторакопластика.
3. Если диагностируют прогрессирование основного заболевания после наложенной торакостомы (например спустя 1–1,5 мес), продолжают проводить перевязывание и симптоматическое лечение. В этом случае, разумеется, об оментоторакопластике речь не идет.
Несмотря на высокую (около 90%) эффективность оментопластики культи бронха, выполненной по поводу постпневмонэктомического бронхиального свища, возможен вариант развития его рецидива.
Клинический случай
Больной С., 54 лет, поступил в торакальное отделение Одесского областного онкологического диспансера 21.11.2014 г. с диагнозом «рак левого легкого, центральная форма, Т2N1M0, IIБ стадия, II клиническая группа, осложненный ателектазом нижней доли легкого (цитологически — плоскоклеточный рак)». 27.11.2014 г. пациент оперирован, выполнена левосторонняя пульмонэктомия с лимфодиссекцией до D2.
Получено гистологическое заключение № 42877-87 от 01.12.2015 г.: G2–3 плоскоклеточный рак легкого, в лимфоузлах корня легкого и бифуркационных лимфоузлах — метастазы, другие группы лимфоузлов — реактивная гиперплазия, край резекции без особенностей. Диагноз после операции — рак левого легкого, центральная форма, pT2N2M0, IIIA стадия, II клиническая группа. На 17-е сутки послеоперационного периода состояние больного резко ухудшилось: отмечали повышение температуры тела до 38,5 °С, кашель с обильным выделением серозной мокроты, подкожную эмфизему грудной клетки (преимущественно слева), шеи, лица, одышку при физической нагрузке. Выполнена диагностическая плевральная пункция слева — получено 500 мл серозного экссудата и воздух, то есть «герметизм» не удерживался. Дополнительно проведена КТ ОГП (рис. 1), диагностирован бронхиальный свищ культи левого главного бронха протяженностью около 5 мм (по данным КТ от 16.12.2014 г.). Больному в ургентном порядке выполнено дренирование остаточной плевральной полости слева, налажена система пассивной аспирации по Бюлау. За сутки состояние пациента значительно улучшилось: одышка исчезла, подкожная эмфизема значительно уменьшилась; принято решение повторно оперировать. 16.12.2014 г. произведено хирургическое вмешательство — верхнесрединная лапаротомия, мобилизация большого сальника на правых желудочно-сальниковых сосудах, реторакотомия слева, диафрагмотомия, пластика культи левого главного бронха большим сальником. С учетом наличия культи длиной около 2 см выбран способ тампонады культи левого главного бронха «биологическим тампоном» из большого сальника с фиксацией к культе бронха П-образным и непрерывным атравматичным швом. На 6-е сутки послеоперационного периода диагностирован рецидив свища культи левого главного бронха (рис. 2), в связи с чем принято решение о выполнении еще одного оперативного вмешательства — наложения торакостомы слева (проведено 25.12.2014 г.). Состояние больного в 1-е сутки после операции было стабильное, начиная со 2-х суток — ближе к удовлетворительному. У пациента с 1-х суток применяли перевязки, оставляя в остаточной плевральной полости две большие салфетки, пропитанные 1% раствором повидон-йода. На 10-е сутки послеоперационного периода большой сальник плотно фиксировался к культе главного бронха; свищ ликвидирован (рис. 3). В дальнейшем констатировано значительное уменьшение объема остаточной плевральной полости (рис. 4) — для перевязок спустя месяц достаточно было только одной салфетки. Больной от торакопластики отказался, был выписан для перевязок по месту жительства в удовлетворительном состоянии с контролем в диспансере через месяц.
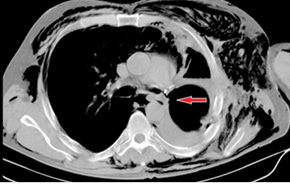
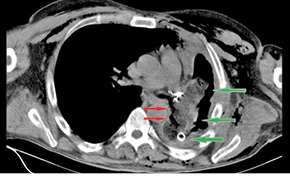
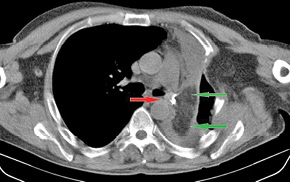
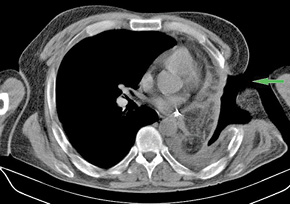
Профилактика
Учитывая особенности выполнения пульмонэктомий с лимфодиссекциями и высокий риск развития бронхиального свища после таких операций, большое внимание исследователи уделяют профилактике развития этого осложнения. Разработана методика (Д.А. Чичеватов) превентивной диафрагмопластики культи правого главного бронха [13]. В меньшей степени отработана подобная операция при культе левого главного бронха. Но, принимая во внимание то, что слева бронхиальный свищ развивается в пять раз реже, чем справа, автор рекомендует выполнять диафрагмопластику при культе правого главного бронха у 100% больных и лишь в исключительных случаях применять эту процедуру при левосторонних операциях. Результаты подобных оперативных вмешательств следующие: только у 3 (2,6%) из 114 пациентов возник бронхиальный свищ, еще у 5 (4,4%) больных эндоскопически зафиксирована несостоятельность культи бронха, тем не менее ни у одного из них бронхиальный свищ не сформировался. Диафрагмальный лоскут автономно, несмотря на расхождение краев культи бронха, обеспечивал герметичность плевральной полости, затем дефект культи быстро гранулировал в течение 7–10 сут. Таким образом, применение диафрагмального лоскута не снижало частоту развития несостоятельности культи бронха, но приводило к уменьшению количества бронхиальных свищей, что является прямым свидетельством эффективности лоскута [14]. Технический аспект этой операции заключается в проведении двух торакотомий: основной — по V межреберью и дополнительной — по VIII или IX межреберью, из которой происходит мобилизация лоскута. Авторы не отмечают развития осложнений, связанных с дополнительной торакотомией. Сама же операция (пульмонэктомия с лимфодиссекцией до D2 и диафрагмопластикой культи бронха) удлиняется в среднем на 40 мин. Диафрагмальный лоскут фиксируют к культе правого главного бронха пятью П-образными швами (аналогично фиксации сальникового лоскута — см. выше). Сальниковый лоскут также можно применить (в действительности используют значительно реже) с превентивной целью аналогично диафрагмальному, но это менее предпочтительный вариант в связи с громоздкостью такой операции (вскрытие двух полостей, значительное удлинение времени операции и т.д.), хотя биологические свойства сальникового лоскута ничуть не хуже диафрагмального. Уместно отметить еще одну деталь: диафрагмальный лоскут можно применять для оперативного лечения по поводу уже возникшего постпневмонэктомического бронхиального свища в ситуациях, когда большой сальник отсутствует ввиду ранее перенесенных операций на органах брюшной полости, но в таком случае его ограничением являются сроки возникновения острого бронхиального свища. Для реализации пластического потенциала диафрагмального лоскута его следует фиксировать к культе главного бронха строго определенным образом, когда анатомические отношения органов в средостении не нарушены. Это возможно только при лечении свищей, образовавшихся в первые 10–15 сут с момента операции, в более поздние сроки применение диафрагмального лоскута в такой ситуации невозможно технически.
Предлагаю алгоритм лечения пациентов с постпневмонэктомическим бронхиальным свищом (рис. 5).
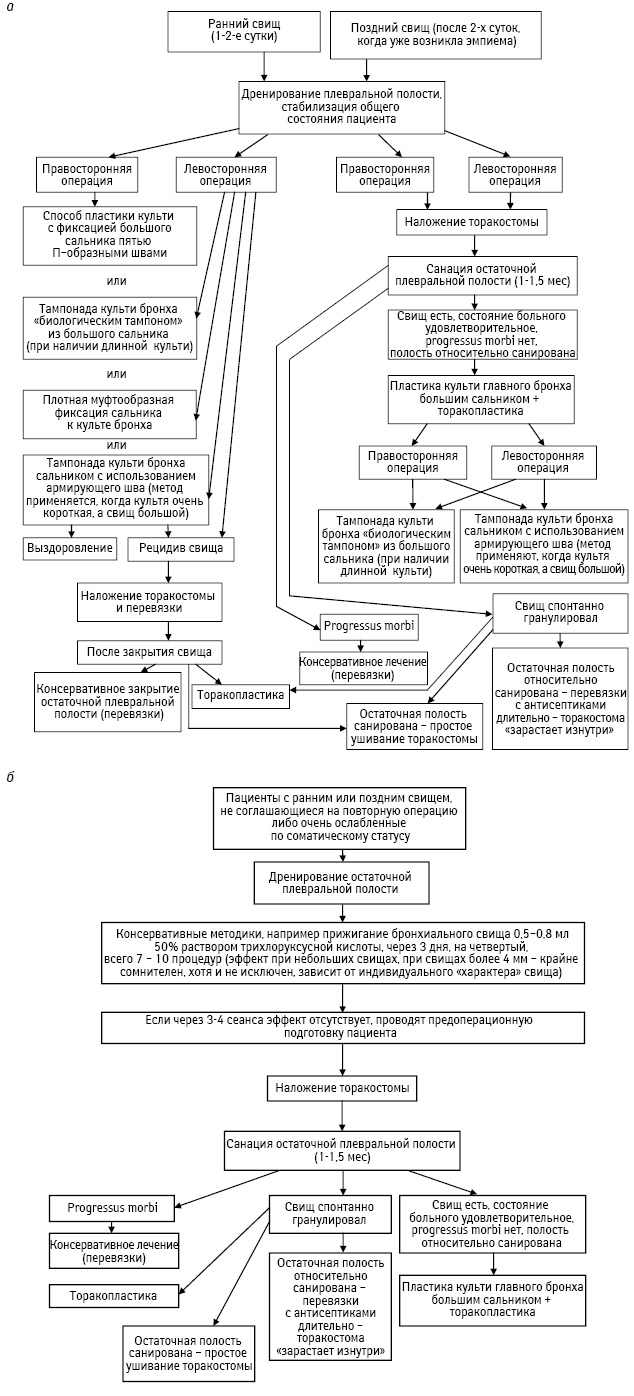
Выводы
Проблема постпневмонэктомических бронхиальных свищей в торакальной онкохирургии также актуальна сегодня, как и 2–3 десятилетия назад, с учетом выполняемых лимфодиссекций, большого количества расширенных и комбинированных пульмонэктомий, проводимых по поводу рака легкого, применения неоадъювантных полихимиотерапии и лучевой терапии (неоадъювантная лучевая терапия в настоящее время исключена из стандартов лечения пациентов с раком легкого в Украине, но ее используют в других странах). Лечение по поводу реализовавшегося постпневмонэктомического бронхиального свища представляет собой весьма сложную задачу, прогноз для больных неудовлетворительный, эффективность консервативных методов терапии оставляет желать лучшего. Ранее практиковавшиеся методы оперативного вмешательства, разработанные в 50–70-х годах ХХ века, постепенно уходят в прошлое по причине их большой технической сложности выполнения, травматичности для больного, недостаточной эффективности, большого количества осложнений. Разработанные в последние 10–15 лет современные хирургические методы лечения: оментопластика культи главного бронха — при острых (ранних) свищах и оментоторакопластика (с предварительно наложенной торакостомой на 1–1,5 мес и санацией остаточной плевральной полости) — при поздних (с эмпиемой) бронхиальных свищах, — кардинально изменили прогноз у этого контингента пациентов. Созданы и внедряются новые методы профилактики постпневмонэктомических бронхиальных свищей — превентивная диафрагмопластика культи главного бронха и превентивная оментопластика культи главного бронха (намного реже). В основном такие операции выполняют справа, подобные левосторонние оперативные вмешательства применяют как исключение при очевидной необходимости.
Список использованной и рекомендованной литературы
1. Атлас грудной хирургии (1971). Под ред. Б.В. Петровского. Т. I. Медицина, Москва, 440 с.
2. Атлас онкологических операций (2008). Под ред. В.И. Чиссова, А.Х. Трахтенберга, А.И. Пачеса. ГЭОТАР-Медиа, Москва, 632 с.
3. Большой сальник (1989) Пер. с англ. под ред. Д. Либерманн-Мефферд, Х. Уайта. Медицина, Москва, 336 с.
4. Гетьман В.Г. (1995) Клиническая торакоскопия. Здоров’я, Киев, 208 с.
5. Наружные и внутренние свищи (1990) Под ред. Э.Н. Ванцяна. Медицина, Москва, 224 с.
6. Проценко А.В., Лукьянов Ю.В. (2007) Факторы, влияющие на частоту развития бронхиального свища после пульмонэктомии. Онкология, 9(4): 361–364.
7. Справочник по онкологии (2008) Под ред. С.А. Шалимова, Ю.А. Гриневича, Д.В. Мясоедова. Здоров’я, Киев, 576 с.
8. Торакальная хирургия (2004) Под ред. Л.Н. Бисенкова. ЭЛБИ-СПб, Санкт-Петербург, 928 с.
9. Трахтенберг А.Х., Попов М.И., Захарченков А.В. и др. (1990) Методика обработки культи бронха при хирургическом и комбинированном лечении больных раком легкого. Хирургия, 4: 15–18.
10. Трахтенберг А.Х., Чиссов В.И. (2000) Клиническая онкопульмонология. ГЭОТАР Медицина, Москва, 600 с.
11. Трахтенберг А.Х., Чиссов В.И. (2009) Рак легкого. Атлас. ГЭОТАР-Медиа, Москва, 656 с.
12. Хирургия легких и плевры (1988) Под ред. И.С. Колесникова, М.И. Лыткина. Медицина, Ленинград, 384 с.
13. Чичеватов Д.А., Горшенев А.Н., Силев Е.Н. (2005) Клинический прогноз несостоятельности культи главного бронха у больных раком легкого. Вопросы онкологии, 51(1): 122–124.
14. Чичеватов Д.А. (2013) Диафрагмальный и сальниковый лоскуты в грудной хирургии. ЭЛБИ-СПб, Санкт-Петербург, 144 с.
15. Шкваровский И.В. (2000) Дислокация сальника в правую плевральную полость. Вестник хирургии им. И.И. Грекова, 159(2): 19–20.
16. Apostolakis E., Panagopoulos N., Dougenis D. (2008) Comment: Routine or selective reinforcement of bronchial stump after pneumonectomy? Interact. Cardiovasc. Thorac. Surg., 7: 625.
17. Hollaus P.H., Lax F., El-Nashef B.B. et al. (1997) Natural history of bronchopleural fistula after pneumonectomy: a review of 96 cases. Ann. Thorac. Surg., 63: 1391–1397.
Адрес:
Душко Николай Евгеньевич
65055, Одесса, ул. Неждановой, 32
Одесский областной клинический онкологический диспансер
Е-mail: dushcko.nickolai@yandex.ua














Leave a comment