Місцеві ускладнення хіміотерапії: токсичні флебіти та екстравазації
Сивак Л.А., Філоненко Е.С., Губарева Г.О.
Резюме. У статті представлено огляд літератури щодо розвитку, діагностики та лікування токсичних флебітів та екстравазацій хіміопрепаратів внаслідок проведення хіміотерапії (ХТ), а також продемонстровано власний досвід з вивчення даних ускладнень. Виявлено, що місцеві ускладнення ХТ є досить частими (до 15%) та серйозними ускладненням лікування, розвиток яких може призводити до зниження ефективності ХТ та вимагає активного лікування і профілактики.

Серед місцевих токсичних наслідків хіміотерапевтичного лікування достатньо частою та найбільш серйозною проблемою є розвиток токсичних флебітів та екстравазацій хіміопрепаратів. Хоча ці ускладнення і є локальними, проте часом вони завдають значної шкоди пацієнтам, оскільки пов’язані з вираженим больовим синдромом, порушенням функції ураженого органу на обмежений час, а у деяких випадках пожиттєво, впливаючи, таким чином, на якість життя хворого і вимагаючи додаткових фінансових витрат на лікування та відновлення функціонування ушкодженого органу або кінцівки.
Втім, незважаючи на актуальність даного питання, ці ускладнення, як правило, належать до буденних, у зв’язку з чим у світі не проводять серйозних досліджень токсичних флебітів та екстравазацій хіміопрепаратів на великих популяціях пацієнтів. Більшість досліджень ретроспективні та мають епідеміологічний характер.
Зокрема, результати одного з найбільш широких досліджень епідеміології флебітів та екстравазацій хіміопрепаратів були опубліковані у 2007 р. у вигляді Рекомедацій з лікування екстравазацій Європейським онкологічним співтовариством медичних сестер (European Oncology Nursing Society Extravasation guideline) [1]. Авторами було проаналізовано понад 2000 випадків екстравазацій та токсичних флебітів.
Згідно з результатами цього дослідження місцеві ускладнення хіміотерапії (ХТ) зустрічаються частіше у жінок (58%). Серед вікових груп найбільший ризик їх виникнення у пацієнтів похилого віку (серед пацієнтів у віці 50–64 років зареєстровано 650 випадків, понад 65 років — 840 випадків), у той час як у молодих пацієнтів він нижчий (у віці 1–18 років — 51 випадок, 18–34 роки — 157 випадків, 35–49 років — 312 випадки).
За даними С. Sauerland (2006) [2], при проведенні інфузії найвищий ризик виникнення цих ускладнень у 44% пацієнтів відмічено з 14 до 22 години. До препаратів, які найчастіше викликають виникнення токсичних флебітів та екстравазацій хіміопрепаратів належать: 5-фторурацил — у 35%, препарати платини — у 22%, доксорубіцин та етопопзид — у 9% хворих.
С. Sauerland та співавтори (2006) [2] відмічають ряд факторів ризику розвитку токсичного флебіту та екстравазації цитотоксичних агентів за межі кровоносного русла. До них належать: онкологічне захворювання, ушкодження вени, застосування катетера неадекватної довжини та діаметра відносно обраної вени, властивості інфузійних препаратів (цитотоксичність, вазодилятуючий ефект, pH, осмолярність) та їх взаємодії з тканинами організму, надмірна концентрація та об’єм препарату, порушення судинного тонусу, фактор пацієнта, конкурентні медикаменти, техніка втручання.
Вплив на ці фактори ризику розвитку флебітів та екстравазацій хіміопрепаратів, на думку R. Wickham та співавторів (2006), є основою профілактики виникнення локальних ускладнень цитостатичної терапії [3].
Онкопатологія сама собою є фактором ризику ускладнень лікування. Пацієнти онкологічних закладів зазвичай отримують численні інфузії, що часто призводять до ламкості, порушень рухомості та складностей катетеризації судини. Супутні захворювання периферичних вен, кахексія, зміни еластичності тканин після радіотерапії, вторинна лімфедема також сприяють високому ризику розвитку екстравазації судин [3]. Ушкодження судин у онкологічних пацієнтів обумовлено багаторазовими внутрішньовенними (в/в) втручаннями, іноді — недостатньо надійним закріпленням інфузійного обладнання (інфузійної системи, голки, катетера), часом — надмірно активними маніпуляціями з катетером [3].
Ризик розвитку токсичних флебітів та екстравазацій хіміопрепаратів залежить від властивостей розчинів, зростає при рівні pH розчину за межами 5,5– 8,5 та при осмолярності, що перевищує осмолярність плазми (290 мосмоль/л), а також наявності певних компонентів розчину (етиловий спирт, поліетиленгліколь). Осмолярність інфузійного розчину, вища за осмолярність сироватки крові та міжклітинної рідини, обумовлює як безпосереднє пошкодження клітин за рахунок осмолярного тиску (відбувається дегідратація та зморщування клітини), так і за рахунок транспорту хіміопрепарату, тобто поширення пошкодження за межі площі первинного ушкодження. До таких речовин належать гіпертонічні розчини глюкози, натрію, калію та кальцію хлориду, парентеральне харчування, контрастні препарати для рентгенологічних досліджень, антибіотики. Низькоосмолярні речовини в основному проявляють свою цитотоксичну дію шляхом набухання клітин і розриву їх зовнішньої мембрани. Крім того, великі об’єми інфузійних розчинів також можуть призвести до виникнення місцевих ускладнень за рахунок тривалості їх введення [3].
Завдяки механізму дії цитостатичних препаратів питання їх екстравазації є дуже актуальним. Більшість із них належать до везикантів, тобто речовин, які призводять до тяжких ушкоджень тканин. Вони безпосередньо взаємодіють з ДНК клітини, спричиняючи поступове вмирання здорових клітин, що зовні проявляється розширенням країв виразки. Наприклад, доксорубіцин виявляють у тканинах впродовж 5 міс після екстравазації, а це означає, що весь цей час продовжується ушкодження тканин. Виразки, обумовлені дією високотоксичних агентів, зазвичай не загоюються і потребують пластичної хірургії та пересадки шкіри [2].
На виникнення токсичних флебітів та екстравазацій хіміопрепаратів впливає фактор пацієнта, тобто наявність супутньої патології (лімфедема, цукровий діабет, захворювання периферичних судин, синдром верхньої порожнистої вени, високий артеріальний тиск, ампутовані кінцівки, що обмежують вибір венозного доступу), проведення попередньої променевої терапії на ділянку ураження або на суміжну з нею зону та соціальні особливості. Окрему групу ризику становлять новонароджені, діти, літні люди та пацієнти з обмеженими можливостями спілкування. Немовлята потрапляють у цю категорію завдяки особливостям будови шкіри, необхідності тривалої антибіотикотерапії та парентерального харчування, складностям повідомлення про біль та при спробах його локалізувати. Літні люди потрапляють до групи ризику у зв’язку зі зниженням больової чутливості, підвищенням ламкості судин та загальним ослабленням організму. Усе це може призвести до запізнілої діагностики місцевих ускладнень поліхіміотерапії (ПХТ). Пацієнти з обмеженими можливостями спілкування (пацієнти під загальною анестезією, заінтубовані хворі у відділенях інтенсивної терапії, хворі у коматозних станах, паралізовані, німі пацієнти) іноді не мають змоги повідомити про якісь негаразди [3].
Згідно з даними А. Corrigan та співавторів (2000) перед початком інфузії завжди слід попереджати пацієнта про можливі ускладнення хіміотерапевтичного лікування, повідомити його, на що слід звертати увагу та в яких випадках необхідно звертатися за медичною допомогою [4].
Застосування деяких медикаментів сприяє підсиленню місцевих ускладнень ХТ за рахунок певного механізму дії. Особливості дії найчастіше застосовуваних препаратів представлено в табл. 1.
Таблиця 1. Ліки, що підвищують ризик місцевих ускладень ХТ
| Клас препаратів | Особливості механізму дії |
|---|---|
|
Антикоагулянти Антифібринолітики Антиагреганти |
Можуть ускладнювати екстравазацію хіміопрепаратів чи спричиняти додаткове пошкодження, підсилюючи місцеву кровотечу |
|
Вазодилятатори |
Можуть прискорювати місцевий кровотік та збільшувати ділянку ураження |
|
Діуретики |
Можуть прискорювати місцевий кровотік |
|
Антигістамінні препарати |
Можуть звужувати капіляри та артеріоли, спричиняючи ішемічне ураження |
|
Анальгетики |
Зниження больового відчуття може призвести до запізнілої діагностики екстравазації хіміопрепаратів |
|
Внутрішньовенні |
Повторювані венозні крововиливи та пошкодження судинної стінки можуть спричиняти тромбоз судин |
Введення катетера або інше в/в втручання має проводитися в анатомічно зручному як для пацієнта, так і для медичного персоналу місці. За даними літератури, частіше проблеми виникають при катетеризації вени тильної сторони долонь та стоп, гомілки, ліктьової ямки, біля суглобів та в інших місцях [2–4]. Несвоєчасне виявлення екстравазацій можливе, якщо місце введення буде чимось приховане. Введення рідини під тиском або ж у обмежений простір також може призвести до виходу її у позасудинний простір і, таким чином, сприяти виникненню екстравазації. Ризик розвитку токсичних флебітів та екстравазацій хіміопрепаратів залежить також від засобів, які використовуються для інфузії: в/в катетери для постановки у периферичні (ПВВК) або центральні вени; імплантовані інфузійні системи венозного доступу (порти). Встановлення в/в катетера дозволяє не тільки зменшити кількість втручань у вену, а й допомагає шляхом адекватного підбору місця введення і розміру катетера безпечно ввести цитотоксичні препарати. Різноманіття існуючих фіксованих катетерів дозволяє підібрати зручний і відповідний біологічним властивостям вен екземпляр. Встановлення катетера металевого типу «метелик» у 2 рази частіше супроводжується ускладненнями, ніж тефлонового катетера [5]. Менший за діаметром та довжиною катетер є менш травматичним. Це пов’язано з фізичними властивостями капілярів: чим менший і коротший капіляр, тим більший опір, а отже менший потік рідини через нього. Використання катетера нерозривно пов’язане з венепункцією, стінка стає більш ламкою, а отже високий тиск (вищий ніж всередині вени) може спричинити вихід рідини за межі вени через ушкоджені місця.
На розвиток екстравазацій також може впливати швидкість інфузії, яку необхідно обрати відповідно до пропускної здатності вени, загального об’єму інфузії, особливо при одночасному введенні декількох розчинів [6]. Цитостатики повинна вводити лише досвідчена та компетентна медична сестра, обізнана з токсичними ефектами ХТ та правилами надання екстреної медичної допомоги. Інфузійний розчин слід готувати лише за правилами, вказаними виробником. Для досягнення якісної роботи медичного персоналу потрібне постійне його навчання, створення відповідних правил роботи.
Токсичні флебіти розвиваються у 12–15% інфузій. Згідно з дослідженнями, проведеними S. Ikeda та співавторами (2004), частіше токсичні флебіти розвиваються внаслідок лікування цитарабіном, доксорубіцином, епірубіцином, дакарбазином та таксанами. Частота токсичних флебітів прямо пропорційна кількості введень препаратів та концентрації хіміопрепарату в розчині [7].
Клінічно токсичний флебіт має практично схожий перебіг з іншими типами флебітів. Сильний біль за ходом вени під час введення хіміопрепарату, почервоніння, набряк шкіри над веною, набряк дистальних відділів кінцівки.
Як зазначається у дослідженні M. Nassaji-Zavareh та співавторів (2007), лікування їх в основному консервативне [8]. Більшість дій, спрямованих на максимальне зменшення ступеня прояву токсичного флебіту, належать до немедикаментозних заходів (негайна зупинка інфузії, оцінка місця ушкодження, перевірка зворотнього току крові, роз’яснення пацієнту, що трапилося, зміна катетера, приведення руки у підвищене положення, систематичний огляд місця ушкодження). Із медикаментозних засобів застосовуються знеболюючі, антигістамінні засоби, системно та місцево — нестероїдні протизапальні засоби, антикоагулянти (гепарин, низькомолекулярні гепарини), препарати, що покращують реологію крові та трофіку венозної стінки. За спостереженнями цих самих авторів, лікування триває від 14 днів до 1–2 міс.
Наслідками або ж супутніми явищами токсичного флебіту є тромбоз, обтурація просвіту судини з можливою наступною тромбоемболією, косметичний дефект.
Екстравазації виникають при потраплянні медикаментів під час в/в їх введення у навколишні тканини з центральної або периферичної вени або катетера. Екстравазація — не дуже рідкісне явище. За даними популяційного дослідження, опублікованого R.A. Ener та співавторами (2004), частота цього явища досягає 0,1–6% серед усіх пацієнтів, що отримують в/в лікування. Удітей ці ускладнення досягають 58% в/в втручань, 5–10% — у пацієнтів, які отримують лікування цитостатичними препаратами [9]. Проте на практиці цей відсоток виявляється більшим, адже левова частка цих випадків не документується [10].
Як зазначається у дослідженні О. Dougherty (2008), на етапі оцінки серйозності події надзвичайно важливо відрізнити екстравазацію хіміопрепаратів від місцевої алергічної реакції, що найчастіше відбувається при введенні антрациклінів [9]. Як правило, остання проявляється у вигляді кропивниці та гіперемії за ходом або навколо вени, що не завжди супроводжується болем, набряком та втратою зворотного току крові, та зникає приблизно через 30–60 хв після появи.
Результати екстравазації хіміопрепаратів можуть мати різний ступінь тяжкості: від короткотривалих, легких (дискомфорт, гіперемія), до утворення везикул, ерозій, ослаблення венозного відтоку. Якщо екстравазація сталася, вона може тривати протягом декількох місяців, вражати нерви, сухожилля і суглоби. У разі несвоєчасно розпочатого лікування, як зазначається у публікаціях E. Kassner (2000), S. Mullin та співавторів (2000), подальша тактика може потребувати хірургічного втручання (пересадки шкіри або навіть ампутації) [11, 12].
Наслідки екстравазації цитотоксичних агентів залежать від класу цих речовин (табл. 2). Згідно з наведеною класифікацією препарати групи низького ризику — нейтральні, запальні та іританти (група А) — призводять до м’яких подразнюючих короткотривалих ушкоджень, які самостійно проходять [13]. Тоді як ексфоліанти та везиканти (групи В і С) належать до груп високого ризику. Їх екстравазації призводять до тяжчих наслідків, що супроводжуються серйозним ураженням навколишніх тканин.
Таблиця 2. Класифікація цитотоксичних агентів залежно від їх потенційної ушкоджуючої дії
|
Нейтральні речовини |
Ірританти |
Ексфоліанти |
Везиканти |
|---|---|---|---|
|
Аспарагіназа |
Карбоплатин |
Цисплатин |
Кармустин |
|
Блеоміцин |
Іринотекан |
Доцетаксел |
Дакарбазин |
|
Кладрибін |
Тенипозид |
Доксорубіцин ліпосомальний |
Доксорубіцин |
|
Циклофосфамід |
Етопозид |
Мітоксантрон |
Епірубіцин |
|
Цитарабін |
5-Фторурацил |
Оксаліплатин |
Ідарубіцин |
|
Флударабін |
Метотрексат |
Топотекан |
Мітоміцин |
|
Гемцитабін |
Паклітаксел |
||
|
Іфосфамід |
Вінбластин |
||
|
Мелфалан |
Вінкрістин |
||
|
Ритуксимаб |
Вінорельбін |
||
|
Тіотепа |
При потраплянні великої кількості агента за межі судини виникає некроз, який може поглиблюватися протягом кількох днів. Це пов’язано з пошкодженням ДНК клітин як у момент потрапляння хіміотерапевтичних препаратів за межі судини, так і при подальшому їх перебуванні у тканинах. Повільне загоєння виразок при екстравазації також обумовлене пошкодженою структурою ДНК. Виникає болісне виразкування з червоними підритими краями, що загоюється струпом. Близько однієї третини всіх екстравазацій завершуються таким чином.
Зворотня реакція на екстравазацію хіміопрепаратів виникає на місці попередньої екстравазації при утворенні нової в іншій ділянці і може варіювати від еритеми до виразкування (часто при екстравазації паклітакселу).
Зважаючи на патогенез екстравазацій, пильність та своєчасність у розпізнаванні та лікуванні екстравазацій хіміопрепаратів відіграють головну роль у обмеженні ушкодження тканин. Основний спосіб ведення пацієнтів з екстравазаціями консервативний. Проте при будь-якому варіанті перебігу екстравазації необхідна консультація хірурга щодо раннього хірургічного лікування [9].
Запідозрити екстравазацію периферичної вени можна за наявності будь-якого з наступних проявів: біль різної інтенсивності, як правило пекучий, почервоніння, набряк, виникнення пухирців навколо катетера (останнє свідчить про часткове ураження прошарків шкіри), пігментація шкіри, індурація, підтікання в місці встановлення катетера, відсутність зворотного току крові через катетер, резистентність поршня під час болюсного введення препаратів, відсутність самостійного току під час проведення інфузії. Екстравазації центральних вен мають тенденцію до більш тяжкого перебігу за рахунок більш складної діагностики та потрапляння більшої кількості рідини за межі вени. Симптомами екстравазації центральної вени є: лихоманка, біль або дискомфорт у плечі та шиї, біль та печіння, набряк грудної стінки, жорстокий плевральний біль, підтікання в місці встановлення катетера, некроз шкіри, можливе розширення тіні середостіння при рентгенографії.
Тактика лікування екстравазацій хіміопрепаратів залежить від індивідуального перебігу. Нагляд можуть здійснювати спеціалісти від медичної сестри до пластичного хірурга та анестезіолога. Особливу увагу слід звертати на знеболення та профілактику інфекцій [13]. Окрема роль, за рекомендаціями групи North Trent Cancer Network, відводиться знеболенню, яке має надзвичайне значення для пацієнта. Воно забезпечує можливість дотримання та виконання усіх призначень лікарів, позитивне ставлення до дій медичного персоналу з боку пацієнта, уникнення зайвого стресу для організму [14]. Цією групою приділено увагу в/ш, п/ш та місцевому застосуванню кортикостероїдів, що допомагає зменшити місцеве запалення.
При екстравазації препаратів групи А лікування розпочинається із застосування холоду/тепла (тільки для вінка-алкалоїдів) по 20 хв 4 рази на добу впродовж 3 днів, не допускаючи безпосереднього контакту зі шкірою, якщо пацієнт має місцеві прояви. Так, за даними T.V. Goolsby та співавторів (2006), стрибкоподібне місцеве охолодження без іншої терапії має ефективність 89% у профілактиці виразкування [15]. Кінцівці надається підвищене положення впродовж 48 год, рухи кінцівкою мають бути обережними. За наявності місцевих симптомів використовують 1% мазь гідрокортизону. Як правило, це єдине необхідне лікування. Медикаментозна підтримка потрібна завжди при екстравазації великого об’єму рідини. У такому випадку згідно з розробленими алгоритмами тактика лікування екстравазації має здійснюватися відповідно до алгоритму лікування при екстравазації хіміопрепаратів групи C.
Для препаратів групи В необхідно додатково застосовувати медикаментозне лікування. Якщо шкіра інтактна (немає везикул), місцево аплікації розчину або крему з диметилсульфоксидом DMSO (антидот при екстравазації доксорубіцину, даунорубіцину, мітоміцину) або компреси з ним (з анальгетиками, кортикостероїдами) (наносяться квачиком) 4 рази на добу впродовж 14 днів. Залишити оброблену ділянку непокритою. Якщо наявні везикули, DMSO не застосовувати [14].
Значну увагу також приділяють застосуванню антидотів [14]. Для групи С необхідне ін’єкційне введення гіалуронідази S/C відповідно до полюсів компасу навколо площі ураження (128 ОД у 2 мл 0,9% хлориду натрію) до 14 днів [16]. Тіосульфат натрію рекомендований як антидот до мехлоретаміну, мустину, цисплатину. Використовують 1,6 мл 25% розчину цього препарату численними інстиляціями у та навколо місця екстравазації (п/ш та в/ш) [3].
Згідно з останніми дослідженнями при доксорубіцинових виразках використовують локальне введення гранулоцитарно-макрофагального фактору росту (ГМ-КСФ). Але тактика недостатньо вивчена і потребує подальшого дослідження. Це стосується використання піридоксину гідрохлориду для лікування екстравазацій мітоміцину [3]. Доведено успішне використання локального введення фізіологічного розчину на стадії розрішення екстравазації та з метою профілактики виразкування [3].
Матеріали та методи дослідження
Впродовж 2010 року у науково-дослідному відділі консервативних методів лікування Національного інституту раку вивчено розвиток токсичних флебітів на фоні ХТ та екстравазацій хіміопрепаратів у 604 хворих. Серед них 286 чоловіків та 318 жінок віком від 18 до 82 років (медіана віку 47 років) (рис. 1).
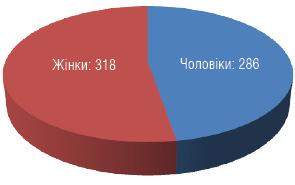
Враховувалися клінічні прояви та результати лабораторно-інструментальних методів дослідження (проводили сонографічне обстеження ушкодженої вени, консультація хірурга). Оцінювали фактори ризику розвитку токсичних флебітів та екстравазацій. Було враховано ступені проявів місцевої токсичності ПХТ за шкалою NCI-CNC V.4.0., час виникнення (кількість циклів ПХТ), тривалість ускладнення, вплив на інтенсивність терапії.
Результати та їх обговорення
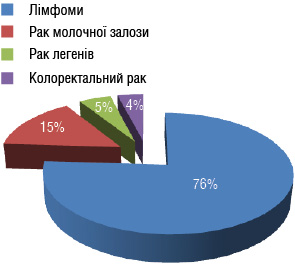
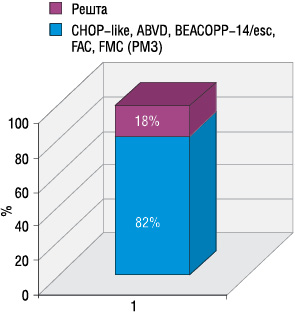
Найбільшу частину пролікованих становили пацієнти з лімфомами (76%), хворі на рак грудної залози (15%), рак легенів (5%) та колоректальний рак (4%). Сумарно хворим проведено 2840 курсів ХТ, від 1 до 9 курсів (в середньому 4,7 курси кожному пацієнту). Найбільшу частину (82%) становили СНОР-подібні схеми, ABVD, BEACOPP-14/ескальований, FAC, FMC (рис. 2, 3).
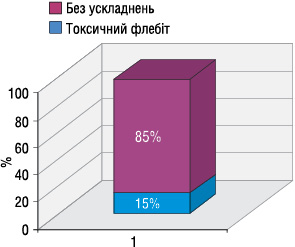
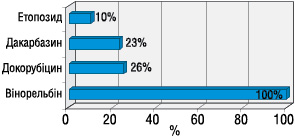
Розвиток токсичних флебітів відзначали у 90 хворих (15%) (рис. 4). Токсичні флебіти виникали уже після 1 курсу ХТ, та їх кількість збільшувалася з кількістю курсів ХТ: після 1-го курсу розвиток даного ускладнення відбувся у 22 хворих, а після 6-го курсу — у 64 хворих. Усі епізоди розвитку токсичного флебіту мали ІІ ступінь тяжкості (рис. 5). Серед курсів ХТ з вінорельбіном токсичні флебіти виникали у 100%, докорубіцином — у 25%, дакарбазином — у 23%, етопозидом — у 10% (рис. 6). У разі виникнення токсичного флебіту застосовували консервативні методи лікування. Консультація суміжних спеціалістів не проводилася у зв’язку з легким та помірним ступенем розвитку даного ускладнення. Лікування токсичних флебітів проводили з використанням нестероїдних протизапальних засобів (НПЗЗ), антиагрегантів, знеболювальних препаратів, місцево наносили гепаринові та мазі з НПЗЗ. Процес репарації тривав від 30 до 64 днів (у середньому — 41 день). Залишкові зміни у вигляді індурації стінки вени виявлено лише при вінорельбінових флебітах. В усіх випадках виникнення токсичного флебіту не впливало на подальшу терапію основного захворювання.

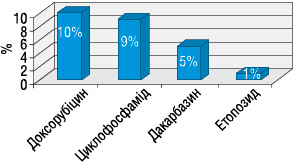
Екстравазації хіміопрепаратів зареєстровано у 12 хворих (2%) (рис. 7). Виникнення екстравазацій частіше відбувалося після 4–7-го курсів ХТ. У 6 з цих хворих розвиток даного ускладнення призвів до зниження інтенсивності ХТ шляхом редукції дози або подовження інтервалу між курсами. Після курсів з доксорубіцином екстравазації хіміопрепаратів виникали у 10%, циклофосфамідом — у 9%, дакарбазином — у 5%, етопозидом — у 1% (рис. 8). В 1 випадку спостерігали екстравазацію вінкристину. У 74% хворих зареєстровано екстравазації ІІ ступеня. У 25% хворих екстравазації хіміопрепаратів супроводжувалися порушенням шкірного покриву (рис. 9), серед яких 24% мали ІІІ ступінь та 1 пацієнтка мала IV ступінь екстравазації (рис. 10).
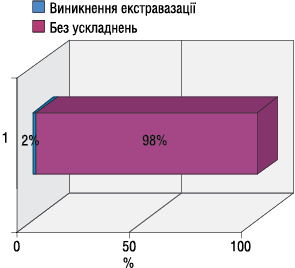
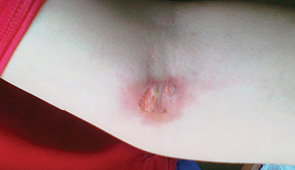
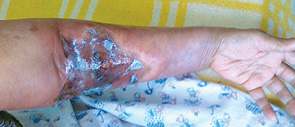
Для лікування застосовували введення знеболювальних та антигістамінних препаратів: місцево — 1% мазь гідрокортизону при збереженні цілісності шкірних покривів, аплікації 25–50% розчину димексиду та компреси з ним. Процес репарації тривав у середньому 76 днів (від 40 до 156 днів). У 44% хворих він завершився повним одужанням (рис. 11, 12).
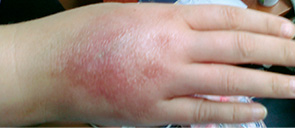
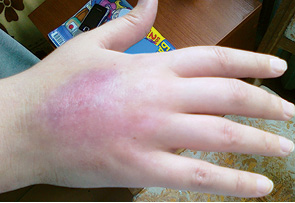
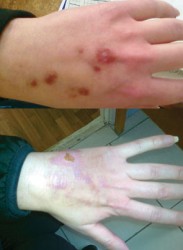
Таким чином, токсичні флебіти є менш тяжким ускладненням ХТ, ніж екстравазації. Поява токсичних флебітів може спостерігатися вже після 1-го курсу ХТ. Кількість цих ускладнень збільшується зі збільшенням кількості курсів ХТ. Препарати, що найчастіше їх викликають — це вінорельбін, доксорубіцин, дакарбазин, етопозид. Причому введення вінорельбіну у 100% випадків призводить до виникнення токсичного флебіту. Лікування їх в цілому консервативне. Залишкові зміни у вигляді індурації стінки вени виявлено лише при вінорельбінових флебітах. Виникнення токсичного флебіту не впливало на подальшу терапію основного захворювання. Екстравазації є більш серйозним ускладненням, що можуть призвести до тяжких наслідків: порушення інтенсивності терапії основного захворювання, нанесення шкоди здоров’ю пацієнта. Вони вимагають додаткових фінансових затрат на терапію, допомоги суміжних спеціалістів, призводять до погіршення якості життя пацієнтів та функціонування їх органів та систем. Найчастіше розвиток екстравазацій відзначають при інфузіях доксорубіцину, циклофосфаміду, дакарбазину та етопозиду.
Висновки
Місцеві ускладнення ХТ (токсичні флебіти та екстравазації хіміопрепаратів) можуть призвести до досить серйозних наслідків (виразкування шкіри, стриктури м’язів, ампутації кінцівок).
Місцеві ускладнення ХТ призводять до зниження інтенсивності спеціального лікування, що може спричинити прогресування хвороби.
Виникнення даних ускладнень погіршує якість життя онкохворих.
Розвиток токсичних флебітів та екстравазацій хіміопрепаратів вимагає додаткових фінансових витрат на їх лікування.
Дотримання правил профілактики та вчасно розпочате адекватне лікування токсичних ускладнень дозволяють уникнути їх розвитку та попередити подальше поглиблення ступеня токсичних флебітів та екстравазацій хіміопрепаратів.
Література
1. Wengström Y., Margulies A. (2008) European Oncology Nursing Society extravasation guidelines. Eur J Oncol Nurs. 12(4): 357–61.
2. Sauerland C., Engelking C., Wickham R., Corbi D. (2006) Vesicant extravasation part I: Mechanisms, pathogenesis, and nursing care to reduce risk. Oncol Nurs Forum. Nov 27, 33(6): 1134–41. Review.
3. Wickham R., Engelking C., Sauerland C., Corbi D. (2006) Vesicant extravasation part II: Evidence-based management and continuing controversies. Oncol Nurs Forum. Nov 27, 33(6): 1143–50. Review.
4. Corrigan A., Pelletier G., Alexander M. (Eds.) (2000) Core Curriculum for Intravenous Nursing. 2 edition. Philadelphia, PA: Lippincott.
5. Mukai H., Katsumata N., Ishii K., Ozawa K. et al., (2001) Flexible Intravenous (IV) Catheter Should Be Used for a Chemotherapeutic IV Device to Prevent Drug Extravasation, J Clin Oncol, 24(6): 768–771.
6. Kagel E.M., Rayan G.M. (2004) Intravenous catheter complications in the hand and forearm. J Trauma, 56: 123–7.
7. Ikeda S., Douchi T., Nagata Y. (2004) Effective prevention of chemotherapy — induced phlebitis by low-dose heparin: A prospective randomised trial. Ann Oncol, jun, 16(7): 942–45.
8. Nassaji-Zavareh M., Ghorbani R. (2007) Peripheral intravenous catheter-related phlebitis and related risk factors. Singapore Med J, 48: 733–6.
9. Ener R.A., Meglathery S.B., Styler M. (2004) Extravasation of systemic hemato-oncological therapies. Ann Oncol. Jun, 15(6): 858–62.
10. Dougherty (2008). IV therapy: recognising the difference between infiltration and extravasation British Journal of Nursing, 17(14): 896–901.
11. Kassner E. (2000) Evaluation and treatment of chemotherapy extravasation injuries, Journal of Paediatric Oncology, 24: 24–28.
12. Mullin S. et al. (2000) Prevention and management of antineoplastic extravasation injury, Hospital Pharmacy, 35: 57–74.
13. Mader I. et al. (2006) Extravasation of cytotoxic agents. Infect Control., 34: 308–12.
14. Extravasation guidlines North Trent Cancer Network Approved: 13.11.2008 To be reviewed by: Extravasation Sub-Group from North Trent Haemato-Oncology Nurse Group and the Pharmacist Group.
15. Goolsby T.V., Lombardo F.A. (2006) Extravasation of chemotherapeutic agents: prevention and treatment. Semin Oncol. Feb., 33(1): 139–43. Review.
16. Disa Joseph J., Chang Raymond R., Mucci Samuel J. and Nelson H. (2005) Goldberg Prevention of Adriamycin-Induced Full-Thickness Skin Loss Using Hyaluronidase Infiltration. New Engl J Med., 15: 987–993.
Местные осложнения химиотерапии: токсические флебиты и экстравазации
Национальный институт рака, Киев
Резюме. В статье представлен обзор литературы, посвященный развитию, диагностике и лечению токсических флебитов и экстравазаций химиопрепаратов, а также продемонстрирован собственный опыт в изучении данных осложнений. Выявлено, что местные осложнения химиотерапии являются достаточно частыми (до 15%) и серьезными осложнениями лечения, развитие которых может приводить к снижению эдиктивности химиотерапии и требовать активного лечения и профилактики.
злокачественные опухоли, токсический флебит, экстравазация химиопрепаратов, химиотерапия, лечение.














Leave a comment