Екстрена гастректомія з пластикою голодною кишкою під час операції Льюїса через ішемію культі шлунка: опис клінічного випадку
Лукашенко А.В., Кулай А.А., Нагорний А.В., Віноградова М.О.
Резюме. Рак стравоходу є досить поширеним захворюванням, що потребує комплексного підходу до лікування. Хірургічне лікування кардіоезофагіального новоутворення залишається стандартом. Проте при виконанні оперативного втручання трапляються інтраопераційні ускладнення, які потребують негайного ухвалення рішень. Цей клінічний випадок демонструє тактику при виявленні ішемії культі шлунка під час операції Льюїса. Не існує уніфікованих протоколів обсягу резекції та методів реконструкції при виявленні такого стану. Метою цього дослідження є представлення клінічного випадку успішного лікування раку стравоходу з переходом на кардіальний відділ шлунка з інтраопераційним виявленням нежиттєдіяльності культі шлунка при операції Льюїса. Висновки. Гастректомія з пластикою стравоходу голодною кишкою може бути використана у деяких пацієнтів при ішемії культі шлунка під час операції Льюїса.
Одержано 24.11.2025
Прийнято до друку 28.11.2025
DOI: 10.32471/clinicaloncology.2663-466X.35319
ВСТУП
Рак стравоходу посідає 11-те місце у світі щодо виявлення нових випадків та 7-ме місце за смертністю серед онкологічних захворювань, у 2022 р. діагностовано 511 054 нових випадки захворюваності на рак стравоходу [1]. За світовими даними (GLOBOCAN, 2022), аденокарцинома стравоходу становить 55% усіх випадків, тоді як в Україні переважає плоскоклітинна карцинома — 63,6% [2]. Згідно з міжнародними стандартами однією зі схем лікування хворих на аденокарциному нижньої третини стравоходу з поширенням на кардіальний відділ шлунка II стадії є проведення діагностичної лапароскопії, неоад’ювантної терапії. Радикальний обсяг оперативного лікування при відповіді пухлини на хімієтерапію зазвичай полягає у виконанні операції Льюїса [3] та проведенні ад’ювантної терапії [4]. На жаль, на будь-якому з цих етапів лікування можуть викинути ускладнення [5, 6]. У цьому клінічному випадку ми представляємо наш досвід боротьби з інтраопераційним ускладненням під час операції Льюїса. Одним з відомих, але нечастих ускладнень є ішемія культі шлунка, що виникає у 2–10% випадків і повʼязана з технічними помилками під час мобілізації шлунка [7]. Цей клінічний випадок свідчить про можливість такого ускладнення у пацієнтів з попередньо оперованим шлунком, коли протокол первинної операції недоступний. Виявлення стану ішемії культі шлунка потребує від операційної бригади негайного ухвалення рішення про зміну обсягу оперативного втручання з урахуванням онкологічних, хірургічних принципів, анатомічних особливостей та забезпечення найвищої якості життя пацієнта для вибору методу реконструкції.
Матеріали і методи дослідження. Хірургічне втручання виконане в умовах Державного некомерційного підприємства «Національний інститут раку» (Київ) за участі мультидисциплінарної хірургічної команди.
КЛІНІЧНИЙ ВИПАДОК
До клініки звернувся чоловік С., 52 роки, зі скаргами на дисфагію І ступеня, зменшенням маси тіла на 3 кг за останній місяць. Супутні захворювання: ішемічна хвороба серця. Фіксована хіатальна кила. Помірна рубцева деформація цибулини дванадцятипалої кишки зі звуженням просвіту та формуванням хибного дивертикулу. Еритематозна дуоденопатія. ASA I. З анамнезу відомо, що у 1989 р. проведено лапаротомію, ушивання перфоративної виразки шлунка. Спадковий анамнез не обтяжений.
За результатами езофагогастродуоденоскопії з біопсією верифіковано діагноз: аденокарцинома G1. Zivert I–II.
Антропометричні та клінічні дані: зріст — 167 см, маса тіла — 82 кг, індекс маси тіла (ІМТ) — 29,4, артеріальний тиск — 124/73 мм рт.ст., пульс — 78 уд./хв.
Обстеження та планування лікування. Лабораторні показники без клінічно значущих відхилень. Радіологічні дані, комп’ютерна томографія органів підтвердили наявність потовщення стінок нижньої третини стравоходу та кардіального відділу шлунка до 31 мм (рис. 1).
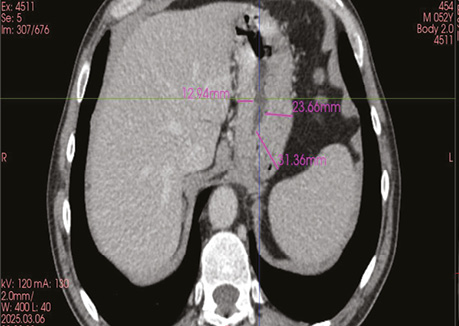
Рис. 1. Радіологічні дані локалізації первинної пухлини
Згідно з класифікацією TNM (T — tumor, «пухлина»; N — nodus, «вузол»; M — metastasis, «метастази») Американського об’єднаного комітету з боротьби проти раку (American Joint Committee on Cancer — AJCC, 8-ме видання) — стадія IІ, cT3N0M0.
Перед початком лікування проведено діагностичну лапароскопію та виключено наявність метастатичного ураження в черевній порожнині (рис. 2).
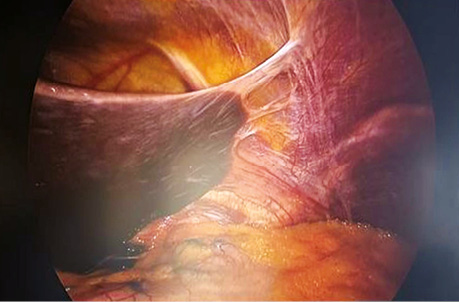
Рис. 2. Інтраопераційне фото черевної порожнини при діагностичній лапароскопії
Мультидисциплінарною комісією ухвалено рішення про призначення 4 курсів неоад’ювантної терапії за схемою FLOT, радіологічний та ендоскопічний контроль після проходження курсів неоад’ювантної терапії з ухваленням подальшої тактики лікування.
Передопераційну хімієтерапію хворий переніс задовільно. Ефект хімієтерапії — частковий регрес (стоншення стінок на 41%) (рис. 3).
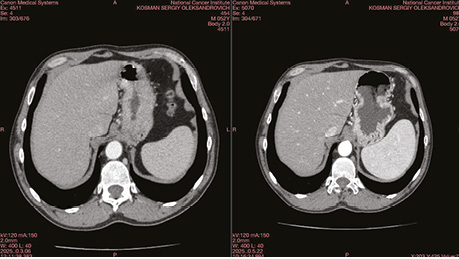
Рис. 3. Радіологічний ефект після проведення 4 курсів неоад’ювантної хімієтерапії
При повторному винесенні на мультидисциплінарну комісію було ухвалено рішення про проведення радикального обсягу оперативного лікування — операції Льюїса.
Хірургічне втручання. У положенні пацієнта на спині, під комбінованою анестезією, що включала ендотрахеальну анестезію (з інтубацією трахеї) та епідуральну анестезію, за Хассоном параумбілікально встановлено оптичний троакар 10 мм. При ревізії — даних за вторинне ураження не виявлено. Типово, зі збереженням онкологічних принципів скелетизовано проксимальні 2/3 шлунка з пересіченням лівих шлункових, шлунково-сальникових судин та коротких шлункових судин. Лінійними зшиваючими апаратами відсічено шлунок на 5 см, дистальніше за пухлину [8]. Пошарово ушиті рани. Накладено асептичну повʼязку. Хворого перевернуто в положення на лівий бік. По 5-му міжребер’ю виконано торакотомію. Мобілізовано нижню та середню третини стравоходу. Стравохід відсічено на 2 см, проксимальніше за пухлину [9]. Культю шлунка заведено в торакальну порожнину. Під час підготовки до накладання езофагогастроанастомозу при повторному візуальному дослідженні культі виявлено значний ціаноз культі. При тесті на капілярну кровотечу — кровопостачання незадовільне. Гіпотеза — порушення периферичного кровопостачання шлунка після попередньої операції через перфоративну виразку.
Ухвалено рішення про гастректомію з пластикою стравоходу голодною кишкою. За неможливості пластики голодною кишкою — пластика товстою кишкою [10]. Торакотомічну рану ушито. Накладено асептичну повʼязку.
Хворого перекладено на спину. Виконано мінілапаротомію. Остаточно мобілізовано та відсічено шлунок (рис. 4). Відсічено голодну кишку на відстані 20 см від звʼязки Трейца. Скелетизовано 10 см голодної кишки. Після 10 хв очікування — трансплантат життєздатний. Заведено в торакальну порожнину. Сформовано ентеро-ентероанастомоз. Накладено пошарові шви на рану. Хворого повторно перевернуто в положення на лівий бік. Виконано торакотомію по попередній рані. Сформовано езофагоюєноанастомоз кінець у бік [11] (рис. 5).
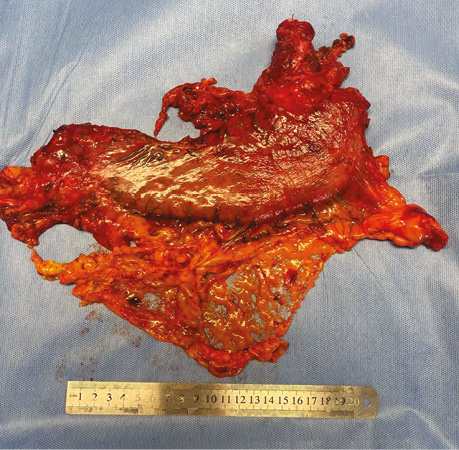
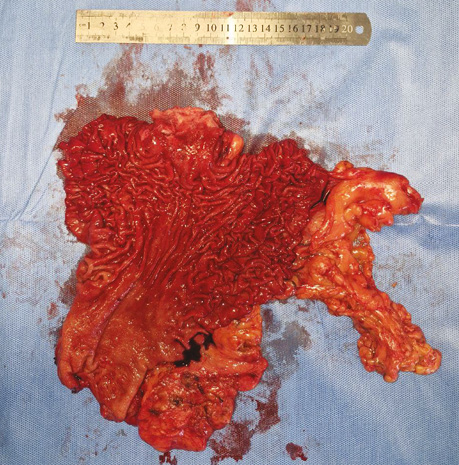
Рис. 4. Післяопераційний препарат
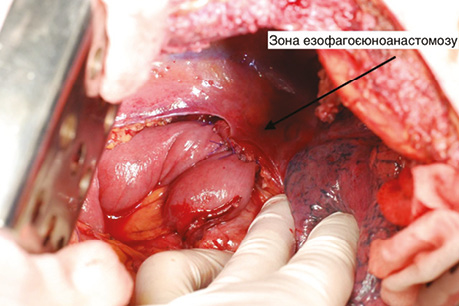
Рис. 5. Езофагоєюноанастомоз
Загальна тривалість операції — 420 хв, крововтрата — 150 мл.
Післяопераційний період пройшов без ускладнень.
Плевральний дренаж забрано на 3-тю післяопераційну добу після рентгенографії грудної клітки.
Абдомінальний дренаж видалено на 6-ту післяопераційну добу після контролю пасажу (рис. 6).
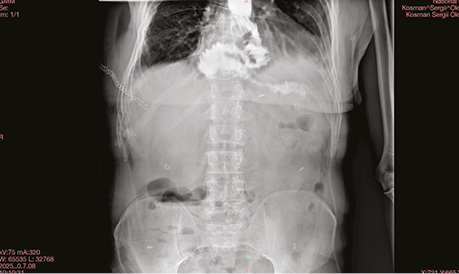
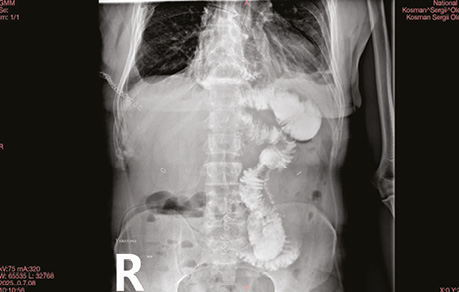
Рис. 6. Післяопераційне контрастне дослідження пасажу кишкового вмісту
На 9-ту післяопераційну добу хворого виписано в задовільному стані, лабораторні показники без клінічно значущих відхилень.
Обговорення: ішемія культі шлунка під час операції Льюїса завжди стає фактором, що кардинально змінює інтраопераційну тактику [12]. Цей випадок свідчить, що попередні операції на шлунку — це фактор ризику ішемії культі, який потребує підвищеної уваги під час мобілізації та фіксує можливість у таких випадках, якщо це анатомічно можливо, виконувати пластику нижньої та середньої третини стравоходу саме голодною кишкою [13], що, на відміну від пластики товстою кишкою, скорочує час оперативного втручання [14] та знижує ступінь тяжкості інтраопераційної травми, а також досить мʼяко впливає на післяопераційну якість життя, на відміну від формування стом.
ВИСНОВки
Гастректомію з пластикою стравоходу голодною кишкою може бути використано у деяких пацієнтів при ішемії культі шлунка під час операції Льюїса.
Згода та конфлікт інтересів. Отримано інформовану згоду. Автори заявляють про відсутність конфлікту інтересів.
СПИСОК ВИКОРИСТАНОЇ ЛІТЕРАТУРИ
1. Liu, C. Q., Ma, Y. L., Qin, Q., Wang, P. H., Luo, Y., Xu, P. F., & Cui, Y. (2023). Epidemiology of esophageal cancer in 2020 and projections to 2030 and 2040. Thoracic Cancer, 14(1), 3–11. doi: 10.1111/1759-7714.14745.
2. Global Cancer Observatory. Ukraine Fact Sheets (2022). Retrieved from: gco.iarc.fr/en.
3. Pennathur, A., Zhang, J., Chen, H., & Luketich, J. D. (2010). The «Best Operation» for Esophageal Cancer? Annals of Thoracic Surgery, 89(6), S2163–S2167. doi: 10.1016/j.athoracsur.2010.03.068.
4. Esophageal Cancer Treatment (PDQ®)—Health Professional Version. Retrieved from: http://www.cancer.gov/types/esophageal/hp/esophageal-treatment-pdq#_60.
5. Xu, Q. L., Li, H., Zhu, Y. J., & Xu, G. (2020). The treatments and postoperative complications of esophageal cancer: a review. Journal of Cardiothoracic Surgery, 15(1), 163. doi: 10.1186/s13019-020-01202-2.
6. Holakouie-Naieni, K., Mansournia, M. A., Doosti-Irani, A., Rahimi-Foroushani, A., & Haddad, P. (2021). Treatment-related complications in patients with esophageal cancer: A systematic review and network meta-analysis. Surgeon, 19(1), 37–48. doi: 10.1016/j.surge.2020.01.010.
7. Parekh, K., & Iannettoni, M. D. (2007). Complications of Esophageal Resection and Reconstruction. Seminars in Thoracic and Cardiovascular Surgery, 19(1), 79–88. doi: 10.1053/j.semtcvs.2006.11.002.
8. Tsai, W. S., Levy, R. M., & Luketich, J. D. (2009). Technique of Minimally Invasive Ivor Lewis Esophagectomy. General Thoracic Surgery, 14(3), 176–192. doi: 10.1053/j.optechstcvs.2009.06.002.
9. Reed, C. E. (2009). Technique of Open Ivor Lewis Esophagectomy. General Thoracic Surgery, 14(3), 160–175. doi: 10.1053/j.optechstcvs.2009.06.001.
10. Baldwin, D. L., Gonzalez, S. R., & Anand, S. (2025). Esophageal Reconstruction. Retrieved from: pubmed.ncbi.nlm.nih.gov/33232006.
11. Omori, T., Oyama, T., Mizutani, S., Tori, M., Nakajima, K., Akamatsu, H., … Nishida, T. (2009). A simple and safe technique for esophagojejunostomy using the hemidouble stapling technique in laparoscopy-assisted total gastrectomy. American Journal of Surgery, 197(1), e13-7. doi: 10.1016/j.amjsurg.2008.04.019.
12. Latzko, M., Ahmed, B., & Awad, Z. (2021). Minimally Invasive Ivor-Lewis Esophagectomy for Esophageal Cancer After Gastric Bypass. Annals of Surgical Oncology, 28(1), 203. doi: 10.1245/s10434-020-08646-9.
13. Roussel, E., Papet, E., Chati, R., Schwarz, L., Tuech, J. J., & Huet, E.(2023). When Gastroplasty Is Not Feasible in Ivor Lewis Esophagectomy: A Single-Center Study of Intrathoracic Esophagojejunostomy. Journal of Laparoendoscopic & Advanced Surgical Techniques, 33(11), 1102–1108. doi: 10.1089/lap.2023.0197.
14. Jiang, R., Wang, Y., Xu, J., Chen, Z., & Pang, L. (2023). Reconstruction using the colon or jejunum in patients with synchronous advanced esophageal and gastric cancers: a retrospective study from a single institutional database. BMC Surgery, 23(1), 175. doi: 10.1186/s12893-023-02072-w.
Адреса для листування:
Кулай Аліна Анатоліївна
03022, Київ, вул. Здановської Юлії, 33/43
Державне некомерційне підприємство «Національний інститут раку»
E-mail: alina.kulay@unci.org.ua
Correspondence:
Alina Kulay
33/43 Yulii Zdanovskoi str., Kyiv, 03022
Nonprofit Organization National Cancer Institute
E-mail: alina.kulay@unci.org.ua32.














Leave a comment