Гетерогенність нейробластом за вмістом у їхніх клітинах нуклеїнових кислот (попереднє спостереження)
Грабовий О.М., Зарецький М.Б., Климнюк Г.І.
Резюме. Нейробластома є однією з найбільш специфічних для дитячого віку солідних злоякісних пухлин з розвитком, що погано прогнозується. Проведені дослідження показали, що нейробластоми характеризуються значним різноманіттям клітинного складу. У ранжованому ряду клітин нейробластоми за ступенем кореляції між вмістом нуклеїнових кислот у їх ядрі та в цитоплазмі з високою достовірністю пухлини можуть бути поділені на 3 групи: І — з низьким (до 0,4), ІІ — із середнім (0,4-0,7) і ІІІ — високим (0,7-1) ступенем. Відсутність кореляції між середніми значеннями вмісту нуклеїнових кислот в ядрі та цитоплазмі клітин нейробластоми і широка мінливість ступеня кореляції між цими показниками у ранжованих за вмістом нуклеїнових кислот рядах у ядрах пухлинних клітин свідчать про наявність у нейробластомах різних морфофункціональних типів клітин. Отже, не тільки окремі ознаки (поліплоїдія тощо), а й ступінь зв’язку між певними ознаками може також виступати у якості критеріїв при оцінці властивостей нейробластом.
 Нейробластома є однією з найбільш специфічних для дитячого віку солідних злоякісних пухлин, яка зустрічається найчастіше, становить близько 8% й займає 6-те місце в структурі дитячої онкозахворюваності. Цей тип пухлин виявляють у середньому в кількості 8–10 випадків на 1 млн дитячого населення, найчастіше у дітей до 1 року та 2–4 років життя [4, 6, 7, 14]. Частота виявлення нейробластом при аутопсіях більш ніж у 400 разів перевищує кількість клінічно виявлених випадків, що вказує на спонтанну інволюцію більшості цих новоутворень [2, 3].
Нейробластома є однією з найбільш специфічних для дитячого віку солідних злоякісних пухлин, яка зустрічається найчастіше, становить близько 8% й займає 6-те місце в структурі дитячої онкозахворюваності. Цей тип пухлин виявляють у середньому в кількості 8–10 випадків на 1 млн дитячого населення, найчастіше у дітей до 1 року та 2–4 років життя [4, 6, 7, 14]. Частота виявлення нейробластом при аутопсіях більш ніж у 400 разів перевищує кількість клінічно виявлених випадків, що вказує на спонтанну інволюцію більшості цих новоутворень [2, 3].
Нейробластома належить до групи ембріональних пухлин, проте має ряд специфічних біологічних властивостей, не притаманних іншим злоякісним пухлинам [10, 11]:
1. Здатність до спонтанної регресії. Однак досі не виявлено жодного маркера, який визначає злам у перебігу захворювання від прогресування до регресії.
2. Здатність до диференціювання. Ця властивість була виявлена при дослідженні культури клітини, що вирощувалася з агресивної пухлини, яка доволі рідко (1:1150), проте переконливо набувала ознак диференціювання.
3. Властивість до стрімкого агресивного розвитку та бурхливого метастазування. Майже у 50% дітей, хворих на нейробластому, при надходженні в клініку спостерігаються метастази в кістковий мозок та кістки, лімфатичні вузли.
Нейробластоми, як й інші злоякісні пухлини, виникають завдяки накопиченню мутацій у критичних прото-онкогенах і генах-супресорах пухлинного росту. Відповідно до центральної догми молекулярної біології [12] реалізація спадкової інформації відбувається в ланцюзі ДНК→РНК→білок, що втілюється у певні ознаки. Множинні ж зміни у геномі при онкогенезі призводять до порушення багаточисленних внутрішньоклітинних процесів, які накладаються один на одний, що проявляється формуванням нового, «пухлинного» фенотипу з рядом характерних ознак. Слід також зазначити, що генетичні порушення, що призводять до виникнення пухлини, супроводжуються змінами молекулярних сигнальних каскадів, які є певною мірою специфічними для кожної конкретної пухлини та привносять унікальні додатки до загальних механізмів пухлинного росту [13] та до доповнення/збіднення фенотипу пухлини тими чи іншими ознаками. Розвиток новоутворення поступово призводить до набуття ним злоякісності та гетерогенності клітинного складу, виникає декілька субпопуляцій клітин, що відрізняються своїми біологічними властивостями, морфологією, імунофенотипом. Тому визначення у складі нейробластоми морфофункціональних груп клітин, які мають різні властивості, може дати підґрунтя для встановлення ступеня її злоякісності та прогнозування перебігу хвороби.
Мета роботи — оцінити гетерогенність клітинного складу нейробластом за пов’язаними морфофункціональними ознаками клітин та визначити принципову можливість їх використання для виявлення злоякісності пухлини та прогнозу розвитку захворювання.
Об’єкт та методи дослідження
Дослідження було проведено на матеріалі біопсій або вилученому при оперативному втручанні від 20 пацієнтів з нейробластомою. Гістологічне типування було проведено з використанням рутинного (гематоксилін і еозин) забарвлення та імуногістохімічного дослідження. Наявність метастазів, у тому числі й віддалених, спостерігалася у 8 пацієнтів, і за Міжнародною патологічною класифікацією нейробластом (INPC), 10 були віднесені до сприятливої й 10 до несприятливої форми.
Отриманий матеріал фіксували в забуференому 10% формаліні з pH 7,4 та ущільнювали у парафін із застосуванням гістіопроцесора Histos-5 (Milestone, Italy). З отриманих блоків виготовляли гістологічні зрізи товщиною 5 мкм за допомогою мікротома Microm НМ325 (Thermo scientific, Germany). Зрізи забарвлювали азур-ІІ-еозином для загальної оцінки пухлини та галоціанін-хромовим галуном за Ейнарсоном (pH 1,62, 37°С протягом 24 год) для виявлення вмісту нуклеїнових кислот (НК) у клітинах [5, 8]. Отримані препарати вивчали та фотографували за допомогою мікроскопа Nikon Eclipse 80i з камерою DS-5SMc та блоком контролю L2 за стандартизованих умов. Обробку цифрових зображень здійснювали за допомогою системи аналізу зображення Image J 1,4.
На препаратах, забарвлених за Ейнарсоном, у 30 клітинах кожної пухлини визначали: площу перетину ядра клітини (N area), питому оптичну щільність ядра клітини (N DM), інтегративну оптичну щільність ядра клітини (N IntDen), а також розраховували вміст НК на реконструйований об’єм ядра клітини пухлини (N Кооф НК) для екстраполяції результатів вимірювання у площині зрізу за формулою:
N Кооф НК = N IntDen * ¾* N area *√( N area/π) (1)
Для цитоплазми пухлинних клітин визначали: площу перетину цитоплазми клітини (С area), питому оптичну щільність цитоплазми клітини (С DM), інтегративну оптичну щільність цитоплазми клітини (С IntDen), вміст НК на реконструйований об’єм (за формулою, аналогічною 1) цитоплазми клітини (С Кооф НК). У якості вихідної точки відліку для оцінки вмісту НК використали показник, прийнятий за одиницю, притаманний ядрам лімфоцитів, що знаходилися у стромі пухлин. Для кожної окремої пухлини проведено попарний кореляційний аналіз між отриманими показниками.
Клітини кожної окремої пухлини були ранжировані за вмістом НК у ядрі. Отримана послідовність була поділена на інтервали із кроком, що дорівнював середньому вмісту НК у ядрах лімфоцитів. У межах кожного інтервалу визначали абсолютну кількість клітин, що відображують клітинний склад пухлин за вмістом у ядрах їх клітин НК. Для кожного інтервалу в спектрі складу клітин пухлини за вмістом НК у ядрах розрахували середні значення вмісту НК у ядрі (MN НК) та цитоплазмі (МC НК) та визначали кореляцію між цими показниками. За ступенем цієї кореляції між зазначеними показниками пухлини були розподілені на групи, достовірність відмінності яких визначалася за критерієм Фішера. У кожній виділеній групі нейробластом обчислювали середній вміст НК у ядрі пухлинних клітин.
Отримані результати зіставляли з клінічними даними (наявністю регіональних та віддалених метастазів) та оцінкою пухлин за INPC як зі сприятливою так і несприятливою гістопатологічною будовою [15, 16]. Для цього враховували: ступінь диференціації, наявність або відсутність шваннівської строми (багаті стромою, бідні стромою), мітотично-каріорексичний індекс (МКІ, індекс Шимади — кількість мітозів та каріорексисів на 5000 пухлинних клітин), нодулярну будову, вік хворого.
Отримані результати та їх обговорення
На препаратах, забарвлених за Ейнарсоном, для кожної з 30 клітин кожної пухлини визначали планіметричні та денсіометричні показники, зроблено перерахунок даних вимірювання оптичної щільності ядра та цитоплазми у площині зрізу на реконструйований об’єм ядра (за формулою 1). Середня оптична щільність ядер лімфоцитів була взята за одиницю вмісту НК в ядрах пухлинних клітин. У межах кожної окремої пухлини проведено попарний кореляційний аналіз між отриманими показниками, що визначалися (табл. 1).
Таблиця 1 Кореляція між парами морфометричних та денсіометричних показників стану ядер та цитоплазми клітин нейробластом (жирним шрифтом виділені високі значення кореляції між ознаками)
| № пухлини Кореляція | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | 19 | 20 |
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| N area-N DM | -0,16 | -0,45 | -0,7 | -0,25 | -0,44 | 0,02 | -0,04 | -0,18 | 0,35 | -0,37 | -0,54 | -0,15 | -0,3 | 0,03 | -0,31 | -0,61 | -0,36 | -0,11 | -0,35 | 0,16 |
| N area-N IntDen | 0,97 | 0,87 | 0,9 | 0,85 | 0,96 | 0,93 | 0,91 | 0,98 | 0,91 | 0,84 | 0,97 | 0,95 | 0,82 | 0,87 | 0,85 | 0,89 | 0,92 | 0,98 | 0,74 | 0,96 |
| N area-C area | 0,26 | 0,33 | 0,31 | 0,49 | 0,22 | 0,54 | 0,61 | 0,82 | -0,02 | 0,21 | 0,82 | 0,47 | 0,35 | 0,26 | 0,28 | 0,56 | -0,04 | 0,56 | 0,35 | 0,15 |
| N area-C DM | -0,09 | -0,14 | -0,14 | -0,37 | 0,26 | 0,19 | -0,13 | -0,2 | 0,21 | -0,06 | 0,02 | -0,01 | -0,26 | -0,1 | -0,11 | -0,3 | -0,3 | -0,22 | -0,26 | 0,13 |
| N area-C IntDen | 0,3 | 0,17 | 0,36 | 0,44 | 0,28 | 0,52 | 0,5 | 0,81 | 0,04 | 0,29 | 0,77 | 0,39 | -0,03 | 0,14 | 0,32 | 0,49 | 0,24 | 0,42 | 0,2 | 0,16 |
| N DM-N IntDen | 0,07 | 0,87 | -0,32 | 0,29 | -0,2 | 0,38 | 0,37 | 0 | 0,7 | 0,18 | -0,41 | 0,11 | 0,29 | 0,51 | 0,21 | -0,22 | 0,01 | 0,08 | 0,36 | 0,43 |
| N DM-C аrea | -0,18 | -0,27 | -0,21 | -0,23 | -0,11 | 0,22 | -0,36 | -0,31 | -0,23 | 0,16 | -0,56 | 0,14 | -0,13 | -0,01 | 0,22 | -0,17 | 0,33 | -0,2 | 0,36 | 0 |
| N DM-C DM | 0,47 | 0,49 | 0,16 | 0,37 | 0,13 | 0,34 | 0,49 | 0,22 | 0,53 | 0,52 | 0,22 | 0,55 | 0,76 | 0,43 | 0,16 | 0,56 | 0,82 | 0,74 | -0,26 | 0,55 |
| N DM-C IntDen | -0,03 | 0,12 | -0,22 | -0,01 | -0,07 | 0,28 | -0,02 | -0,28 | -0,1 | 0,42 | -0,53 | 0,27 | 0,5 | 0,14 | 0,28 | -0,12 | 0,5 | 0,07 | 0,51 | 0,4 |
| N IntDen-C аrea | 0,24 | 0,23 | 0,26 | 0,33 | 0,24 | 0,56 | 0,4 | 0,73 | -0,14 | 0,33 | 0,76 | 0,49 | 0,24 | 0,19 | 0,41 | 0,59 | 0,07 | 0,52 | 0,62 | 0,14 |
| N IntDen-C DM | 0 | 0,1 | -0,07 | -0,15 | 0,32 | 0,29 | 0,07 | -0,18 | 0,4 | 0,19 | 0,04 | 0,12 | 0,21 | 0,1 | -0,02 | -0,11 | -0,01 | -0,08 | 0,17 | 0,27 |
| N IntDen-C IntDen | 0,31 | 0,25 | 0,33 | 0,41 | 0,32 | 0,57 | 0,44 | 0,73 | -0,04 | 0,56 | 0,72 | 0,45 | 0,26 | 0,24 | 0,48 | 0,53 | 0,47 | 0,43 | 0,58 | 0,27 |
| C Area-C DM | -0,48 | -0,07 | -0,74 | -0,54 | 0,28 | 0,38 | -0,21 | -0,3 | -0,44 | -0,17 | 0,12 | 0,33 | -0,13 | -0,08 | -0,5 | -0,06 | 0,14 | -0,36 | 0,36 | -0,49 |
| C Area-C IntDen | 0,92 | 0,69 | 0,96 | 0,84 | 0,97 | 0,97 | 0,81 | 0,98 | 0,94 | 0,77 | 0,98 | 0,96 | 0,61 | 0,75 | 0,94 | 0,99 | 0,12 | 0,84 | 0,9 | 0,77 |
| C DM-C IntDen | -0,15 | 0,64 | -0,59 | -0,14 | 0,46 | 0,57 | 0,36 | -0,13 | -0,14 | 0,42 | 0,22 | 0,5 | 0,67 | 0,55 | -0,22 | 0,02 | 0,56 | 0,06 | 0,68 | 0,12 |
| N Кооф НК-C area | 0,1 | 0,27 | 0,29 | 0,38 | 0,22 | 0,54 | 0,46 | 0,78 | -0,13 | 0,31 | 0,82 | 0,46 | 0,31 | 0,21 | 0,4 | 0,65 | 0,02 | 0,53 | 0,58 | 0,15 |
| N Кооф НК-N area | 0,51 | 0,94 | 0,96 | 0,92 | 0,97 | 0,95 | 0,95 | 0,98 | 0,94 | 0,92 | 0,98 | 0,96 | 0,91 | 0,93 | 0,92 | 0,95 | 0,97 | 0,97 | 0,83 | 0,97 |
| N Кооф НК-C Кооф НК | 0,98 | 0,25 | 0,35 | 0,4 | 0,22 | 0,54 | 0,47 | 0,74 | -0,09 | 0,53 | 0,78 | 0,35 | 0,14 | 0,24 | 0,42 | 0,59 | 0,05 | 0,52 | 0,54 | 0,25 |
| C Кооф НК-C area | 0,1 | 0,8 | 0,98 | 0,92 | 0,97 | 0,99 | 0,92 | 0,97 | 0,97 | 0,87 | 0,98 | 0,96 | 0,77 | 0,85 | 0,98 | 0,99 | 1 | 0,92 | 0,91 | 0,93 |
N area — площа перетину ядра клітини; N DM — питома оптична щільність ядра клітини; N IntDen — інтегративна оптична щільність ядра клітини; N Кооф НК — вміст НК у перерахунку на реконструйований об’єм ядра клітини пухлини; С area — площа перетину цитоплазми клітини; С DM — питома оптична щільність цитоплазми клітини; С IntDen — інтегративна оптична щільність цитоплазми клітини; С Кооф НК — вміст НК у перерахунку на реконструйований об’єм цитоплазми клітини пухлини
Проведений аналіз показав, що у клітинах нейробластом існує стійкий кореляційний зв’язок між розмірами ядра та вмістом у ньому НК (N area-N IntDen, а також N Кооф НК-N area), що було виявлено в усіх досліджених пухлинах. Також високий коефіцієнт кореляції притаманний для площі цитоплазми клітин пухлини та вмісту у ній НК (C аrea-C IntDen). Однак із загальної закономірності зв’язків випадає № 11, коли у пухлині визначалися додатково високі індекси кореляції між іншими парами показників. Крім того, в № 8 і № 11 виявилася висока кореляція між площею ядер та цитоплазми (N area-C area), а в № 13 і № 17 спостерігається висока кореляція між питомими щільностями (за вмістом НК) ядра та цитоплазми (N DM-C DM). Пряма залежність між вмістом НК у ядрі та цитоплазмі клітин пухлини відсутня.
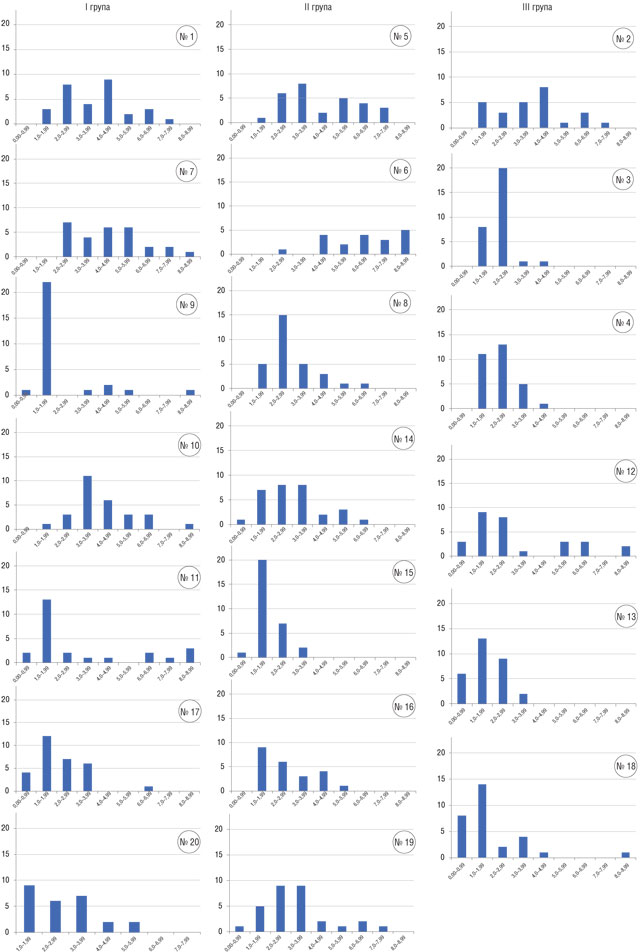
Виходячи з загального положення, що рак є генетичною хворобою і, відповідно, зміни клітини перш за все торкаються геному та ядра, а пухлинна прогресія веде до поліплоїдії [1, 9, 17], клітини кожної пухлини були ранжировані за вмістом НК у ядрі. Отримана послідовність була поділена на інтервали із кроком, що дорівнював одиниці (вміст НК у ядрі лімфоцита). У межах кожного інтервалу визначалася абсолютна кількість клітин. Побудовано гістограми, що відображають клітинну гетерогенність пухлин за вмістом у ядрах їх клітин НК (рисунок). Для кожного інтервалу в спектрі складу клітин пухлини за вмістом НК у ядрах визначені середні значення вмісту НК у ядрі (MN НК) та цитоплазмі (МC НК) клітин та кореляція між цими показниками (табл. 2).
Таблиця 2 Середні значення вмісту НК у ядрі (MN НК) та цитоплазмі (МC НК) клітин нейробластом, що були досліджені, для ранжованого ряду з кроком у одиницю (вміст НК у ядрі лімфоцита) та кореляція між зазначеними показниками
| № | Локалізація НК | Інтервал | Індекскореляції | ||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| 0,00–0,99 | 1,0–1,99 | 2,0–2,99 | 3,0–3,99 | 4,0–4,99 | 5,0–5,99 | 6,0–6,99 | 7,0–7,99 | 8,0–8,99 | |||
| 1 | MN НК | – | 1,5±0,3 | 2,3±0,2 | 3,6±0,2 | 4,4±0,1 | 5,4±0,0 | 6,5±0,2 | 7,0±0,0 | – | 0,31 |
| МC НК | – | 2,0±0,6 | 2,2±0,9 | 1,6±0,4 | 3,1±0,7 | 2,4±0,0 | 2,4±0,8 | 2,2±0,0 | – | ||
| 2 | MN НК | – | 1,6±0,1 | 2,4±0,1 | 3,6±0,0 | 4,9±0,0 | – | – | – | – | 0,76 |
| МC НК | – | 1,1±0,3 | 1,1±0,6 | 1,6±0,0 | 1,2±0,0 | – | – | – | – | ||
| 3 | MN НК | – | 1,8±0,1 | 2,5±0,1 | 3,4±0,1 | 4,1±0,0 | – | – | – | – | 0,69 |
| МC НК | – | 3,0±0,6 | 2,8±0,5 | 5,7±1,4 | 4,3±0,0 | – | – | – | – | ||
| 4 | MN НК | 0,9±0,0 | 1,5±0,1 | 2,3±0,1 | 3,1±0,1 | – | – | – | – | – | 0,92 |
| МC НК | 0,7±0,0 | 1,3±0,2 | 2,6±0,8 | 2,4±0,9 | – | – | – | – | – | ||
| 5 | MN НК | – | 1,6±0,0 | 2,4±0,1 | 3,3±0,1 | 4,4±0,1 | 5,4±0,1 | 6,3±0,1 | 7,2±0,1 | – | 0,64 |
| МC НК | – | 2,8±0,0 | 12,9±3,7 | 19,7±5,7 | 17±10,7 | 28±10,1 | 9,5±3,6 | 27,9±5,1 | – | ||
| 6 | MN НК | – | – | 2,4±0,0 | – | 4,5±0,1 | 5,4±0,1 | 6,5±0,1 | 7,1±0,1 | 8,3±0,1 | 0,4 |
| МC НК | – | – | 15,1±0,0 | – | 12,8±1,8 | 40±25 | 25,5±2,6 | 29,8±6,8 | 23,9±8 | ||
| 7 | MN НК | – | – | 2,5±0,1 | 3,6±0,1 | 4,6±0,1 | 5,4±0,2 | 6,3±0,3 | 7,4±0,3 | 8,5±0,0 | 0,38 |
| МC НК | – | – | 1,5±0,1 | 2,9±0,6 | 3,9±0,5 | 4,3±1,5 | 6±0,6 | 2,7±0,5 | 3,4±0,0 | ||
| 8 | MN НК | 0,5±0,0 | 1,6±0,1 | – | 3,4±0,0 | 4,8±0,1 | 5,5±0,0 | – | – | 8,8±0,0 | 0,59 |
| МC НК | 0,6±0,0 | 1,4±0,2 | – | 1,6±0,0 | 4,3±0,9 | 2,4±0,0 | – | – | 2,5±0,0 | ||
| 9 | MN НК | – | 1±0,1 | 2,5±0,1 | 3,3±0,0 | 4,7±0,1 | 5,2±0,0 | 6,2±0,0 | – | – | -0,38 |
| МC НК | – | 2,2±0,5 | 3,9±0,5 | 3,8±0,9 | 2,3±0,1 | 3,1±0,0 | 1,9±0,0 | – | – | ||
| 10 | MN НК | – | 1,9±0,0 | 2,2±0,1 | 3,6±0,1 | 4,3±0,1 | 5,5±0,2 | 6,1±0,1 | – | 8,5±0,0 | -0,38 |
| МC НК | – | 1,2±0,0 | 0,9±0,1 | 1,2±0,2 | 0,8±0,3 | 1,2±0,2 | 1,9±0,5 | – | 0,5±0,0 | ||
| 11 | MN НК | 0,3±0,1 | 1,4±0,1 | 2,0±0,0 | 3,8±0,0 | 4,2±0,0 | – | 6,8±0,1 | 7,7±0,0 | 8,6±0,1 | 0,38 |
| МC НК | 2,4±1,4 | 12±1 | 4,5±3,4 | 26,6±0,0 | 7,5±0,0 | – | 24,1±5 | 17,1±0,0 | 7,5±2,9 | ||
| 12 | MN НК | 0,6±0,1 | 1,4±0,1 | 2,5±0,1 | 3,2±0,0 | – | 5,7±0,0 | 6,4±0,1 | – | 8,3±0,3 | 0,84 |
| МC НК | 0,7±0,2 | 22±12 | 18±14 | 25,2±0,0 | – | 38±4,7 | 23±8,8 | – | 84±15 | ||
| 13 | MN НК | 0,8±0,1 | 1,7±0,1 | 2,3±0,1 | 3,2±0,2 | – | – | – | – | – | 0,72 |
| МC НК | 0,6±0,1 | 1,2±0,1 | 1,1±0,1 | 1,1±0,2 | – | – | – | – | – | ||
| 14 | MN НК | 0,7±0,0 | 1,6±0,1 | 2,5±0,1 | 3,4±0,1 | 4,4±0,1 | 5,7±0,2 | 6,0±0,0 | – | – | 0,61 |
| МC НК | 0,4±0,0 | 0,6±0,1 | 0,8±0,2 | 1,1±0,2 | 0,4±0,6 | 0,9±0,4 | 1,5±0,0 | – | – | ||
| 15 | MN НК | – | 1,3±0,1 | 2,5±0,1 | 3,7±0,2 | 4,6±0,1 | 5,5±0,1 | 6,2±0,0 | 7,0±0,0 | – | 0,54 |
| МC НК | – | 4,2±2,5 | 2,1±1,4 | 2,8±1,9 | 4,0±0,5 | 4,4±1,4 | 8,7±0,8 | 4,4±0,0 | – | ||
| 16 | MN НК | – | 1,6±0,1 | 2,5±0,1 | 3,4±0,1 | 4,8±0,1 | 5,3±0,0 | – | – | – | -0,51 |
| МC НК | – | 14±0,1 | 2,9±0,1 | 1,4±0,1 | 1,8±0,1 | 6,2±0,0 | – | – | – | ||
| 17 | MN НК | 0,8±0,1 | 1,5±0,1 | 2,4±0,1 | 3,5±0,1 | – | – | 6,3±0,0 | – | – | -0,06 |
| МC НК | 1,0±0,1 | 1,3±0,1 | 11,5±0,1 | 2,3±0,1 | – | – | 1,7±0,0 | – | – | ||
| 18 | MN НК | 0,6±0,1 | 1,4±0,1 | 2,3±0,1 | 3,2±0,1 | 4,2±0,0 | – | – | – | 8,3±0,0 | 0,82 |
| МC НК | 1,1±0,1 | 1,3±0,1 | 2,9±0,1 | 1,3±0,1 | 2,3±0,0 | – | – | – | 3,9±0,0 | ||
| 19 | MN НК | 0,9±0,0 | 1,5±0,1 | 2,5±0,1 | 3,4±0,1 | 4,5±0,4 | 5,3±0,0 | 6,4±0,3 | 7,1±0,0 | – | 0,63 |
| МC НК | 0,6±0,0 | 1±0,4 | 1±0,2 | 1,1±0,2 | 1,8±0,5 | 0,4±0,0 | 2±0,9 | 9,6±0,0 | – | ||
| 20 | MN НК | – | 1,4±0,0 | 2,4±0,1 | 3,6±0,1 | 4,7±0,1 | 5,4±0,2 | 6,6±0,1 | – | – | 0,08 |
| МC НК | – | 1,8±0,0 | 2,5±0,2 | 2,7±0,5 | 2,8±0,5 | 4,5±0,9 | 1,5±0,3 | – | – | ||
Аналіз отриманих даних кореляційних зв’язків між середніми значеннями вмісту НК у ядрі та цитоплазмі ранжованого ряду клітин пухлин дозволив за різним рівнем кореляції MN НК/МC НК серед них виділити 3 групи нейробластом: І — до 0,4 (низька); ІІ — 0,4–0,7 (середня); 0,7–1 (висока) (див. рисунок). Обчислення значення критерію Фішера для визначення достовірності між зазначеними групами нейробластом показав, що при порівнянні груп І і ІІ він дорівнює 86,5, що більше за табличне значення (6,16), та при порівнянні груп ІІ і ІІІ він дорівнює 7,1, що також більше за табличне значення (6,39). Отже, визначені групи нейробластом достовірно значимо відрізняються одна від одної.
Порівняння спектру пухлинних клітин у нейробластомах І, ІІ і ІІІ груп показує, що між ними є певні відмінності (див. рисунок). Так, у І групі пухлин клітинний склад характеризується переважанням клітин початкової та середньої частин спектру. У групі ІІ визначається тенденція до переважання у складі пухлин клітин з вмістом НК у ядрі середньої частини спектру. У ІІІ групі превалюють клітини початкової частини спектру. Середній вміст НК у ядрі клітин нейробластоми є найбільшим у ІІ групі, а найменшим — у ІІІ (табл. 3.). Це дає привід припустити, що зміни клітинного спектру нейробластом відображують стадію їх розвитку (пухлинної прогресії).
Таблиця 3 Деякі характеристики груп нейробластом, визначені за рівнем кореляції вмісту НК у ядрі та цитоплазмі пухлинних клітин, ранжованих за вмістом НК у ядрі
| Група | Кількість досліджених пухлин | Середній вміст НК у ядрі пухлинних клітин (умовні одиниці) | Кількість досліджених пухлин у групі з наявністю метастазів / % | Гістологічна група за INPC | |
|---|---|---|---|---|---|
| сприятлива | несприятлива | ||||
| I | 7 | 5,8±0,21 | 2 / 28 | 5 | 2 |
| II | 7 | 7,44±0,33 | 2 / 28 | 4 | 3 |
| III | 6 | 4,64±0,35 | 4 / 66 | 1 | 5 |
Зіставлення визначених груп нейробластом з клінічними даними та гістологічними типами згідно з INPC виявило також певні тенденції. Так, наявність метастазів, у тому числі й віддалених, найчастіше визначається у пацієнтів з пухлинами ІІІ групи, а відносна частка несприятливих гістологічних форм нейробластом збільшується у ряду І — ІІ — ІІІ груп (див. табл. 3.).
Таким чином, спостереження показали, що нейробластоми характеризуються значним різноманіттям клітинного складу. У ранжованому ряді клітин нейробластоми за ступенем кореляції між вмістом НК у їх ядрі та в цитоплазмі з високою достовірністю пухлини можуть бути поділені на 3 групи: І — з низьким (до 0,4), ІІ — із середнім (0,4–0,7) та ІІІ — високим (0,7–1) значенням цього показника. Відсутність кореляції між середніми значеннями вмісту НК в ядрі та цитоплазмі клітин нейробластоми (див. табл. 1) і широка мінливість ступеня кореляції між цими показниками у ранжованих за вмістом НК рядах у ядрах пухлинних клітин (див. табл. 2) свідчать про наявність у нейробластомах різних морфофункціональних типів клітин. Отже, не тільки окремі ознаки (поліплоїдія тощо), а й ступінь зв’язку між певними ознаками може також виступати у якості критеріїв при оцінці властивостей нейробластом. Звертає на себе увагу те, що в ІІІ групі досліджених нейробластом найчастіше зустрічаються випадки з наявністю метастазів, несприятливою гістологічною будовою пухлин та високим МКІ (див. табл. 3.). Це дає підставу припускати, що найбільш агресивними та з несприятливим прогнозом перебігу є пухлини ІІІ групи.
Привертає також увагу той факт, що у ІІІ групі нейробластом, яка включає найбільшу відносну кількість пухлин з метастазами та несприятливим гістологічним типом, клітини містять у середньому меншу кількість НК в ядрі в порівнянні як з ІІ, так і І групами (див. табл. 3.). Враховуючи доведений факт, що кількість ДНК у ядрах клітин новоутворень зростає у міру пухлинної прогресії [1, 9, 17], привертає прискіпливу увагу вміст РНК у клітинах нейробластоми. Слід зважати на те, що поділ клітин та виконання ними специфічних функцій умовно можна розглядати як антагоністичні стани. При цьому поділ клітин зазвичай супроводжується відповідно редукцією метаболічного апарату, в тому числі й білоксинтезувального (гранулярної ендоплазматичної сітки) та практичним припиненням синтезу РНК у ядрі. Виходячи з цього, вміст РНК в клітинах пухлини можна розглядати у якості критерію його метаболічної активності та рівня їхнього диференціювання. Можна припустити, що збільшення вмісту ДНК у ядрі з одночасним зменшенням кількості РНК як у ядрі, так і в цитоплазмі може виступати показником високої агресивності пухлини: зниження рівня диференціювання її клітин, зростання проліферативної активності та, можливо, інвазивного потенціалу нейробластоми.
Література
1. Автандилов Г.Г. (2002) Основы количественной и патологической анатомии. М.: Медицина: 240.
2. Детская гематология и онкология. (2005) Ланцковский Филип (пер. с англ. С.Шершаков). М.: Лори: 764.
3. Афанасьев Б.В., Балдуева И.А., Белогурова М.Б. и др. (2002) Детская онкология. Руководство для врачей. Под ред. М.Б. Белогуровой. СПб.: Спец. Лит.: 351
4. Ивановская Т.Е., Гусман Б.С. (1988) Патологическая анатомия болезней плода и ребенка. М.: Медицина: 298.
5. Лупа Х. (1980) Основы гистохимии. (Пер. с немец.). М : Мир: 344.
6. Оберзер А., Тайсен Д., Вестерман Ф. (2009) Характеристика и классификация нейробластом. Будущие онкологи, 5(5): 265–239.
7. Шалимов С.А., Гриневич Ю.А., Возианов А.Ф. и др. (2008) Справочник по онкологии. Под ред.: С.А. Шалимова, Ю.А. Гриневича, Д.В. Мясоедова. К.: Здоров’я: 576.
8. Ташке К. (1980) Введение в количественную цитогистологическую морфологию. (Пер. с рум.). М.: Из. Акад. Соц. Респ. Румынии: 192.
9. Bown N. (2001) Neuroblastoma tumour genetics: clinical and biological aspects. J Clin Pathol.: 54 (12): 897–910.
10. Brodeur G.M., Maris J.M. (2002) Neuroblastoma. Principles and Practice of Pediatric Oncology. Pfiladelphia: Lippincott Willians &Wilkins: 937.
11. Brodeur G.M. (2003) Neuroblastoma. Nature Rev Cancer.: 3: 203–216.
12. Crick F. (1970) Central dogma of molecular biologia. Nature: 227: 561–563.
13. Petricoin E.F., Bichesel V.E., Calvert V.S. et al. (2005) Mapping molecular networks using proteomics: a vision for patient-tailored combination therapy. Biochim. Biophys. Acta.: 23: 3614–3621.
14. Ross J.A., Severson R.K., Pollock B.H. et al. (1996) Childhood cancer in United States. A geographical analysis of cases from the Pediatric Cooperative Clinical Trials group. Cancer: 77: 201–207.
15. Shimada H., Ambros I.M., Dehner L.P. et al. (1999) Terminology and morphologic of with neuroblastic tumor: recommendations by the International Neuroblastoma Pathology Commititte. Cancer: 86: 349–363.
16. Shimada H., Ambros I.M., Dehner L.P. et al. (1999) The International Neuroblastoma Pathology Classification. Cancer: 86: 364–372.
17. Variend S., Burchill S.A. (2003) Neuroblastoma. Mol. biol. pathol. paediatr. cancer: 161–3.
Гетерогенность нейробластом по содержанию в их клетках нуклеиновых кислот (предварительные наблюдения)
Резюме. Нейробластома является одной из наиболее специфических злокачественных солидных опухолей детского возраста с плохо прогнозируемым развитием. Проведенные исследования показали, что нейробластомы характеризуются значительным разнообразием клеточного состава. В ранжированном ряде клеток нейробластомы по степени корреляции между содержанием нуклеиновых кислот в их ядре и цитоплазме опухоли с высокой достоверностью могут быть разделены на 3 группы: І — с низкой (до 0,4), ІІ — со средней (0,4–0,7) и ІІІ — высокой (0,7–1) степенью. Отсутствие корреляции между средними значениями содержания нуклеиновых кислот в ядре и цитоплазме клеток нейробластомы и широкая вариабельность степени корреляции между этими показателями в ранжированных по содержанию нуклеиновых кислот рядах в ядрах опухолевых клеток свидетельствует о наличии в нейробластомах различных морфофункциональных типов клеток. Таким образом, не только отдельные признаки (полиплоидия и др.), а и степень связи между признаками также может выступать в качестве критериев оценки свойств нейробластом.
нейробластома, клеточная гетерогенность, нуклеиновые кислоты.














Leave a comment