Нирково-клітинний рак
Результаты хирургического лечения раннего рака почки
А.В. Бондарев1, С.В. Ефетов1, В.В. Олексенко2, И.Н. Дыленок1, Т.Р. Джемилев1, К.А. Алиев2
1Отделение абдоминальной онкологии, Крымское республиканское учреждение «Онкологический клинический диспансер» имени В.М. Ефетова, Симферополь, Украина
2Кафедра онкологии, ГУ «Крымский государственный медицинский университет имени С.И. Георгиевского», Симферополь, Украина
В последние годы опубликованы многочисленные исследования ведущих отечественных и зарубежных клиник, свидетельствующие об одинаковой онкоспецифической эффективности радикальной нефрэктомии и резекции при раке почки в стадии Т1N0M0.
Цель работы — проанализировать опыт хирургического лечения больных ранним раком почки.
Анализу подвергнуты результаты лечения 50 пациентов с раком почки в стадии T1а, распределенные на две сопоставимые группы: основную — 30 (60%) больных, которым была выполнена резекция почки (21 — абдоминальным и 9 — люмботомическим доступом); контрольную — 20 (40%) пациентов, которым абдоминальным доступом произведена радикальная нефрэктомия.
Проведено сравнение основной и контрольной группы по возрасту (59,3±13,9 года против 57,6±12,2 года [p=0,41]), интраоперационной кровопотере (352,5±53,6 мл против 324,6±46,8 мл [p=0,25]), длительности операции (94,3±22,8 мин против 86,8±12,4 мин [р=0,19]), статусу ECOG (0,49±0,1 против 0,56±0,2 [p=0,22]), до- и послеоперационного уровня креатинина в крови (94,33±19,5 мкмоль/л против 96,24±19,9 мкмоль/л [p=0,20] и 121,91±16,2 мкмоль/л против 129,5±23,9 мкмоль/л [p=0,80]), продолжительности пребывания в стационаре (14,6±3,2 сут против 14,9±5,1 сут [p=0,92]).
Единственным статистически значимым отличием у исследуемых групп была разница в размере опухоли: основная группа — 30,8±6,2 мм, контрольная — 37,1±4,4 мм [р=0,009]. Летальных исходов в исследуемых группах не отмечено. У одного больного основной группы (p=0,51) в ранний послеоперационный период было кровотечение из зоны резекции, при котором потребовалась нефрэктомия, и у другого пациента развился мочевой затек, ликвидированный консервативными методами.
При раке почки в стадии T1a отдаленные результаты после выполнения органосохраняющей операции в объеме резекции сопоставимы с отдаленными результатами после радикальной нефрэктомии. Безрецидивный период наблюдения после резекции почки составил 16,3±8,9 мес, нефрэктомии — 17,7±8,2 мес (p=0,56).
Оцінка агресивності пухлин воріт нирки
Е.О. Стаховський, Ю.В. Вітрук, О.Е. Стаховський, О.А. Войленко, П.С. Вукалович, О.В. Буйвол
Відділення пластичної та реконструктивної онкоурології,
Національний інститут раку, Київ, Україна
Результати проведених досліджень, опубліковані в літературі, показали чітку залежність метастатичної хвороби від розміру пухлини нирки, а також асоціацію її розташування у воротах нирки із нижчими показниками безрецидивної виживаності, ніж при новоутвореннях іншої локалізації.
Метою нашого дослідження був порівняльний аналіз впливу локалізації пухлин нирки на виникнення клінічних проявів та можливість метастазування.
Проведено ретроспективний аналіз лікування 599 хворих із однобічною пухлиною нирки Т1 стадії. Вік пацієнтів коливався від 25 до 82 років (55,3±10,6). Чоловіків було 350 (58,4%), жінок — 249 (41,6%). Розміри пухлини в середньому становили 43,4±14,4 мм.
З метою оцінки агресивності пухлин хворих розподілено на чотири групи: до першої групи увійшли 207 (34,6%) пацієнтів із пухлиною в медіальному (N), до другої — 126 (21%) із пухлиною у верхньому (U), до третьої — 112 (18,7%) із пухлиною в нижньому (I), до четвертої — 154 (25,7%) із пухлиною в латеральному (C) сегменті нирки згідно з N.C.I.U. нефрометрією (рисунок).
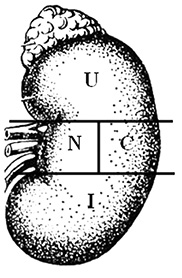
Рисунок. Схема поділу нирки на медіальний (N), латеральний (C), нижній (I) та верхній (U) сегменти згідно з N.C.I.U. нефрометрією
Статистичної різниці в групах порівняння за віком, статтю, тривалістю захворювання, загальним станом здоров’я, наявністю больового синдрому, розміром пухлини, відсотком збереженої паренхіми нирки, а також показником загальної швидкості клубочкової фільтрації та на боці ураження не виявлено (р>0,05). Також не зафіксовано різниці у гістологічній структурі пухлини: більше ніж у 82% випадків діагностовано світлоклітинний нирково-клітинний рак в усіх досліджуваних групах (р>0,15).
Однак встановлено достовірно вищі показники в групі з медіально розміщеними пухлинами щодо кількості хворих із наявністю гематурії — у 14% (р=0,006), артеріальної гіпертензії — у 31,4% (р=0,004) та віддалених метастазів — у 20,8% (р=0,0004) пацієнтів порівняно з іншими групами, що пов’язано з їх близькістю до судинної ніжки та порожнинної системи нирки.
Пухлини воріт нирки Т1 стадії — це агресивні пухлини, які, незважаючи на свої розміри та початкову стадію, у 14% випадків викликають гематурію, у 31,4% — артеріальну гіпертензію та мають у 2 рази більший потенціал метастазування, ніж пухлини інших локалізацій.
Локальна ішемія при резекції нирки з приводу нирково-клітинного раку
Е.О. Стаховський, Ю.В. Вітрук, О.А. Войленко, О.Е. Стаховський, П.С. Вукалович, О.В. Буйвол
Відділення пластичної та реконструктивної онкоурології,
Національний інститут раку, Київ, Україна
Зупинка кровообігу в нирці під час резекції зменшує крововтрату, покращує візуалізацію її структур, що дозволяє здійснити адекватне ушивання порожнинної системи та якісно провести гемостаз. Однак теплова ішемія більше 20 хв може бути пов’язана з незворотними змінами проксимальних збірних канальців, що призводить до нефросклерозу та розвитку ниркової недостатності у віддалений післяопераційний період.
Мета дослідження — оцінити ефективність локальної ішемії при резекції нирки з приводу нирково-клітинного раку та її вплив на функціональний стан нирки.
Проаналізовано результати лікування 291 пацієнта, яким виконано резекцію нирки з приводу нирково-клітинного раку. Вік хворих становив від 25 до 83 років (у середньому 55±11,2 року). Чоловіків було 163 (56%), жінок — 128 (44%). Розміри пухлини становили від 10 до 208 мм (у середньому 48,7±28,3 мм). Об’єм функціонуючої паренхіми нирки на боці ураження був >55% і в середньому досягав 83,7±12,2%.
З метою оцінки впливу ішемії на об’єм крововтрати та функціональний стан нирки хворих розділено на дві групи: до першої увійшли 107 (46,7%) пацієнтів, у яких оперативне втручання виконано з центральною ішемією тривалістю від 5 до 21 хв (9,9±3,3 хв), до другої — 122 (53,3%) хворих із використанням локальної ішемії за методикою клініки (рисунок).
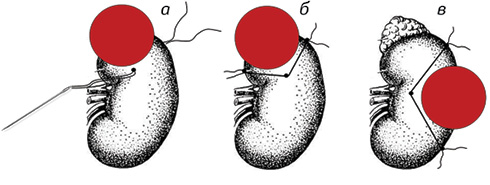
Рисунок. Спосіб локальної ішемії при резекції нирки: а) проведення двох гемостатичних знімних лігатур через нирку на здоровий край паренхіми, що прилягає до об’ємного процесу; б) стискання прилеглої паренхіми нирки до об’ємного процесу, який локалізується у верхньому чи нижньому сегменті; в) стискання прилеглої паренхіми нирки до об’ємного процесу, який локалізується по латеральному краю
Оперативні втручання виконували як відкритим, так і лапароскопічним способом. Статистичної різниці за розміром пухлини (46,7±22,9 та 46,9±25,6 мм), об’ємом функціонуючої паренхіми нирки (82,7±13,2 та 84,9±12,3%) та об’ємом інтраопераційної крововтрати (332,9±126,5 та 343,1±230,9 мл) відповідно в двох групах порівняння не виявлено (р>0,2), що підтверджувало адекватність виконання локальної ішемії та схожість із показниками при центральній ішемії. Також не встановлено різниці в кількості інтра- та післяопераційних ускладнень у вигляді кровотечі, гіпертермії чи сечової нориці — у 9 (8,4%) та 10 (8,2%) випадках відповідно (р>0,9).
При порівнянні показників швидкості клубочкової фільтрації на боці ураження виявлено, що, незважаючи на відсутність достовірної різниці показників у доопераційний період (44,2±11,7 та 45,6±13,4 мл/хв/1,73 м2 відповідно), центральна ішемія достовірно знижує її функцію в післяопераційний період як через 3 міс (на 25,9% до значення 33,8±10,7), так і через 1 рік (на 28,5% до значення 32,6±11,9; р<0,05). При локальній ішемії через 3 міс після операції відмічено достовірне зниження показника на 11,5% — до рівня 39,1±10,9 (р<0,05), проте через 1 рік функція нирки достовірно не відрізнялася (р>0,05) та була близькою до початкових значень і становила 42,3±9,8 мл/хв/1,73 м2.
Локальна ішемія при резекції нирки як відкритим, так і лапароскопічним способом дає можливість покращити техніку гемостазу, зменшує тривалість та об’єм ішемії нирки, що знижує ризик виникнення порушення її функції в майбутньому.
Аналіз факторів, що впливають на вибір тактики оперативного лікування при раку нирки
О.А. Войленко, О.Е. Стаховський, Ю.В. Вітрук, П.С. Вукалович, Е.О. Стаховський
Відділення пластичної та реконструктивної онкоурології,
Національний інститут раку, Київ, Україна
Радикальна нефректомія (НЕ) та резекція нирки (РН) є стандартними операціями в лікуванні пацієнтів із локалізованим нирково-клітинним раком (НКР). При однакових онкологічних результатах і кращих функціональних за умови виконання РН показання до цих операцій залишаються дискутабельними. Жодна спроба об’єктивізувати показання до РН і НЕ не увінчалася успіхом. Застосування нефрометрії дало можливість прогнозувати ризик виникнення ускладнень після РН, але не дозволило розробити показання до РН.
З урахуванням вищезазначеного метою роботи було визначити основні фактори, що впливають на вибір оперативної тактики у хворих на НКР, шляхом проведення мультифакторного аналізу основних клінічних і нефрометричних параметрів.
З 2008 р. у клініці проведено оперативне лікування 1179 хворих з однобічним НКР. З січня 2010 по грудень 2014 р. при плануванні оперативного втручання у пацієнтів визначали нефрометричні параметри, що дозволило провести аналіз їх впливу на вибір методу оперативного лікування. У дослідження включено 940 пацієнтів із НКР Т1–Т2 стадії, яких розділили на 2 групи: в I групу включено 560 (59,6%) хворих, що підлягли РН, у II — 380 (40,4%) пацієнтів, яким виконано НЕ. Групи були зіставними за основними клінічними параметрами. Середній вік становив 54,2±11,1 і 55±10,9 року у порівнюваних групах відповідно. Обидві групи ідентичні за статтю (58,6 і 41,4% проти 58,7 і 41,3% чоловіків та жінок відповідно). Сумарна клубочкова фільтрація становила 86,9±17,8 мл/хв/1,73 м2 проти 84,4±19,8 мл/хв/1,73 м2; ECOG статус — 0,54±0,42 бала проти 0,55±0,41 бала для групи РН і НЕ відповідно.
У подальшому проведено мультифакторний аналіз в групах порівняння за параметрами, які можуть вплинути на вибір методу оперативного лікування, такими як: максимальний розмір пухлини, локалізація (центральна, латеральна і полярна), вид росту (екзо-, ендофітний), відстань до порожнинної системи нирки, розташування на передній або задній поверхні, об’єм функціонуючої паренхіми. Усі представлені фактори оцінювали за даними комп’ютерної томографії.
При аналізі кожного з перелічених параметрів нефрометрії статистично достовірну різницю виявлено в локалізації пухлини (РН частіше виконували при полярному розташуванні пухлини і НЕ — при центральному) (χ2=149; р<0,0001). Настільки ж суттєву різницю встановлено при порівнянні розмірів пухлини (46,7±20,7 см — при РН проти 83,1±35,1 см — при НЕ; р<0,001). Максимальний розмір пухлини при РН становив 15,3 см, а при НЕ — 17,5 см, що не суттєво. Максимальну різницю результатів виявлено при аналізі об’єму збереженої паренхіми нирки (84,5±12,4% — при РН проти 50,8±21,8% — при НЕ; р<0,00001). Зазначені дані стали приводом для проведення аналізу показників у підгрупах за локалізацією пухлини. Нирку умовно розділили на 4 сектори (NCIU nephrometry). При латеральному і полярному розташуванні пухлини порогове значення відсотка збереженої паренхіми, при якому виконували РН, становило 57% з чутливістю 94,4% і специфічністю 85,7%, а при медіальному розташуванні основну роль відіграв розмір пухлини до 4 см з чутливістю 95,7% і специфічністю 94,1%.
Проведений мультифакторний аналіз показав, що основними чинниками, що впливають на вибір оперативної тактики лікування при НКР, був розмір пухлини, її локалізація і відсоток збереженої паренхіми нирки. Представлені в роботі дані дозволяють об’єктивізувати показання до проведення РН і НЕ. При центральному розташуванні утворення основним показанням до РН є розмір пухлини <4 см, а при латеральному і полярному — збереження об’єму функціонуючої паренхіми нирки >57%. У всіх інших випадках пацієнтам із НКР показано проведення НЕ.
Особливості раку ниркових канальців Белліні
Е.О. Стаховський, Ю.В. Вітрук, О.А. Войленко, О.Е. Стаховський, О.В. Буйвол, М.С. Кротевич
Відділення пластичної та реконструктивної онкоурології, Національний інститут раку, Київ, Україна
Тубулярна карцинома нирки (тубулярний рак, рак ниркових канальців Белліні) відзначається у <1% випадків всіх злоякісних уражень нирки та належить до агресивних пухлин. Тактика ведення таких пацієнтів має відрізнятися від стандартних методів лікування хворих на нирково-клітинний рак.
Мета дослідження — визначити особливості та тактику лікування хворих на рак ниркових канальців Белліні.
У період з 2008 по 2014 р. у відділенні виконано 1224 оперативних втручання у хворих на нирково-клітинний рак.
Гістологічно рак ниркових канальців Белліні діагностовано у 21 (1,7%) пацієнта, які й стали об’єктом подальшого аналізу. Вік хворих становив від 35 до 69 років (у середньому 56,3±10,3 року). Чоловіків було 11 (52,4%), жінок — 10 (47,6%). Розмір пухлини досягав 29–140 мм (64,9±25,9 мм). Загальна сума балів за R.E.N.A.L. score — від 7 до 12 (9,6±1,4), причому пацієнти високого ризику становили 61,9%. Об’єм функціонуючої паренхіми нирки на боці ураження коливався від 24 до 99% (58,7±21,3%). Загальна швидкість клубочкової фільтрації становила 84±20,3 мл/хв, а на боці ураження — 38,5±12,6 мл/хв.
У 7 (33,3%) випадках виконано резекцію нирки, у 14 (66,6%) — нефректомію. У 12 (57,1%) хворих оперативне втручання доповнено лімфодисекцією, у 5 (23,8%) — адреналектомією. У 5 (23,8%) пацієнтів операція мала циторедуктивний характер.
При аналізі скарг хворих у 12 (57,1%) пацієнтів виявлено больовий синдром, у 10 (47,6%) — паранеопластичний синдром (артеріальна гіпертензія, втрата маси тіла, гіпертермія, підвищення швидкості осідання еритроцитів, анемія), у 5 (23,8%) — гематурію.
За даними комп’ютерної томографії, у 9 (42,9%) пацієнтів пухлина локалізувалася в медіальному (N), у 8 (38,1%) — в латеральному (C), у 4 (19%) — у верхньому (U) чи нижньому (І) сегменті нирки згідно з N.C.I.U. нефрометрією, тобто у 81% випадків пухлина містилася в інтерполярній ділянці відповідно до R.E.N.A.L. score (p<0,001). У 12 (57,1%) хворих зафіксовано метастатичне ураження регіонарних лімфовузлів, у 5 (23,8%) — легень, в 1 (4,8%) — іпсилатеральної надниркової залози.
Період спостереження за хворими становив від 3 до 67 міс (21,7±17,5 міс). Статистично достовірного впливу проведеного оперативного втручання на виживаність не виявлено (p>0,3). Загинуло від прогресування основного захворювання в термін до року 6 (28,6%) пацієнтів із метастатичним раком, ще у 5 (23,8%) хворих діагностовано прогресування пухлинного процесу у вигляді метастазування у вісцеральні органи впродовж 3–21 міс після операції. Медіана виживаності без прогресування становила 19,8 міс (рис. 1). Медіани загальної виживаності поки не досягнуто (рис. 2).
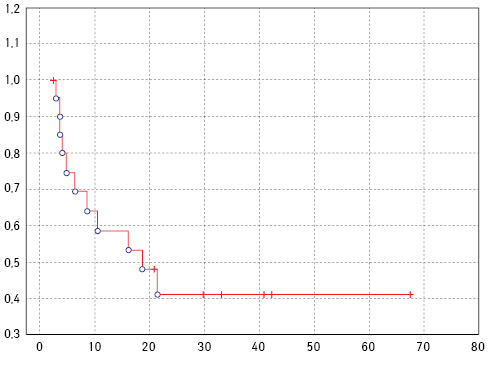
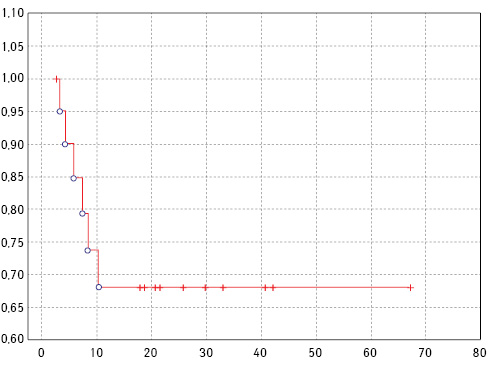
Рис. 2. Загальна виживаність хворих на рак ниркових канальців Белліні
У 1 (4,8%) хворого через 20 міс після резекції діагностовано місцевий рецидив, що змусило в подальшому виконати нефректомію.
Тубулярна карцинома нирки у 57,1% випадків викликає больовий синдром, у 47,6% — паранеопластичний синдром, у 23,8% — гематурію, в 42,9% локалізується у воротах нирки та у 57,1% — метастазує в регіонарні лімфовузли. Результати нефректомії та резекції нирки зіставні — виживаність без прогресування захворювання та загальна виживаність є низькими, тому кратність диспансерного спостереження за такими хворими протягом перших 2 років має бути частішою, ніж у інших пацієнтів, з метою раннього виявлення та лікування прогресування хвороби.
Новый хирургический подход к контролю почечной артерии при удалении опухолевых тромбов нижней полой вены
В.Н. Лесовой1, Д.В. Щукин1, И.А. Гарагатый1, Г.Г. Хареба1, Н.Н. Поляков2
1Харьковский национальный медицинский университет, Харьков, Украина
2Коммунальное учреждение здравоохранения «Областной центр урологии и нефрологии им. В.И. Шаповала»,
Харьков, Украина
Контроль почечной артерии — один из наиболее ответственных этапов радикальной нефрэктомии с венакаватромбэктомией. Мы представили результаты новой хирургической техники, включающей переднее лигирование почечной артерии после осуществления венакаватромбэктомии.
В исследование вошли 13 пациентов с распространением почечно-клеточного рака в просвет основной почечной (n=3) или нижней полой вены (n=10). При удалении опухолевых тромбов ни в одном из наблюдений не использовали искусственное кровообращение. Во всех случаях вначале выполняли тромбэктомию и лишь затем перевязывали почечную артерию. Результаты оценивали на основании анализа сложности этапа перевязки артерии, общего объема интраоперационной кровопотери, количества случаев кровопотери >100,0 мл во время выделения и перевязки почечной артерии, а также продолжительности операции.
Перевязку почечной артерии из переднего доступа удалось успешно выполнить у всех 13 пациентов. Общий уровень значительных технических трудностей при осуществлении данного маневра составил 7,7%. Серьезные технические проблемы отмечали только у одного больного из группы левосторонних опухолей. Это было связано с наличием метастазов в параортальных лимфоузлах. При новообразованиях правой почки технических проблем не зафиксировано. Клинически значимое кровотечение (>100 мл) в результате попыток выделения и перевязки почечной артерии отмечали у 1 (7,7%) пациента с опухолевым тромбом левой почечной вены. Средний объем кровопотери в течение всей операции не превышал 1990,0 мл (1350,0 мл — для правосторонних новообразований и 2630,0 мл — для левосторонних). Интраоперационной смертности и эмболии легочной артерии фрагментами тромба удалось избежать. Общее время операции варьировало от мин до мин и составляло в среднем мин.
Наш опыт продемонстрировал выполнимость и безопасность новой хирургической техники, включающей переднее лигирование почечной артерии после осуществления венакаватромбэктомии. Этот подход позволяет уменьшить объем кровопотери из венозных коллатералей при мобилизации почки и снизить риск эмболии легочной артерии фрагментами опухолевого тромба.
Резекция почки против радикальной нефрэктомии: анализ периоперационных осложнений
С.П. Степушкин, В.П. Чайковский, Р.В. Соколенко, В.О. Новиков
Урологическое отделение № 1, КУ «Днепропетровская городская многопрофильная клиническая больница № 4» Днепропетровского областного совета», Днепропетровск, Украина
На данном этапе развития хирургии резекция почки является операцией выбора для лечения больных с опухолями почки размером до 7 см. К ее основным достоинствам относят отличные онкологические результаты совместно с сохранением почечной функции. Вместе с тем резекция почки является более сложным видом оперативного лечения, нежели нефрэктомия, и, по данным ряда публикаций, сопряжена с большим количеством периоперационных осложнений.
Цель нашей работы — сравнительный анализ частоты периоперационных осложнений в течение 30 дней при хирургическом лечении пациентов с опухолями почки путем выполнения радикальной нефрэктомии или парциальной резекции почки.
В нашем отделении с января 2010 г. по апрель 2014 г. одним хирургом прооперировано 135 пациентов по поводу опухолей почки размерами до 7 см. Из этой группы были исключены 19 пациентов с почечно-клеточным раком в стадии pT3a. В анализ включены пациенты с доброкачественными опухолями и почечно-клеточным раком в стадии pT1: 56 радикальных лапароскопических нефрэктомий и 60 резекций почки (43 открытым доступом и 17 — лапароскопическим). 52 (86%) резекции выполнены в условиях тепловой ишемии почки (тотальной или селективной). У 8 (14%) больных резекция почки проведена без тепловой ишемии. У 33 (55%) пациентов при резекции почки производили ушивание чашечно-лоханочной системы. Обе группы больных были сопоставимы по клиническим данным. Средние размеры опухоли были больше в группе радикальной лапароскопической нефрэктомии. Все тесты были двусторонними, а значения р<0,05 считали статистически значимыми. Результаты анализа представлены в таблице.
Таблица. Хирургические вмешательства у пациентов
с почечно-клеточным раком и доброкачественными
опухолями почки
|
Показатель |
Лапароскопическая нефрэктомия (n=56) |
Резекция |
р |
|
среднее значение |
|||
|
Возраст |
59,6 (60; 27–78) |
57,4 (58; 30–75) |
0,24 |
|
Индекс массы тела |
27,5 |
27,8 |
0,60 |
|
Charlson score |
5,5 (5; 2–11) |
4,9 (5; 2–10) |
0,23 |
|
Размер опухоли, см |
5,5 (5,7; 3,5–7) |
3,6 (3,5; 1,5–7) |
<0,001 |
|
n (%) |
|||
|
Мужчины |
24 (43) |
20 (33) |
0,87 |
|
Женщины |
32 (57) |
40 (67) |
|
|
Симптомы |
34 (61) |
24 (40) |
0,12 |
|
ECOG статус: 0 >0 |
30 (54) 26 (46) |
35 (58) 25 (42) |
0,53 |
|
Гистологические подтипы: • почечно-клеточный рак Т1а • почечно-клеточный рак Т1в • доброкачественные опухоли |
8 (14) 45 (80) 3 (6) |
41 (68) 8 (14) 11 (18) |
<0,001 <0,001 0,07 |
|
Ранние операционные осложнения (в течение 30 дней): • интраоперационное ранение главных сосудов • гематома • артериочашечная фистула • раневая инфекция • гиперволемия • пребывание |
1 (1,8) 1 (1,8) 0 1 (1,8) 1 (1,8) 2 (3,6) |
2 (3,3) 1 (1,6) 1 (1,6) 1 (1,6) 0 2 (3,3) |
0,72 0,9 0,35 0,9 0,35 0,9 |
Госпитальной смертности не было в обеих исследуемых группах больных. В нашей серии наблюдений не выявлено достоверной разницы периоперационных осложнений в группах лапароскопической нефрэктомии и резекции почки. При этом следует отметить, что в группе резекции почки не было такого вида осложнений, как уринома.
Резекция почки является безопасным и эффективным методом лечения пациентов с опухолями почки размером до 7 см, что подтверждают результаты нашего исследования. Артериочашечная фистула является характерным осложнением лапароскопической резекции. У специально отобранных для органосохраняющей операции больных резекция почки может приводить к такому же проценту периоперационных осложнений, что и лапароскопическая радикальная нефрэктомия.
Исследование активности матриксной металлопротеиназы-9 при внутривенозном распространении почечно-клеточного рака
В.Н. Лесовой1, Д.В. Щукин1, И.И. Яковцова2, И.А. Гарагатый1, С.В. Данилюк, Г.Г. Хареба1, М.Н. Бабич, В.Д. Товажнянская
1Харьковский национальный медицинский университет, Харьков, Украина
2Харьковская медицинская академия последипломного образования, Харьков, Украина
3Коммунальное учреждение здравоохранения
«Областной центр урологии и нефрологии им. В.И. Шаповала», Харьков, Украина
Мы исследовали экспрессию матриксной металлопротеиназы-9 (ММР-9) у пациентов с внутривенозной опухолевой инвазией.
В исследовании приняли участие 94 пациента, которых разделили на 3 группы: в первую вошли больные почечно-клеточным раком без признаков макро- или микроскопической инвазии в венозные сосуды (n=21); во вторую — пациенты с почечно-клеточным раком с микроскопической внутривенозной инвазией (n=22); в третью — с почечно-клеточным раком с макроскопической инвазией в венозные сосуды почки и нижнюю полую вену (n=51). Для иммуногистохимического исследования опухолей и неопластических тромбов на содержание металлопротеиназы-9 использовали концентрированные кроличьи поликлональные антитела к ММР-9, 92 кДа Collagenase IV фирмы «Thermo scientific» (Великобритания) в разведении 1:50.
Результаты нашего исследования продемонстрировали очевидную роль MMP-9 в патогенезе внутривенозного распространения почечно-клеточного рака. В опухолях без признаков внутривенозной инвазии уровень ее экспрессии был низким. Окрашивание фиксировалось преимущественно в цитоплазме и ни в одном из наблюдений не охватывало все опухолевые клетки. Умеренная экспрессия встречалась лишь у 12% новообразований данной группы. Микроскопическая внутривенозная инвазия сопровождалась умеренной экспрессией MMP-9 в более 70% наблюдений.
Для макроскопических опухолевых тромбов в почечной или в нижней полой вене была характерна картина «металлопротеиназного взрыва». 100% опухолей с этой формой инвазии демонстрировали высокие уровни экспрессии MMP-9. При этом металлопротеиназу выявляли не только в опухолевых клетках, но и в эндотелиоцитах опухолевого тромба и почечных вен, а также в лимфоцитах, макрофагах, гистиоцитах инфильтрата зоны инвазии стенки вены. В отдельных случаях отмечена сверхэкспрессия ММР-9, когда окраска фиксировалась в 100% клеток как эпителиального, так и лимфогистиоцитарного ряда. Экспрессия ММР-9 была гораздо выше в группе опухолей с макроскопическим внутривенозным распространением. Она не коррелировала с протяженностью (р=0,68) опухолевого тромба или с размерами основной опухоли (р>0,05).
Наличие отдаленных и лимфогенных метастазов, а также низкая степень дифференцировки опухолевых клеток были позитивными прогностическими параметрами в плане выявления гиперэкспрессии ММР-9 (р<0,01).
ММР-9 может быть одним из наиболее значимых показателей инвазивного и метастатического потенциала эпителиальных светлоклеточных опухолей почки. Более агрессивный фенотип светлоклеточного почечно-клеточного рака ассоциируется со сверхэкспрессией ММР-9. ММР-9 играет важную роль в патогенезе внутривенозного распространения почечно-клеточного рака.
Изучение активности ММР-9 в почечно-клеточных опухолях может иметь значительные перспективы в определении метастатического потенциала у пациентов с внутривенозным распространением данных новообразований. Для подтверждения этой гипотезы необходимо дальнейшее клинико-морфологическое исследование с изучением корреляций между экспрессией ММР-9, уровнем метастазирования опухолей и выживаемостью пациентов.
Опыт использования аппарата искусственного кровообращения в хирургии осложненных гигантских нефробластом у детей
И.Б. Щепотин1, И.Н. Емец2, Г.И. Климнюк1, А.Й. Ижовский1, О.В. Белоконь1, М.А. Стежка1, О.В. Проценко2
1Национальный институт рака, Киев, Украина 2ГУ «Научно-практический медицинский центр детской кардиологии и кардиохирургии», Киев, Украина
Хирургическое лечение нефробластом (опухоль Вильмса) у детей является одним из основных этапов комбинированного лечения, радикальность которого непосредственно влияет на отдаленные результаты, продолжительность безрецидивного периода и общий уровень пятилетней выживаемости у данной категории пациентов.
При ретроспективном анализе установлено, что в течение 5 лет в Украине произведено 5 оперативных вмешательств с использованием аппарата искусственного кровообращения у детей с опухолью Вильмса.
У 4 пациентов диагностирована монолатеральная нефробластома (у всех случаях с бластемным типом опухоли), из них у 3 выявлена III стадия процесса, у 1 — IV стадия и еще у 1 — двухсторонняя опухоль Вильмса (V стадия процесса). Средний возраст больных на момент операции составил 3,4 года.
Отбор больных для оперативного вмешательства с применением аппарата искусственного кровообращения проводили по следующим критериям:
- наличие огромной симптомной осложненной нефробластомы с предпологаемой значительной интраоперационной кровопотерей;
- наличие опухолевого тромба в нижней полой вене и/или правом предсердии;
Все оперативные вмешательства выполнены в объеме радикальной нефрэктомии: у одного больного симультанно проведена операция по удалению новообразования правого предсердия с резекцией его стенки, у другого — удаление флотирующего тромба из нижней полой вены и правого предсердия, пролабирующего в просвет правого желудочка.
Одному больному в связи с инвазией процесса в селезеночную артерию и вену, интимным сращением опухоли с паренхимой селезенки выполнена левосторонняя нефрэктомия единым блоком со спленэктомией. Средняя продолжительность операции составила 208 мин, среднее время искусственного кровообращения 127 мин.
Ранние послеоперационные осложнения развились у 2 (40%) больных: у 1 больного (20%) клинико-лабораторными методами установлен диагноз послеоперационного панкреатита, который был пролечен консервативно, еще у 1 (20%) — лимфорея, которая купирована консервативно, и у обоих — явления гастростаза. Послеоперационный период в среднем составил 4,8 койко-дня.
При исследовании отдаленных результатов лечения 2 больных умерли в связи с рефрактерностью опухоли к химиотерапии и прогрессированием заболевания: 1 пациент — с первично метастатической левосторонней монолатеральной нефробластомой и еще 1 — с билатеральной опухолью Вильмса с метастазами опухоли в легких.
Использование аппарата искусственного кровообращения в хирургии осложненных гигантских нефробластом у детей позволяет выполнять сложные хирургические вмешательства при считавшихся раннее нерезектабельных опухолях с проростанием в смежные органы; у пациентов с нарушениями сердечной и дыхательной систем; при предполагаемой значительной интраоперационной кровопотере, у больных с развитыми сосудистыми коллатералями; при тромбозах нижней полой вены и правого предсердия; дает возможность проводить симультанные кардиохирургические операции с минимальным риском летальных интраоперационных осложнений, управлять системой гемостаза пациента.
Зв’язок функції нирки з розміром пухлини та об’ємом залишкової функціонуючої паренхіми
О.Е. Стаховський, П.С. Вукалович, Ю.В. Вітрук, О.А. Войленко, Е.О. Стаховський
Відділення пластичної та реконструктивної онкоурології,
Національний інститут раку, Київ, Україна
Об’єм залишкової функціонуючої паренхіми (ОЗФП) є величиною, що вказує на відсоток неураженої пухлиною ниркової тканини при пухлинах нирки. Цей показник спрощує хірургу вибір тактики оперативного лікування на користь парціальної резекції нирки з пухлиною з урахуванням різних значень ОЗФП залежно від локалізації пухлини. У попередніх роботах продемонстровано кореляцію між розміром пухлини та функцією ураженої нирки у хворих на нирково-клітинний рак.
З урахуванням того, що більшість пухлин нирки не є ендофітними, а отже, лише частково заміщують здорову паренхіму своїм ростом, впливаючи на функцію, метою роботи стало визначення кореляційних зв’язків між ОЗФП та функцією нирки, в якій локалізується пухлина.
Проведено ретроспективний аналіз 442 хворих з однобічними пухлинами нирки у локалізованих стадіях, яким в доопераційний період виконано динамічну нефросцинтиграфію і які лікувалися в період 2010–2014 рр. Середній вік хворих становив 54±9 років. Пацієнти з діабетом, артеріальною гіпертензією та іншими захворюваннями, що могли впливати на функцію нирки, були виключені з дослідження. Середній розмір пухлини сягав 57,8±22,8 мм (від 11 до 195 мм). Швидкість клубочкової фільтрації визначали за допомогою динамічної нефросцинтиграфії, у середньому цей показник становив 43,8±9,7 мл/хв для боку ураження. ОЗФП визначали за формулою обчислення об’єму еліпсоїда, що описано в попередніх роботах. Для оцінки залежності функції ураженої нирки від розміру пухлини, а також ОЗФП побудовано кореляційні графіки.
Оцінка залежності вищезазначених показників на графіках не виявила достовірної різниці між величинами (рисунок), але кореляція ОЗФП виявилась більшою (R2=0,182 та R2=0,124).
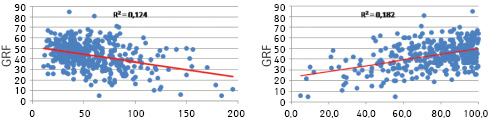
Рисунок. Залежність функції ураженої нирки від розміру пухлини і ОЗФП у хворих з однобічними пухлинами нирки у локалізованих стадіях
ОЗФП і розмір пухлини є основними показниками, що впливають на вибір тактики оперативного лікування хворих з локалізованими пухлинами нирки. ОЗФП має сильніший кореляційний зв’язок із функцією нирки, тому має бути пріоритетним при виборі тактики хірургічного лікування.
Неповна апаратна каваплікація як засіб профілактики тромбоемболії легеневої артерії при хірургічному лікуванні нирково-клітинного раку, ускладненого пухлинним тромбозом нижньої порожнистої вени
В.І. Русин, В.В. Корсак, С.О. Бойко, Я.М. Попович
Державний вищий навчальний заклад «Ужгородський національний університет», Ужгород, Україна
Хірургічне лікування пацієнтів із пухлинним тромбозом нижньої порожнистої вени (НПВ) залишається єдиним ефективним методом терапії при нирково-клітинному раку (НКР), ускладненому судинною інвазією. У результаті застосування агресивної хірургії виникає ризик тромбоемболічних ускладнень як під час операції, так і у післяопераційний період. Тому розробка та удосконалення засобів профілактики тромбоемболії легеневої артерії (ТЕЛА) є актуальним завданням для забезпечення покращення результатів хірургічного лікування при НКР, ускладненому пухлинним тромбозом НПВ.
Мета роботи — вивчити ефективність та розробити показання до виконання неповної апаратної каваплікації як засобу профілактики ТЕЛА під час відкритого видалення пухлинного тромбу з НПВ у хворих на НКР.
У дослідження включено 100 хворих на НКР, ускладнений пухлинною інвазією ниркової вени та НПВ, прооперованих у хірургічній клініці Закарпатської обласної клінічної лікарні ім. А. Новака у 2005–2014 рр. За рівнем поширення пухлинного венозного тромбу (згідно з класифікацією клініки Мейо) хворих розподілили таким чином: нульовий рівень виявлено у 42 пацієнтів; І — у 20; ІІ — у 20; ІІІ — у 14; IV — у 4.
Усі операції виконано з лапаротомного доступу у одній із трьох модифікацій: трансабдомінальний двобічний підребровий доступ у модифікації за типом «Chevron» чи «Mercedes» або розширена серединна лапаротомія. У 18 хворих одним з оперативних прийомів була мобілізація печінки та ротація її правої частки вліво за методикою «piggyback». Методику пальцевого зсування верхівки тромбу у НПВ до рівня нижче головних печінкових вен застосували у 13 з 18 пацієнтів з ІІІ та IV рівнями поширення пухлинного венозного тромбу. У 4 хворих, поряд з онкологічною патологією, розвинувся справжній масивний тромбоз НПВ та спільних клубових вен.
Неповна апаратна аплікація НПВ за розробленою нами методикою застосована у 33 (33%) пацієнтів за допомогою апарата «УКБ 15-1». Ця методика полягає у створенні у НПВ у поперечному напрямку трьох симетричних каналів діаметром 5–8 мм, через які забезпечується розділений і дещо сповільнений відтік крові по НПВ. У 23 випадках її виконали нижче рівня впадіння ниркових вен у НПВ, у 9 — вище рівня впадіння ниркових вен у НПВ і у 1 — вище рівня впадіння головних печінкових вен у НПВ. У 3 хворих проведено протезування НПВ протезами Gor-tex. Усі хворі в післяопераційний період отримували низькомолекулярні гепарини відповідно до стандартів та протоколів лікування пацієнтів зі злоякісними пухлинами.
Ми не зареєстрували випадків інтра- чи післяопераційної летальності внаслідок ТЕЛА. Запропонована хірургічна тактика передбачає виконання обов’язкового першочергового контролю за НПВ над верхівкою тромбу за допомогою судинного затискача чи турнікета. Наступним етапом хірургічної профілактики ТЕЛА є застосування неповної апаратної каваплікації як завершального моменту після відкритого видалення протяжних ретропечінкових, наддіафрагмальних чи фіксованих тромбів НПВ, що супроводжується висіченням стінки чи значним ушкодженням інтими НПВ, а також при супутньому справжньому масивному тромбозі НПВ та спільних клубових вен.
Застосування неповної апаратної каваплікації є ефективним засобом механічної профілактики ТЕЛА під час хірургічного лікування пацієнтів із НКР, ускладненим пухлинним тромбозом НПВ.
Применение нефронсберегающей хирургической техники при нефробластомах у детей и ее влияние на выживаемость
Г.И. Климнюк, О.В. Белоконь, А.Й. Ижовский
Отделение детской онкологии, Национальный институт рака,
Киев, Украина
Нефронсберегающие оператививные вмешательства при злокачественных новообразованиях почки у пациентов в возрасте старше 18 лет в онкоурологии используют достаточно давно. На сегодня есть две группы исследователей, которые имеют прямо противоположные точки зрения на использование данного вида вмешательства в детской онкологии.
Одна группа считает, что нефронсберегающие вмешательства можно применять для лечения детей с нефробластомой, вторая группа придерживается мнения, что данный вид вмешательства может быть применен только при билатеральной нефробластоме.
Целью нашего исследования стало обобщение опыта, накопленного в отделении детской онкологии Национального института рака.
Мы ретроспективно проанализировали базу данных за период 2007–2014 гг. В исследования вошли пациенты в возрасте младше 18 лет с опухолью Вильмса. Проведена оценка клинико-рентгенологических данных. Полученные результаты оценены с использованием многомерной логистической регрессии.
В отделении детской онкологии в 2007–2014 гг. находились на стационарном лечении 186 детей с нефробластомой. Из них у 33 выполнены нефронсберегающие оперативные вмешательства, что составляет 17,7% случаев. 13 больных получали лечение по поводу билатеральной нефробластомы, в 20 случаях диагностирована односторонняя нефробластома. Пациентов с односторонней нефробластомой распределили по стадиям заболевания: с I стадией прооперировано 2 (10%) детей, II — 13 (65%), III — 4 (20%), IV — 1 (5%). Во всех случаях проведена неоадъювантная полихимиотерапия по протоколу SIOP-2001, выявлена регрессия опухоли в пределах 80–95% (объем опухоли определяли согласно методике, обозначенной в протоколе, перед началом лечения и перед оперативным вмешательством).
По результатам патоморфологического исследования пациенты были разделены соответственно гистологическому варианту в группу стандартного или высокого риска: стандартный риск — 19 (57,6%) случаев, высокий риск — 14 (42,4%) На сегодня все дети, находившиеся под наблюдением после нефронсберегающих оперативных вмешательств, живы.
У детей с опухолью Вильмса нефронсберегающие оперативные вмешательства достаточно редко выполняют. Данный вид операций ранее применяли исключительно при билатеральных опухолях, однако в последнее врямя наметилась тенденция к расширению показаний к проведению органосберегающих хирургических вмешательств. Как показали результаты исследования, нет различий в выживаемости у детей после нефронсберегающих операций и детей, перенесших радикальную нефрэктомию. С учетом ряда исследований, которые показали высокий риск развития хронической почечной недостаточности у пациентов с одной почкой после нефрэктомии, применение органосберегающих методик является приоритетным.
«Fast track surgery» при проведенні резекції нирки
О.А. Войленко, О.Е. Стаховський, Ю.В. Вітрук, П.С. Вукалович, Е.О. Стаховський
Відділення пластичної та реконструктивної онкоурології, Національний інститут раку, Київ, Україна
Резекція нирки на сьогодні стала бажаною альтернативою радикальній нефректомії та є стандартном лікування пацієнтів із нирково-клітинним раком (НКР) в стадії Т1. Мультимодальна програма «Fast track surgery» (FTS, хірургія швидкого відновлення) викликає все більший інтерес у хірургів, але досі не застосовується у пацієнтів, які перенесли резекцію нирки.
Мета роботи — проаналізувати ефективність мультимодальної програми «Fast track surgery» після резекції нирки з приводу НКР.
З січня 2013 р. у відділенні пластичної та реконструктивної онкоурології Національного інституту раку проводять рандомізоване дослідження хворих на НКР із застосуванням мультимодальної програми FTS, порівнюючи зі стандартним оперативним лікуванням. Критеріями включення були: однобічний НКР в стадії T1N0M0 за відсутності вираженої супутньої патології. У дослідженні взяли участь 158 пацієнтів із НКР. Чоловіків — 85 (53,8%), жінок — 73 (46,2%). Вік хворих — від 24 до 75 років, у середньому — 52,7±10,2 року.
Пацієнтів шляхом рандомізації (у співвідношенні 1:1) розподілили на 2 групи: до основної (дослідної) включено 78 пацієнтів, до контрольної — 80. Обидві групи хворих були зіставними за факторами клінічного прогнозу. Середній вік хворих становив відповідно 51,2±10,4 та 54,1±9,7 року в основній та контрольній групах. В обох групах більшість хворих — чоловічої статі (56,4 та 51,3% відповідно). Розмір пухлини становив 3,9±1,4 см проти 4,2±1,5 см; тривалість захворювання — 1,9±1,6 міс проти 2,1±1,9 міс; рівень загальної клубочкової фільтрації — 93,8±17,2 мл/хв проти 94,3±18,9 мл/хв; та ECOG статус — 0,4±0,3 бала проти 0,3±0,2 бала в основній та контрольній групах відповідно. Операцію в усіх випадках проводили трансабдомінальним доступом. Ішемію нирки не використовували в жодному випадку.
Основні аспекти стратегії «Fast track surgery» включали:
- передопераційний період: відмова від механічної підготовки кишки (очисні клізми перед операцією); відмова від голодування перед операцією (останній прийом їжі за 5–7 год до операції харчовими сумішами із підвищеним вмістом вуглеводів); відмова від премедикації наркотичними анальгетиками;
- під час операції: епідуральна анестезія розчином біпувакаїну 0,125% 8–9 мл/год, застосування нестероїдних протизапальних діючих речовин; міні-інвазивний оперативний доступ; мінімізація крововтрати; відмова від встановлення дренажів у черевну порожнину;
- післяопераційний період: раннє ентеральне харчування (у середньому через 6 год після операції); рання активізація пацієнта (у 1-шу добу); інтенсивна знеболювальна терапія з використанням подовженої епідуральної анальгезії з місцевими анестетиками, відмова від рутинного використання наркотичних анальгетиків.
Оцінку ефективності стратегії «Fast track surgery» проводили за рівнем післяопераційних ускладнень, тривалістю перебування в стаціонарі, інтенсивністю больових проявів, рівнем повторних госпіталізацій в період до 30 днів після операції. Статистичну інтерпретацію отриманих результатів виконували за допомогою програми Statistica 7.0.
Інтраопераційні ускладнення не виникли в жодному випадку. Об’єм крововтрати становив 295±140 мл в основній та 330±177 мл — в контрольній групі (t-test; р>0,2).
Післяопераційні ускладнення виникли у 4 (2,5%) хворих: 2 (2,6%) — в основній групі та 2 (2,5%) — в контрольній (χ2=0,001; р=0,98). Слід зазначити, що рівень ускладнень був незначним та не перевищував ІІІ ступеня за шкалою Clavien — Dindo. В основній групі в 1 випадку виникла заочеревинна гематома, що потребувала однократної пункції під УЗД-контролем, та ще в 1 хворого розвинулося загострення пієлонефриту. У пацієнтів контрольної групи реєстрували ускладнення гнійно-септичного характеру: 1 випадок пієлонефриту та ще 1 — нагноєння післяопераційної рани.
Оцінку болю проводили за 10-бальною візуально-аналоговою шкалою на 3-й день після операції. Цей показник був дещо нижчим в основній групі (2,9±1,1 бала проти 3,5±1,6 бала в контрольній), однак статистично достовірної різниці не досяг (t-test; р=0,21). У цілому, післяопераційний ліжко-день був статистично достовірно коротшим в основні групі пацієнтів (5,4±1,6 проти 10,1±3,9; t-test; р<0,0001). Загалом в жодному випадку пацієнти не потребували повторної госпіталізації.
Представлені результати рандомізованого дослідження свідчать про перспективність застосуванням мультимодальної програми FTS у хворих на НКР, яким проведено резекцію нирки порівняно зі стандартним оперативним лікуванням, дозволяє скоротити післяопераційний ліжко-день при аналогічному рівні післяопераційних ускладнень та інтенсивності болю.
Клинический пример редкой формы
почечно-клеточного рака — муцинозной тубулярной и веретеновидно-клеточной карциномы почки
П.Г. Яковлев1, В.В. Мрачковский1, В.А. Кропельницкий2, И.В. Саввина3, В.С. Сакало4
1 Отделение урологии, Киевский городской клинический онкологический центр, Киев, Украина
2 Отделение патологии, Киевский городской клинический онкологический центр, Киев, Украина
3Филиал №1 Консультативно-диагностического центра Соломенского района, Киев, Украина
4Государственное учреждение «Институт урологии НАМН Украины», Киев, Украина
К редким формам рака почки относится муцинозная тубулярная и веретеновидно-клеточная карцинома почки. Данный вариант рака почки впервые выделен в классификации ВОЗ в 2004 г. Мы представляем клинические, радиографические, гистологические особенности муцинозной тубулярной и веретеновидно-клеточной карциномы почки.
За период 1998–2014 гг. в отделении урологии Киевского городского клинического онкологического центра получила лечение 1 пациентка с редкой опухолью почки — муцинозной тубулярной и веретеновидно-клеточной карциномой.
Больная В., 58 лет, история болезни № 21557, поступила в клинику 22.10.2014 г. с жалобами на умеренную общую слабость, упадок сил и потерю 8 кг массы тела. На момент обращения болела в течение 6 мес. При осмотре привлекли внимание тусклость, сухость и серость кожных покровов лица. Анализы крови и мочи в норме. На компьютерной томограмме (рис. 1) в нижнем полюсе левой почки определяется дополнительное образование 65 мм в диаметре с четкими неровными контурами относительно однородной структуры. При внутривенном усилении образование умеренно неоднородно накапливает контрастное вещество — менее интенсивно по сравнению с паренхимой почки. Денситометрические характеристики в нативную, кортико-медуллярную, нефрографическую и экскреторную фазу составили соответственно +36 ед.HU, +67 ед.HU, +89 ед.HU и +76 ед.HU. Данных о регионарных и отдаленных метастазах нет.
24.10.2014 г. у больной выполнена операция: люмботомия слева, резекция почки. Интраоперационно установлено, что поверхность опухоли бледная, имеет обедненный сосудистый рисунок. При изучении удаленного макропрепарата — выраженный белесый матовый оттенок опухолевой массы, консистенция опухоли однородная, рыхлая, крошащаяся, мелкозернистая. Кист, некрозов не выявили. При морфологическом исследовании материала опухолевый узел на разрезе — мономорфной консистенции, серо-белого цвета. Микроскопически на большем протяжении опухоль состоит из клеток с округлым или овальным ядром, обильной эозинофильной цитоплазмой (рис. 2). В части клеток отмечали накопление муцина в цитоплазме. Клетки, накапливающие муцин, формируют подобие цепочек. Выявлены участки, состоящие из более мелких клеток, формирующих тубулярные структуры. Очаги некроза отсутствуют.
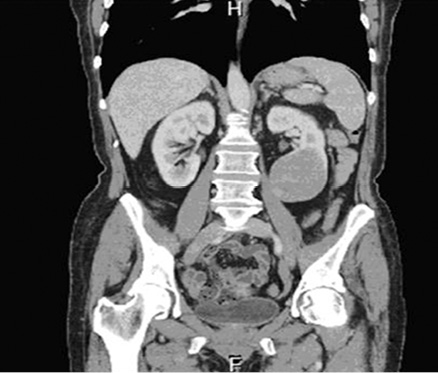
Рис. 1. Компьютерная томограмма больной В., 58 лет, с внутривенным контрастным усилением. Муцинозная тубулярная и веретеновидно-клеточная карцинома нижней половины левой почки, кортико-медуллярная фаза
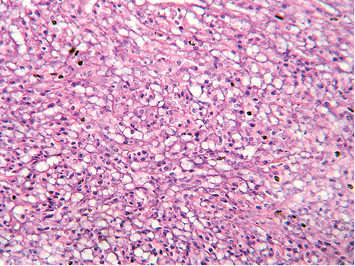
Рис. 2. Удаленный макропрепарат муцинозной тубулярной и веретеновидно-клеточной карциномы почки. Опухоль состоит из клеток с округлым или овальным ядром, обильной эозинофильной цитоплазмой. Фрагмент опухоли, окраска гематоксилином и эозином, ув. ×200
При выписке из стационара на 6-й послеоперационный день у пациентки констатировали нормальную розовую окраску кожных покровов, хороший тургор кожи, прилив сил, улучшение аппетита. Мы оцениваем данную метаморфозу как следствие общего токсического влияния опухоли на организм, что может быть отличительной клинической чертой этой редкой разновидности рака почки.
Муцинозная тубулярная веретеновидно-клеточная карцинома почки — редкий подтип почечно-клеточной карциномы с особым микроскопическим строением. В некоторых случаях необходима дифференциальная диагностика с солидным вариантом папиллярной почечно-клеточной карциномы. Отличается благоприятным течением и прогнозом выживаемости. Возникает чаще у женщин. В клиническом проявлении главным является неспецифический интоксикационный синдром. В лечении методом выбора признают органосохраняющую операцию — резекцию почки.
Результати використання Bone-TRAP-5b
для ранньої діагностики кісткових метастазів у хворих на нирково-клітинний рак
С.І. Бойчук, Е.О. Стаховський, А.Г. Дєдков
Національний інститут раку, Київ, Україна
Кісткові метастази (КМ) у хворих на нирково-клітинний рак (НКР) виникають у 30–50% випадків та займають третє місце за частотою після метастатичного ураження легень та печінки. У 48% пацієнтів НКР діагностують в зв’язку з наявністю КМ. Основними методами лікування цієї категорії пацієнтів є застосування бісфосфонатів, хірургічна та променева терапія.
Мета дослідження — визначити можливість використання маркера кісткової резорбції — тартратрезистентної кислої фосфатази (Bone-TRAP-5b) для ранньої діагностики КМ НКР.
У дослідження включено дві групи хворих. Першу групу (контрольна) — 42 пацієнти із НКР з клініко-рентгенологічно підтвердженими КМ — сформовано для дослідження чутливості та специфічності маркера кісткової резорбції. Другу групу (основна) — 117 пацієнтів із НКР після нефректомії та резекції нирки, без метастазів у кістках та внутрішніх органах (II–IV ступінь морфофункціонального стану ядер епітеліоцитів за Фурманом) — для визначення можливого метастазування в кістки.
Середній вік у першій групі хворих становив 56,3±1,3 року, в другій — 54,5±1,0 року. В основній групі чоловіків було 64 (54,7%), жінок — 53 (45,3%). Основна група поділялася на підгрупу низького (НР) та високого ризику (ВР). Підгрупу з НР розвитку КМ склали хворі, у яких рівень тартратрезистентної кислої фосфатази становив 4,9±0,2 Од/мл в середньому, а підгрупу з ВР — пацієнти з підвищеним рівнем Вone-TRAP-5b (6,5±0,2 Од/мл).
У підгрупі НР переважав II ступінь диференціювання пухлини за Фурманом (61,2%), а в підгрупі ВР — III ступінь (53,1%). Також у підгрупі ВР було значно більше хворих з низьким ступенем диференціювання пухлини (Фурман IV) — 3,5 проти 18,8% у підгрупі НР. Визначення рівня Bone-TRAP-5b проводили щоквартально. Оцінку поширеності виконували за допомогою контрастно підсиленої КТ та МРТ візуалізації, остеосцинтиграфії кісток з 99mTc.
Чутливість методу становила 90,4% у хворих з метастазами в кістках, а специфічність — 85,0%. При аналізі результатів дослідження виявлено достовірне підвищення рівня Bone-TRAP-5b до 6,5±0,2 Од/мл в середньому у підгрупі ВР (p<0,05) порівняно з показниками підгрупи НР (4,9±0,2 Од/мл).
Середній рівень Bone-TRAP-5b в першій підгрупі залишався в межах референтних значень — 4,4±0,4 та 4,2 ±0,2 Од/мл через 3 і 6 міс відповідно. При подальшому спостереженні розвиток КМ виявлено тільки у 4 (4,7%) пацієнтів першої підгрупи НР через 12 міс. У хворих підгрупи ВР рівень залишався високим — 6,7±0,4 і 5,4±0,3 Од/мл через 3 і 6 міс спостереження. З урахуванням вищесказаного в цієї категорії хворих проводили сцинтиграфічне дослідження. У пацієнтів підгрупи ВР при сцинтиграфії виявлено метастази у 27 осіб (84,3%) у середньому через 9,8 міс.
Варто зазначити, що в більшості випадків підвищений рівень Bone-TRAP-5b у підгрупі ВР не залежав від ступеня диференціювання пухлини.
Таким чином, отримані нами попередні дані можуть свідчити про високу діагностичну чутливість TRAP-5b як маркера метастатичного ураження кісток у хворих на НКР. Визначення маркера у цієї категорії пацієнтів може сприяти підвищенню точності ранньої діагностики КМ. Описаний метод може дати можливість провести в підгрупі ВР профілактичні заходи (лікування бісфосфонатами), покращити результати лікування та виживаність, що потребує подальшого вивчення.
Профілактика ускладнень карбоксиперитонеуму при лапароскопічних операціях на нирці
С.В. Байдо1, В.М. Григоренко2, С.І. Приндюк1
1Лікарня Сучасної Онкологічної Допомоги«ЛіСОД», с. Плюти, Обухівський р-н., Київська обл., Україна
2ДУ «Інститут урології НАМН України», Київ, Україна
Однією з умов проведення лапароскопічних операцій є необхідність створення карбоксиперитонеуму, що забезпечує інтраабдомінальний робочий простір та оптимальну візуалізацію анатомічних структур. Відомо, що найбільш значущі зміни центральної гемодинаміки та функції зовнішнього дихання за наявності напруженого карбоксиперитонеуму (НКП) відзначають у хворих із малим резервом компенсаторних механізмів. Із розширенням можливостей лапароскопічної хірургії зростає інтерес до без- або малогазової лапароскопії, при якій інтраабдомінальний простір створюється за допомогою ендоліфтів (механічних підйомників черевної стінки).
Незважаючи на велику кількість різноманітних конструкцій ендоліфтів, жоден з них повністю не влаштовує хірургів, що змусило продовжити пошук шляхів модернізації та оптимізації ліфтингової операції.
У роботі використано оригінальну модель (Патент на корисну модель України № 69135 від 25.04.2012 р.) спірального лапароліфта (зігнутий металевий стрижень діаметром 5 мм, робоча частина якого виконана у вигляді одного витка спіралі радіусом 6–9 см, має на кінці кулеподібне потовщення) зі стельовим кріпленням. При виконанні лапароскопічного втручання після накладання «мінімального» карбоксиперитонеуму (до 8 мм рт. ст.) під відеоскопічним контролем робочу частину ендоліфта вводять у черевну порожнину в точці на рівні пупка по середньоключичній лінії поступально-обертальними рухами. Лапароліфт фіксують на підйомно-утримувальному пристрої зі стельовим кріпленням та проводять десуфляцію.
З використанням лапароліфтингу виконано 19 лапароскопічних радикальних нефректомій та 4 лапароскопічні резекції нирки, середній вік хворих становив 65,5±3,4 року. Усі пацієнти цієї групи раніше отримали відмову у проведенні лапароскопічного втручання в умовах НКП через супутні захворювання (атеросклероз аорти, коронарних артерій, артеріальна гіпертензія II–III ступеня, хронічні обструктивні захворювання легень тощо).
Час встановлення ендоліфта становив у середньому 92,3±2,1 с, середня тривалість операцій — 135±7,3 хв (достовірно не відрізнялася від тривалості таких операцій в умовах НКП — 127±6,4 хв). У всіх випадках здійснювали «безгазову» лапароскопію при виконанні основних етапів операції. Інтра- та післяопераційних ускладнень не відзначали.
Використання пролонгованої епідуральної анальгезії було необхідним протягом 1,5±0,5 доби (від 1 до 2 діб), відновлення перистальтики кишечнику відбувалося через 9±4,5 год (4–15 год), активізація хворих — через 12±4 год (від 8 до 16 год) після операції. Жоден пацієнт не скаржився на біль у надпліччях, характерний для лапароскопічних операцій в умовах НКП. Виписка зі стаціонару була можливою на 4-ту добу після втручання, середній ліжко-день тривав 6,53±1,25 доби.
Таким чином, використання спірального ендоліфта розширює можливості виконання лапароскопічних операцій у пацієнтів із групи ризику за супутньою патологією, а доступність об’єкта операції, робочий простір у черевній порожнині та інтра- й екстракорпоральні просторові взаємодії між встановленим лапароліфтом, лапароскопічними інструментами та об’єктом операції достатні для виконання «безгазових» лапароскопічних втручань на нирці.
Вплив соціально-екологічних факторів на епідеміологію злоякісних пухлин нирки в Прикарпатському регіоні
Є.А. Литвинець, І.В. Білик, Р.Р. Антонів
Кафедра урології, ДВНЗ «Івано-Франківський національний медичний університет», Івано-Франківськ, Україна
За інформацією Всесвітньої організації охорони здоров’я, доведено тісний корелятивний зв’язок між етіологічними факторами злоякісних новоутворень та екологічними умовами проживання людей у різних географічних регіонах. До екологічної патології відносять хвороби та симптомокомплекси, що виникають внаслідок впливу на організм людини різноманітних хімічних, фізичних факторів, а також біологічних чинників, які вибірково локалізуються в певних ділянках біосфери. Дані спостережень свідчать про те, що у 75–80% випадків рак у людей виникає під впливом тих чи інших причин, зумовлених навколишнім середовищем.
При аналізі даних захворюваності населення із різних регіонів Прикарпаття привертає увагу найбільш висока розповсюдженість серцево-судинної патології в рівнинній зоні, тоді як лейкози та злоякісні новоутворення частіше виникають у населення передгір’я.
Мета дослідження — поглибити розуміння ролі факторів геохімічної екології в формуванні та перебігу злоякісних новоутворень нирки.
Нами проведено дослідження даних населення Прикарпатського регіону за останні 25 років. Вивченню підлягали умови проживання, характер професійної діяльності, стать, вік пацієнтів зі злоякісними захворюваннями нирки.
Виявлено, що з 1988 по 2004 р. кількість хворих на рак нирки становила 3–5 випадків, а починаючи з 2005 р. вона збільшилася у 3–4 рази. Нерівномірність розповсюдження онкологічних захворювань у різних районах переконливо свідчить про зв’язок виникнення раку зі станом екології. Достовірним показником служать відомості про підвищення частоти захворювань серед жителів міста — 81 (62,3%) особа порівняно з сільськими мешканцями — 49 (37,7%) хворих.
Ці дані наводять на думку про значний вплив атмосферного забруднення міської місцевості на відміну від сільської, спричиненого багатьма шкідливими факторами: численними токсичними відходами промислових підприємств, автотранспортом, викидними газами, які постійно надходять в атмосферу, прогресуючим забрудненням джерел водопостачання через навколишнє середовище, а також господарсько-побутові та промислові стоки тощо. Підтвердженням цього факту є те, що 98 (75,4%) хворих на рак нирки працювали на промислових об’єктах міста і 32 (24,6%) були зайняті в сільському господарстві.
Результати досліджень захворюваності на злоякісні новоутворення нирки серед вікових груп такі: у віці 20–30 років виявлено 2 (1,5%) пацієнти, 31–40 — 6 (4,6%), 41–50 — 28 (21,5%), 51–60 — 44 (33,8%), 61–70 — 37 (28,5%), 71–80 — 13 (10%). Як свідчать дані, найбільша кількість хворих припадає на осіб на 5–7-му десятку життя.
Встановлено, що чоловіки хворіють значно частіше (92–70,7%), ніж жінки (38–29,2%). Водночас беззаперечної закономірності впливу професійної діяльності на частоту виникнення нирково-клітинного раку в тій чи іншій групі пацієнтів не виявлено.
Проведені дослідження дають підставу стверджувати, що соціально-екологічні проблеми не втрачають своєї актуальності в етіології злоякісних новоутворень нирки. Тому наразі провідною метою залишається охорона навколишнього середовища від факторів, що викликають пухлини, та профілактика канцерогенезу.
Результати резекції нирки при пухлині діаметром більше 7 см
Е.О. Стаховський, Ю.В. Вітрук, О.А. Войленко, О.Е. Стаховський, П.С. Вукалович, О.В. Буйвол
Відділення пластичної та реконструктивної онкоурології, Національний інститут раку, Київ, Україна
Основним методом лікування пацієнтів із пухлинами діаметром >7 см є радикальна нефректомія, однак останні дослідження довели доцільність органозберігаючого лікування в такій ситуації, перевагою якого є можливість збереження функції обох нирок, особливо у пацієнтів із патологією контралатеральної нирки та вісцеральними метастазами.
Мета дослідження — встановити показання до резекції нирки при пухлині розміром >7 см та оцінити анатомічні та функціональні результати.
Проведено аналіз лікування 64 хворих на нирково-клітинний рак, яким виконано резекцію нирки при пухлині діаметром >7 см. Вік хворих — від 19 до 79 років (51,6±13,8 року). Чоловіків було 39 (60,9%), жінок — 25 (39,1%). Розмір пухлини становив 71–208 мм (92,4±24,8 мм). Загальна сума балів за R.E.N.A.L. score — від 6 до 12 (9,3±1,8), причому пацієнти високого ризику становили 53,1%. Об’єм функціонуючої паренхіми нирки на боці ураження коливався від 55 до 88% (69,3±9,4%).
Загальна швидкість клубочкової фільтрації (ШКФ) становила 87,5±20,6 мл/хв (з розрахунку на 1,73 м2 площі тіла), а на боці ураження — 40,6±12,6 мл/хв.
У 29 (45,3%) хворих резекцію виконано за абсолютними показаннями, у 15 (23,4%) — при метастатичній хворобі, яка мала циторедуктивний характер і потребувала призначення подальшого лікування.
У всіх вищеописаних хворих та в решті 20 (31,3%) випадках, незважаючи на досить великий розмір пухлини, завдяки зручній для резекції локалізації основним показанням до її проведення був об’єм збереженої паренхіми >55%.
У всіх випадках резекцію нирки виконували відкритим методом; у 20 (31,3%) хворих — під загальною ішемією, яка тривала від 4 до 25 хв (13,1±5,8 хв). Рівень крововтрати становив від 100 до 2500 мл (550±450 мл), у 5 (7,8%) пацієнтів необхідним було переливання крові.
Відновлення цілісності порожнинної системи нирки шляхом накладання дворядного шва проведено у 52 (81,2%) хворих, при цьому інтраопераційне антеградне стентування нирки виконано в 3 (4,7%) випадках. У 4 (6,3%) пацієнтів проведено спленектомію, у 1 (1,6%) випадку — резекцію хвоста підшлункової залози.
У післяопераційний період розвинулося тільки 6 (9,4%) випадків ускладнень: у 3 (4,7%) діагностовано пієлонефрит з гіпертермією тривалістю більше 5 діб, ще у 3 (4,7%) — сечову норицю, яку було ліквідовано стентуванням нирки.
Період спостереження за хворими становив від 3 до 70 міс (26,2±18,0 міс). Протягом цього часу загинули 4 (6,3%) пацієнти з метастатичним раком від прогресування основного захворювання через 3; 5; 6 та 31 міс відповідно.
Місцевий рецидив діагностовано у 6 (9,4%) хворих упродовж 12–32 міс після резекції, що стало поштовхом до виконання нефректомії у 4 (6,3%) пацієнтів, ще у 2 (3,1%) — призначення таргетної терапії. Прогресування захворювання у вигляді метастазування в легені діагностовано у 2 (3,1%) пацієнтів, що також слугувало причиною призначення таргетної терапії.
При порівнянні доопераційної загальної ШКФ з відповідним показником через 3 міс та 1 рік після операції статистично достовірного його зниження не виявлено (через 3 міс — на 9,3% до рівня 79,4±16,9 мл/хв, через 1 рік — на 8% до рівня 80,5±21,8; р>0,07), що було пов’язано із компенсаторними механізмами. Проте при зіставленні ШКФ на боці ураження отримано статистично достовірне її зниження як через 3 міс, так і через 1 рік після операції (відповідно на 33% до рівня 27,2±8,3 мл/хв та на 28% до рівня 29,2±11,1 мл/хв; р<0,02), однак функція ураженої нирки була збережена (рисунок).
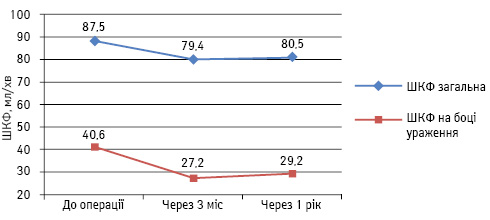
Рисунок. ШКФ пацієнтів до та після проведення резекції нирки
Резекція нирки при пухлині діаметром >7 см може бути виконана за наявності об’єму функціонуючої паренхіми на боці ураження >55% та локалізації утворення в полюсі нирки чи латерально, що дозволить зберегти її функцію в післяопераційний період при низьких показниках інтра- (7,9%) та післяопераційних (9,4%) ускладнень і місцевого рецидиву (9,4%).
Роль резекції нирки в циторедуктивній хірургії хворих на метастатичний нирково-клітинний рак
О.А. Войленко, О.Е. Стаховський, М.В. Пікуль, Ю.В. Вітрук, Е.О. Стаховський
Відділення пластичної та реконструктивної онкоурології, Національний інститут раку, Київ, Україна
Стандартною терапією хворих на метастатичний нирково-клітинний рак (мНКР) залишаються циторедуктивна нефректомія (цНЕ) та таргетна терапія. Однак виконання цНЕ може призвести до розвитку ниркової недостатності, що негативно вплине на ефективність проведення таргетної терапії. Важливим кроком, що дозволяє уникнути такої ситуації є проведення циторедуктивної резекції нирки (цРН), яка поряд з аналогічними онкологічними результатами дозволяє зберегти паренхіму нирки та значно покращити її функцію. Тому метою роботи було проаналізувати онкологічну ефективність цРН в лікуванні хворих на мНКР.
Ретроспективному аналізу підлягали результати лікування 116 пацієнтів із мНКР, прооперованих в Національному інституті раку в період з 2008 по 2014 р. Середній вік хворих становив 55,9±6,4 року. цРН виконано у 44 (37,9%) хворих, а цНЕ — у 72 (62,1%). В обох групах проведено аналіз клінічних даних та побудовано криві виживаності.
Тривалість спостереження за всіма пацієнтами становила 19,3±12 (від 3 до 65) міс. При порівнянні груп цРН та цНЕ не виявлено статистично достовірної різниці за віком, ECOG статусом, тривалістю спостереження, використанням таргетної терапії, об’ємом інтраопераційної крововтрати, передопераційним рівнем креатиніну, а також за тривалістю післяопераційного ліжко-дня. Групи різнилися за розмірами пухлини: 59,3±27,3 мм — в групі цРН і 80,4±36,5 мм — в групі цНЕ (р<0,001). Криві виживаності за Капланом — Мейєром наведено на рисунку.
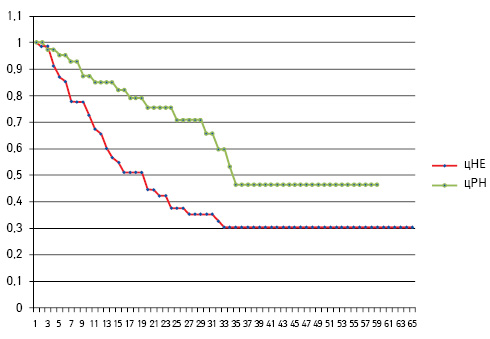
Рисунок. Криві виживаності хворих на мНКР залежно від виду оперативного втручання
Відмічено достовірну різницю виживаності на користь групи цРН (р=0,007). Медіана загальної виживаності для цРН становила 35 міс проти 16 міс для групи цНЕ. При цьому рівень 2-річної виживаності досяг 75,6% у групі цРН проти 37,4% в групі цНЕ.
Проведений аналіз онкологічної ефективності свідчить, що застосування цРН в лікуванні хворих на мНКР дозволяє вдвічі підвищити як медіану загальної виживаності, так і рівень 2-річної виживаності порівняно з пацієнтами, у яких проведено цНЕ.
Выполнимость поперечного тоннеля под устьями главных печеночных вен и piggyback мобилизации печени при удалении опухолевых тромбов нижней полой вены
В.Н. Лесовой1, Д.В. Щукин1, И.А. Гарагатый1, Н.Н. Поляков2, Г.Г. Хареба1
1Харьковский национальный медицинский университет, Харьков, Украина
2Коммунальное учреждение здравоохранения «Областной центр урологии и нефрологии им. В.И. Шаповала»,
Харьков, Украина
Проведен анализ эффективности новой методики тромбэктомии, включающей формирование поперечного тоннеля под устьями главных печеночных вен.
В исследование включены 23 пациента, у которых применяли радикальную нефрэктомию с удалением опухолевых тромбов ретропеченочного или супрадиафрагмального отдела нижней полой вены без искусственного кровообращения. У 15 больных использовали технику piggyback мобилизации печени, у 8 — методику создания поперечного тоннеля под устьями главных печеночных вен.
Успешно выполнить piggyback мобилизацию удалось в 12 (80,0%) случаях, тогда как формирование тоннеля было возможно в 4 (50,0%). Продолжительность этапа piggyback мобилизации печени была значительно больше, чем время формирования тоннеля. Частота кровотечений и их объем были сходны в обеих группах.
Формирование поперечного тоннеля рекомендуется, когда ретропеченочный отдел нижней полой вены охвачен печенью менее чем на 1/2 длины ее окружности или в ситуациях, когда хирург полностью уверен в возможности его выполнения.














Leave a comment