Локальний контроль і фактори ризику виникнення рецидиву раку прямої кишки
Колесник А.А., Безносенко А.П., Шудрак А.А., Махмудов Д.Е.
Резюме. Проблема підвищення ефективності лікування хворих на рак прямої кишки зумовлена значним зростанням захворюваності (20,1 випадку на 100 тис. населення у 2004 р., 21,2 випадку — у 2013 р.), низькою 5-річною виживаністю (31,2% — в Україні, 38,8–59,9% — у країнах Європи, 65,0% — у США, 2008 р.), недостатньою кількістю радикальних оперативних втручань, високою частотою рецидивів, складністю соціальної та трудової реабілітації. Незважаючи на вдосконалення методів терапії, смертність хворих на рак прямої кишки посідає друге місце у структурі загальної смертності від злоякісних новоутворень.

ПРОГНОСТИЧНІ ФАКТОРИ ЛОКАЛЬНОГО РЕЦИДИВУ РАКУ ПРЯМОЇ КИШКИ
Найважливішими прогностичними факторами в лікуванні хворих на рак прямої кишки (РПК) після резекції пухлини є патогістологічна стадія та морфологічний варіант новоутворення [1]. При цьому загалом віддалені результати лікування пацієнтів із РПК гірші, ніж ефекти терапії при раку ободової кишки [2]. Роль біологічних, генетичних та інших гістозалежних чинників прогнозування перебігу РПК визначена в 1999 р. на Prognostic Factors Consensus Conference [1]:
- категорія 1 — найважливіші фактори, підтверджені дослідженнями, статистично достовірними та широко застосовуваними для прийняття рішень при лікуванні пацієнтів;
- категорія 2а — добре обґрунтовані біологічні чи клінічні прогностичні фактори відповіді на лікування. Їх рекомендують до включення у висновок патогістологічного дослідження, проте їхня важливість не підтверджена дослідженнями достатньої статистичної ваги;
- категорія 2б — перевірені за даними численних досліджень фактори, недостатні для включення до категорій 1 та 2а;
- категорія 3 — фактори, недостатньо досліджені для визначення їхньої прогностичної значущості;
- категорія 4 — досліджені фактори, для яких доведена відсутність прогностичного значення.
До категорії 1 відносять кілька факторів, що детально розглянуті нижче.
Локальне розповсюдження пухлини незалежно впливає на віддалені результати лікування [2–4]. Але існують значні труднощі у визначенні інфільтрації серозної оболонки кишки, що призводять до «недостадіювання» пухлини. Наприклад, при цитологічному дослідженні виявляють злоякісні клітини лише у 26% хворих, які були гістологічно стадійовані як рТ3 [5, 6].
Загальноприйнятого визначення локальної перитонеальної інвазії не існує, її діагностують за наявності будь-якого з нижчеперелічених факторів:
- мезотеліальна запальна або гіперпластична реакція пухлинних клітин поблизу серозної оболонки;
- наявність пухлини та запальної реакції по серозній поверхні, мезотеліальна гіперплазія, ерозія чи виразкування;
- вільні пухлинні клітини по серозній поверхні, що призводять до виразкування вісцеральної очеревини.
Усі три типи перитонеальної інвазії відповідають стадії Т4 пухлини та вкрай негативно впливають на віддалений прогноз [1, 5]. Наявність вільних пухлинних клітин вірогідніше прогнозує інтраперитонеальне поширення [5].
Другий фактор, який належить до першої прогностичної категорії, — ураження регіонарних лімфатичних вузлів (більш значущою є тільки наявність віддалених метастазів), що є абсолютним показанням до ад’ювантної терапії. Для РПК частота ураження регіонарних лімфатичних вузлів перебуває у прямій залежності від глибини трансмуральної інвазії та ступеня диференціювання пухлини. Важливим прогностичним фактором є кількість уражених лімфатичних вузлів (N1–N2 категорії) [7–9]. Також на віддалені результати впливає загальна кількість видалених лімфатичних вузлів під час резекції як при ІІ, так і ІІІ стадії РПК [10–15].
Важливим із досліджених прогностичних чинників є коефіцієнт ступеня ураження регіонарних лімфатичних вузлів — lymph node ratio (LNR; відношення кількості уражених до кількості видалених лімфатичних вузлів). Так, при LNR >0,05 1-річна виживаність сягає 79%, а при LNR <0,4 — не перевищує 50% [16, 17].
Третій фактор першої прогностичної категорії — наявність резидуальної пухлини [1, 4, 18, 19]. В основному наявність резидуальної пухлинної тканини залежить від статусу циркулярного краю резекції [20], для визначення якого використовують R-класифікацію:
R0 — гістологічно підтверджена відсутність пухлинних клітин у всіх краях резекції;
R1 — гістологічно підтверджена мікроскопічна інвазія по краю резекції;
R2 — макроскопічно візуалізована під час операції залишкова пухлинна тканина (первинна пухлина, регіонарні лімфатичні вузли).
Також до першої категорії прогностичних факторів належать наявність сателітних мезентеріальних пухлинних вузлів, мікрометастазів у лімфатичних вузлах, судинної інвазії та високий рівень сироваткового раково-ембріонального антигену.
Незначну прогностичну роль (категорії 2а–3) відіграють:
- ступінь диференціювання пухлини;
- регресія пухлини після неоад’ювантної терапії;
- гістологічний тип;
- периневральна інвазія;
- молекулярні маркери;
- k-ras статус, фокальне нейроендокринне диференціювання;
- проліферативна активність.
Доведено відсутність прогностичної значущості (категорія 4) стосовно розміру пухлини [4, 21].
ЗНАЧЕННЯ НЕОАД’ЮВАНТНОЇ ПРОМЕНЕВОЇ ТЕРАПІЇ У ПРОФІЛАКТИЦІ ЛОКАЛЬНОГО РЕЦИДИВУ РПК
В останні 20 років проведено кілька багатоцентрових рандомізованих досліджень з вивчення впливу неоад’ювантної променевої терапії (НПТ) на частоту локальних рецидивів, віддалених метастазів, тривалість безрецидивного періоду. Проте існують різні методики променевої терапії (ПТ) — за дозами і схемами, обсягом опромінення і тривалістю періоду між курсом опромінення та оперативним втручанням, що спричиняють значну розбіжність результатів та ускладнюють їхню інтерпретацію [22–28].
За результатами рандомізованого дослідження, проведеного Swedish Rectal Cancer Trial, інтенсивний курс НПТ до сумарної вогнищевої дози (СВД) 25 Гр (5 фракцій по 5 Гр) у лікуванні 1168 хворих на РПК вірогідно зменшує кількість локальних рецидивів пухлини з 27 до 11%.
Заслуговують на увагу результати ретроспективного дослідження, проведеного в США E.T. Castaldo та співавторами [29], які взяли дані бази SEER (Surveillance, Epidemiology and End Results) Національного інституту раку США (US National Cancer Institute). Хворих на РПК І–ІІІ стадії (10 971 особа) розподілено на дві групи: у 1-й було 7211 пацієнтів із РПК І стадії, які отримували лише хірургічне лікування; у 2-й — 3760 осіб із РПК ІІ–ІІІ стадії, які отримували НПТ. Під час післяопераційного морфологічного дослідження «downstaging» зниження стадії виявили у 792 (21%) пацієнтів (до операції — ІІ–ІІІ стадія захворювання, після операції — 0–І). 5-річна виживаність у групі хворих, у яких відповідь на ПТ оцінювали як регресію чи повну регресію, виявилася вищою на 16% (р<0,001) порівняно з групою пацієнтів, у яких не було позитивної відповіді на НПТ, та становила 94%, що відповідає результатам виживаності у 1-й групі пацієнтів із І стадією захворювання (97%). Інші результати цього дослідження свідчать про необхідність точного доопераційного стадіювання та перспективи проведення адекватної ПТ у хворих на резектабельний РПК [30].
У спільному дослідженні групи нідерландських клінік проаналізовано результати лікування 1417 пацієнтів із неметастатичним РПК з метою оцінки факторів, що впливають на ризик виникнення локальних рецидивів, їх локалізацію, а також значення повного видалення мезоректума та НПТ у профілактиці останніх. Сформовано дві групи хворих: у 1-й 713 пацієнтів отримували НПТ у СВД 25 Гр (5 сеансів по 5 Гр) з подальшим хірургічним втручанням в обсязі тотальної мезоректумектомії (ТМЕ); у 2-й групі 704 хворим було проведене тільки хірургічне лікування в обсязі ТМЕ. Наступним етапом проаналізовано частоту та розміщення локальних рецидивів в обох групах. Рецидиви розподілено за анатомічним принципом: пресакральні, передні, латеральні, промежинні та рецидиви зони анастомозу. За 7-річний період спостереження виявлено 114 рецидивів раку: мінімальний період спостереження становив 1,5 року, максимальний — 9,8 року. У групі комбінованого лікування частота локальних рецидивів сягала 4,6%, у групі хірургічного лікування — 11%. При цьому час до виникнення рецидиву пухлини в групі комбінованого лікування становив 2,6 року порівняно з 1,5 року в іншій групі. Віддалені метастази на момент виявлення локального рецидиву діагностували у 55% пацієнтів, які отримували передопераційну ПТ, і у 41% хворих, які одержали хірургічне лікування.
Основними факторами ризику розвитку рецидиву були низька локалізація пухлини, висока стадія захворювання та R1-резекція. Найчастіше рецидиви раку в обох досліджуваних групах локалізувалися в пресакральній ділянці. Найбільш ефективною НПТ була у профілактиці передніх рецидивів: 5-річні показники в 1-й групі становили 0,7% та 1,9% — у 2-й групі. Ефективність ПТ також підтверджена зменшенням кількості рецидивів у ділянці анастомозу: 5-річні показники в 1-й групі становили 0,7%, у 2-й — 2,7%. Відзначимо, що, незважаючи на наявність пухлинних клітин по циркулярному краю резекції, тільки у 46 (17,2%) із 267 таких пацієнтів виникли місцеві рецидиви. Вочевидь, залучення краю резекції є далеко не єдиним механізмом розвитку рецидиву РПК.
Розмір дистального краю резекції <2 см був вірогідно пов’язаний з підвищеним ризиком виникнення рецидиву, але переважно в групі хворих із наявністю ураження лімфовузлів параректальної клітковини: 19% — при N0 порівняно з 94,3% — при N+ у групі хірургічного лікування та 11,8% — при N0 порівняно з 35,8% — при N+ у групі НПТ. Загальний ризик виникнення рецидиву в групі хворих, які отримували комбіноване лікування, був досить низьким за винятком випадків, коли дистальний край резекції становив <5 мм.
Підтверджено необхідність проведення НПТ абсолютно усім хворим на РПК, незалежно від типу хірургічного втручання та використання техніки ТМЕ. Оскільки більшість локальних рецидивів виникла у групі з поширеними (Т3–4N+M0) стадіями захворювання, автори зробили припущення про необхідність розширення показань до проведення тривалих курсів передопераційної променевої чи хіміопроменевої терапії замість стандартної по 5 Гр протягом 5 сеансів. Також у поля опромінення обов’язково мають бути включені лімфатичні вузли латеральної групи, тому що їх ураження констатують у 10–20% випадків.
Особливості топографо-анатомічної зони прямої кишки (ПК) та інфільтративний ріст РПК зумовлюють труднощі як у діагностиці, так і в лікуванні хворих, що актуалізує на сучасному етапі мультидисциплінарний підхід до лікування цієї категорії пацієнтів.
Об’єкт і методи дослідження
З 2008 до 2013 р. проводили мультицентрове рандомізоване дослідження з вивчення ефективності комбінованого лікування хворих на рак нижньоампулярного відділу ПК ІІ–ІІІ стадії (T2–3N0–2M0) із використанням дрібно- або крупнофракційної НПТ.
Критерії включення в дослідження:
- отримана письмова Інформована згода пацієнта;
- морфологічно підтверджена аденокарцинома ПК;
- локалізація пухлини в нижньоампулярному відділі ПК (нижня межа пухлини не вище 6 см від зубчастої лінії);
- стадія онкологічного захворювання T2–3N0–2M0;
- стан пацієнта за ECOG 0–2;
- вік пацієнта ≥18 років.
Критерії виключення з дослідження:
- наявність синхронних віддалених метастазів (М1) на момент початку комбінованого лікування;
- наявність місцево-поширеної пухлини (Т4);
- наявність іншої синхронної/метахронної злоякісної пухлини;
- супутні захворювання, які можуть істотно вплинути на результати дослідження;
- вік <18 років.
Пацієнти, які за результатами проведених обстежень відповідали критеріям включення/виключення, були рандомізовані у дві групи (рис. 1):
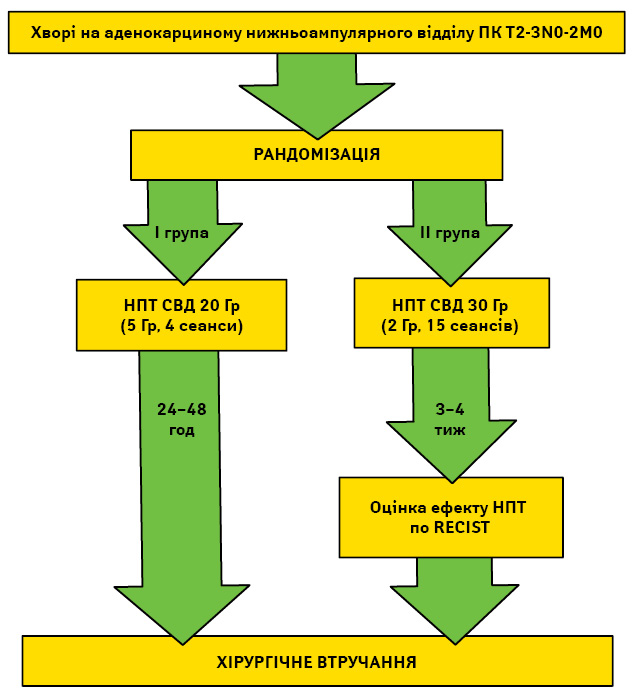
Рис. 1. Дизайн мультицентрового рандомізованого дослідження
- І — 150 хворих, які отримали лікування із застосуванням НПТ у СВД 20 Гр (4 сеанси по 5 Гр) та оперативне втручання на 1–3-тю добу після опромінення;
- ІІ — 101 хворий, які отримали НПТ у СВД 30 Гр (15 сеансів по 2 Гр) з відстроченим оперативним втручанням — не раніше ніж через 21 добу після опромінення.
У дослідження включено 251 пацієнта віком 27–83 роки (середній 66,1±10,6 року): 136 (54,2%) чоловіків та 115 (45,8 %) жінок; різниця між групами за статевим і віковим складом статистично не достовірна (р=0,182).
Діагноз встановлювали на основі загальноклінічних, інструментальних (ректороманоскопія, фіброколоноскопія), променевих (іригоскопія, комп’ютерна томографія (КТ) та магнітно-резонансна томографія (МРТ), трансректальне ультразвукове дослідження (ТРУЗД)) та морфологічного досліджень біопсійного матеріалу.
Прагнучи максимально об’єктивізувати поширеність пухлинного процесу щодо кишкової стінки і навколишніх тканин та визначити можливості радикального хірургічного втручання, ми застосовували МРТ, КТ і ТРУЗД.
Дистанційну НПТ проведено на гамма-терапевтичних установках Рокус-АМ, Тeratron-Elite, Teragam з джерелами випромінювання Со.
У І групі опромінення проводили за методикою крупного фракціонування у разовій вогнищевій дозі (РВД) 4–5 Гр до СВД 20–25 Гр у режимі секторального коливання з полями опромінення 7×12–14 см та з подальшим хірургічним втручанням через 24–48 год. До зони опромінення включали: первинну пухлину, мезоректальну клітковину, ділянки здухвинних лімфатичних вузлів, незмінені ділянки ПК проксимальніше та дистальніше пухлини на 3–5 см.
У ІІ групі дистанційну НПТ проводили з двох зустрічно напрямлених полів (переднє та заднє) розмірами 14×16 см, з ідентичними І групі зонами опромінення упродовж 15 діб у РВД 2 Гр до СВД 30 Гр з подальшим хірургічним втручанням не раніше ніж через 21 добу після опромінення, з урахуванням оцінки ефекту НПТ на пухлину ПК і переоцінки можливості виконання сфінктерозберігальних операцій (СЗО).
Показаннями до СЗО була наявність пухлини ПК, яка, за даними пальцевого ректального, ендоскопічного дослідження, а також МРТ і ТРУЗД, не мала клініко-інструментального підтвердження інвазії в анальний сфінктер (внутрішній та зовнішній) після НПТ. При розміщенні пухлини в безпосередній близькості до анального каналу, але за відсутності інструментального підтвердження інвазії в останній та за можливості R0 резекції виконували проктектомію з колоперіанальним анастомозом без превентивної стоми за розробленою в Національному інституті раку методикою. Показанням до низької передньої та черевно-анальної резекції була наявність як мінімум 2 см кукси ПК після видалення препарату — для формування степлерного апаратного чи колоректального (анального) анастомозу.
Оцінювали можливість виконання СЗО при досягненні позитивного ефекту НПТ (часткова або повна регресія), у тому числі у хворих із пухлинною інвазією в анальний сфінктер ПК до початку опромінення. Показанням до черевно-промежинної екстирпації ПК було клініко-інструментальне підтвердження пухлинної інвазії в анальний сфінктер. Хворим усіх груп хірургічне втручання виконували за принципами ТМЕ зі збереженням автономних вегетативних (симпатичних і парасимпатичних) нервових сплетінь таза (нижнього гіпогастрального та тазового).
Результати та їх обговорення
Досліджено вплив НПТ на пухлину у хворих, які отримали опромінення СВД 30 Гр (група ІІ) за критеріями RECIST (табл. 1).
Таблиця 1. Регресія пухлини після НПТ у ІІ групі
|
Оцінка відповіді |
Кількість хворих, n (%) n=101 |
Диференціювання пухлини |
Кількість випадків, n |
| Повна регресія | 4 (4,0) | G1 | 1 |
| G2 | 3 | ||
| Часткова регресія | 26 (25,7) | G1 | 2 |
| G2 | 19 | ||
| G3 | 5 | ||
| Стабілізація | 71 (70,3) | G1 | 3 |
| G2 | 57 | ||
| G3 | 5 | ||
| G4 + Gx + слизова оболонка | 6 | ||
| Прогресування | 0 (0,0) |
У 29,7% пацієнтів об’єктивний ефект після НПТ зареєстровано у вигляді часткової чи повної регресії пухлини (за рахунок зниження показника Т), у 71 (70,3%) — незначне зменшення пухлини. За допомогою післяопераційного морфологічного дослідження підтверджено повну регресію пухлини ПК у 3,9% випадків. Зменшення кількості хворих, у яких після оперативного втручання морфологічно не доведено метастатичного ураження регіонарних лімфатичних вузлів після НПТ, підтверджує downstaging ефект дрібнофракційного опромінення. Так, з 25,7% пацієнтів, у яких відзначено збільшення лімфатичних вузлів до НПТ, тільки у 15,9% морфологічно підтверджено метастатичне ураження.
Тривалість спостереження за хворими І та ІІ груп становила 40,9±18,8 міс (медіана — 42 (7–75) міс) та 39,9±18,4 міс (медіана — 19 (5–71) міс) відповідно (р=0,809).
Проведено аналіз безрецидивної виживаності у групах дослідження, результати якого графічно представлено на рис. 2.
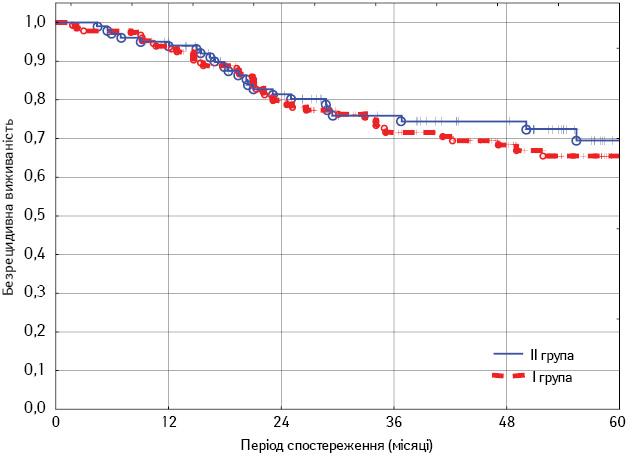
Рис. 2. Безрецидивна виживаність хворих у групах (р=0,235)
При аналізі результатів, наведених у табл. 2, виявлено відсутність статистично достовірної різниці в показниках безрецидивної виживаності в групах (Cox’s F-Test=1,19; р=0,235), проте виживаність має тенденцію до підвищення в групі із застосуванням НПТ у дозі 30 Гр. Так, 3-річна безрецидивна виживаність у I групі становила 73,6%, у II групі — 75,8%. Натомість 5-річна виживаність у I групі сягала 65,3%, II групі — 69,7%.
Таблиця 2. 5-річна безрецидивна виживаність (%) пацієнтів у групах за стадіями захворювання
| Стадія захворювання | Група хворих, % | р | |
| І (n=150) | ІІ (n=101) | ||
| ІІ | 72,1±5,1 | 75,5±4,9 | р=0,285 |
| ІІІ | 37,4±7,1 | 38,4±6,4 | р=0,460 |
| ІІ + ІІІ | 65,3±4,6 | 69,7±3,8 | р=0,235 |
5-річну безрецидивну виживаність за стадіями захворювання подано в табл. 2.
Оцінено частоту виникнення локорегіонарних рецидивів та власне безрецидивну виживаність хворих на рак нижньоампулярного відділу ПК ІІ–ІІІ стадії у групах. Локальні рецидиви виявлено у 18 (12,0%) пацієнтів І групи в середньому через 22,3±13,7 міс (розкид 3–52 міс), у групі ІІ — у 5 (4,9%) у середньому через 15,4±6,8 міс (розкид 4–25); показники статистично відрізняються (р=0,041). Усі рецидиви виникли у хворих з факторами ризику (параметр Т3N+G3).
Встановлено статистично значущу різницю між рівнями загальної виживаності в досліджуваних групах (Cox’s F-Test=1,64; p=0,045). Кращі показники зафіксовано у хворих, у яких застосовано НПТ у режимі 30 Гр дрібними фракціями. Так, 3-річна загальна виживаність у I групі становила 83,9%, а в II групі — 89,7%. 5-річна загальна виживаність досягла 70,6% у I групі, 79,8% — у II групі (Cox’s F-Test=1,64; p=0,045) (рис. 3, а). Таку саму тенденцію відзначено при дослідженні хворих із ІІ стадією: 76,9% — у І групі та 83,7% — у ІІ групі (Cox’s F-Test=2,04; р=0,026). Серед пацієнтів із РПК ІІІ стадії не відмічено достовірної різниці в показниках 5-річної загальної виживаності між групами (50,1 та 52,1% відповідно) (Cox’s F-Test=1,2; р=0,378).
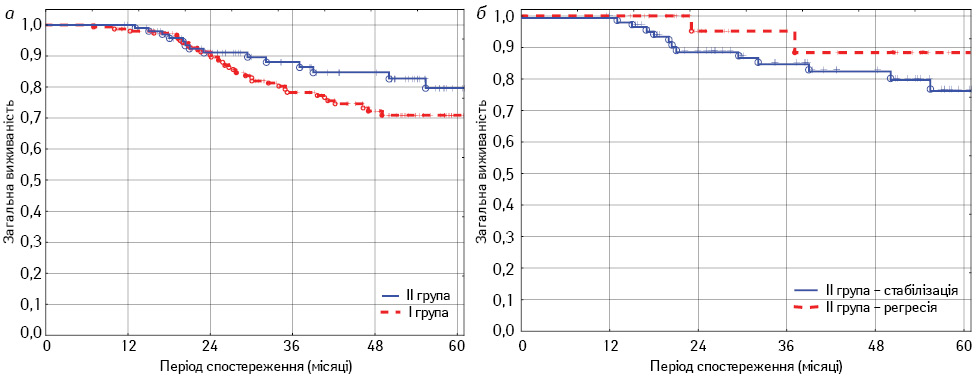
Рис. 3. Загальна виживаність хворих за Капланом — Мейєром: а — показник у хворих у групах (Cox’s F-Test=1,64; p=0,045);б — показник у хворих ІІ групи з повною чи частковою регресією та зі стабілізацією процесу (Cox’s F-Test=2,9; р=0,038)
Підвищення 5-річної загальної виживаності в ІІ групі пояснюємо позитивним впливом часткової чи повної регресії на віддалені результати лікування.
Так, 5-річна загальна виживаність у хворих із повною чи частковою регресією була значно вищою, ніж у пацієнтів зі стабілізацією, — 88,6 і 76,9% відповідно (Cox’s F-Test=2,9; р=0,038) (рис. 3, б). Достовірної різниці щодо показників загальної виживаності хворих після крупно- та дрібнофракційного опромінення, які не мали позитивної відповіді на НПТ, не отримано (Cox’s F-Test=1,3; р=0,191).
Висновки
За результатами проведеного дослідження можна зробити висновок, що у 30% хворих об’єктивного ефекту лікування після дрібнофракційної НПТ досягнуто у вигляді часткової чи повної регресії пухлини за рахунок зниження показника Т, що сприяло підвищенню ефективності лікування: 5-річна загальна виживаність пацієнтів із РПК з повною чи частковою регресією становить 88,6%, при стабілізації — 76,9%.
При аналізі власне безрецидивної виживаності не виявлено значущої різниці (р=0,235), хоча частота локальних рецидивів достовірно вища в I групі порівняно з ІІ групою — 11,9 і 4,9% відповідно.
Комбіноване лікування хворих на рак нижньоампулярного відділу ПК ІІ–ІІІ стадії із застосуванням НПТ дрібними фракціями є більш ефективним методом, який надає можливість знизити частоту локальних рецидивів удвічі (11,9 і 4,9% відповідно) та підвищити 5-річну загальну виживаність на 9% (з 70,6 до 79,8%) (p=0,045) порівняно із крупнофракційним опроміненням.
Список використаної літератури
1. Compton C.C., Fielding L.P., Burgart L.J. et al. (2000) Prognostic factors in colorectal cancer. College of American Pathologists Consensus Statement 1999. Arch. Pathol. Lab. Med., 124: 979.
2. O’Connell J.B., Maggard M.A., Ko C.Y. (2004) Colon cancer survival rates with the new American Joint Committee on Cancer sixth edition staging. J. Natl. Cancer Inst., 96: 1420.
3. Ryan R., Gibbons D., Hyland J.M. et al. (2005) Pathological response following long-course neoadjuvant chemoradiotherapy for locally advanced rectal cancer. Histopathology, 47: 141.
4. Compton C.C. (2000) Updated protocol for the examination of specimens from patients with carcinomas of the colon and rectum, excluding carcinoid tumors, lymphomas, sarcomas, and tumors of the vermiform appendix: a basis for checklists. Cancer Committee. Arch. Pathol. Lab. Med., 124: 1016.
5. Wiggers T., Arends J.W., Volovics A. (1988) Regression analysis of prognostic factors in colorectal cancer after curative resections. Dis. Colon. Rectum., 31: 33.
6. Tominaga T., Sakabe T., Koyama Y. et al. (1996) Prognostic factors for patients with colon or rectal carcinoma treated with resection only. Five-year follow-up report. Cancer, 78: 403.
7. Edge S.B., Byrd D.R., Compton C.C. et al. (2010) AJCC (American Joint Committee on Cancer) Cancer Staging Manual, 7 ed. Springer : New York: 143.
8. Shepherd N.A., Baxter K.J., Love S.B. (1997) The prognostic importance of peritoneal involvement in colonic cancer: a prospective evaluation. Gastroenterology, 112: 1096.
9. Newland R.C., Dent O.F., Lyttle M.N. et al. (1994) Pathologic determinants of survival associated with colorectal cancer with lymph node metastases. A multivariate analysis of 579 patients. Cancer, 73: 2076.
10. Syk E., Glimelius B., Nilsson P.J. (2010) Factors influencing local failure in rectal cancer: analysis of 2315 patients from a population-based series. Dis. Colon. Rectum., 53(5): 744–752.
11. Hida J., Yasutomi M., Maruyama T. et al. (1997) Lymph node metastases detected in the mesorectum distal to carcinoma of the rectum by the clearing method: justification of total mesorectal excision. J. Am. Coll. Surg., 184: 584.
12. Johnson P.M., Porter G.A., Ricciardi R., Baxter N.N. (2006) Increasing negative lymph node count is independently associated with improved long-term survival in stage IIIB and IIIC colon cancer. J. Clin. Oncol., 24: 3570.
13. Chen S.L., Bilchik A.J. (2006) More extensive nodal dissection improves survival for stages I to III of colon cancer: a population-based study. Ann. Surg., 244: 602.
14. Swanson R.S., Compton C.C., Stewart A.K., Bland K.I. (2003) The prognosis of T3N0 colon cancer is dependent on the number of lymph nodes examined. Ann. Surg. Oncol., 10: 65.
15. Chang G.J., Rodriguez-Bigas M.A., Skibber J.M., Moyer V.A. (2007) Lymph node evaluation and survival after curative resection of colon cancer: systematic review. J. Natl. Cancer Inst., 99: 433.
16. Compton C.C. (2007) Optimal pathologic staging: defining stage II disease. Clin. Cancer Res., 13: 6862s.
17. Baxter N.N., Ricciardi R., Simunovic M. et al. (2010) An evaluation of the relationship between lymph node number and staging in pT3 colon cancer using population-based data. Dis. Colon. Rectum., 53: 65.
18. Matzel K.E., Stadelmaier U., Muehldorfer S., Hohenberger W. (1997) Continence after colorectal reconstruction following resection: impact of level of anastomosis. Int. J. Colorectal. Dis., 12: 82.
19. Compton C., Fenoglio-Preiser C.M., Pettigrew N., Fielding L.P. (2000) American Joint Committee on Cancer Prognostic Factors Consensus Conference: Colorectal Working Group. Cancer, 88: 1739.
20. National Comprehensive Cancer Network: National Comprehensive Cancer Network clinical practice guidelines (2015). Rectal cancer (http://www.nccn.org).
21. Rödel C., Martus P., Papadoupolos T. et al. (2005) Prognostic significance of tumor regression after preoperative chemoradiotherapy for rectal cancer. J. Clin. Oncol., 23: 8688.
22. van de Velde C., Boelens P., Borras G. et al. (2014) EURECCA colorectal: Multidisciplinary management: European consensus conference colon & rectum. Eur. J. Cancer, 50(1): 1.
23. Baker B., Salameh H., Al-Salman M. et al. (2012) How does preoperative radiotherapy affect the rate of sphincter-sparing surgery in rectal cancer? Sur. Oncol., 21: 103–109.
24. Van Cutsem E., Dicato M., Haustermans K. et al. (2008) The diagnosis and management of rectal cancer: expert discussion and recommendations derived from the 9 World Congress on Gastrointestinal Cancer, Barcelona, 2007. Ann. Oncol., 19 (suppl. 6): vi1–vi8.
25. Fazio V.W., Zutshi M., Remzi F.H. et al. (2007) A randomized multicenter trial to compare long-term functional outcome, quality of life, and complications of surgical procedures for low rectal cancer. Ann. Surg., 246(3): 481–490.
26. Кикоть В.А. (2003) Сравнительная эффективность различных методов хирургического, комбинированного комплексного лечения больных раком прямой кишки. Клін. хірургія, 3: 36–39.
27. Marijnen C.A., Nagtegaal I.D., Kapiteijn E. et al. (2003) Cooperative investigators of the Dutch Colerectal Cancer Group. Radiotherapy does not compensate for positive resection margins in rectal cancer patients: report of a multicenter randomized trial. Int. J. Radiat. Oncol. Biol. Phys., 55(5): 1311–1320.
28. Барсуков Ю.А., Николаев А.В., Тамразов Р.И., Ткачев С.И. (2002) Сравнительный анализ хирургического и комбинированного лечения больных операбельным раком прямой кишки (результаты рандомизированного исследования). Практ. онкол., 3(2): 105–113.
29. Castaldo E.T., Parikh A.A., Pinson C.W. et al. (2009) Improvement of survival with response to neoadjuvant radiation therapy for rectal cancer. Arch. Surg., 144(2): 129–134.
30. Тюряева Е.И. (2008) Химиолучевое лечение рака прямой кишки. Практ. онкол., 9(1): 31–38.
Локальный контроль и факторы риска возникновения рецидива рака прямой кишки
Национальный институт рака, Киев
Резюме. Проблема повышения эффективности лечения больных раком прямой кишки обусловлена значительным ростом заболеваемости (20,1 случая на 100 тыс. населения в 2004 г., 21,2 — в 2013 г.), низкой 5-летней выживаемостью (31,2% — в Украине, 38,8–59,9% — в странах Европы, 65,0% — в США, 2008 г.), недостаточным количеством радикальных оперативных вмешательств, высокой частотой рецидивов, сложностью социальной и трудовой реабилитации. Несмотря на совершенствование методов терапии, смертность пациентов с раком прямой кишки занимает второе место в структуре общей смертности от злокачественных новообразований.
рак прямой кишки, неоадъювантная лучевая терапия, выживаемость.
Адреса:
Безносенко Андрій Петрович
03022, Київ, вул. Ломоносова, 33/43
Національний інститут раку
E-mail: beznosenko82@gmail.com














Leave a comment