Тричі негативний рак грудної залози: сучасний погляд на проблему
Сивак Л.А., Лялькин С.А., Майданевич Н.Н., Климанов М.Ю., Аскольский А.В., Касап Н.В.
Резюме. Терапія тричі негативного раку грудної залози (ТНРГЗ) залишається однією з найбільш актуальних проблем сучасної онкології. Біологічна агресивність даного підтипу РГЗ поєднується з обмеженістю лікувальних підходів, а також переважним ураженням пацієнток молодого віку. Зі значного арсеналу сучасних методів системної терапії РГЗ для тричі негативного фенотипу сприйнятною є тільки цитостатична терапія. Незважаючи на значну кількість клінічних досліджень, на сьогодні у світі не існує стандартної схеми хіміотерапії даного варіанта РГЗ, а результати лікування залишаються невтішними. Активно впроваджені в останні роки принципи максимальної індивідуалізації терапії при РГЗ даного підтипу не є успішними. У статті представлено огляд найбільш відомих клінічних досліджень останніх років, присвячений неоад’ювантній та ад’ювантній хіміотерапії ТНРГЗ.
Резюме. Терапия трижды негативного рака грудной железы (ТНРГЖ) остается одной из самых актуальных проблем современной онкологии. Биологическая агрессивность данного подтипа РГЖ сочетается с ограниченностью лечебных подходов, а также преимущественным поражением пациенток молодого возраста. Из значительного арсенала современных методов системной терапии РГЖ для трижды негативного фенотипа приемлемым является только цитостатическая терапия. Несмотря на значительное количество проводимых клинических исследований, на сегодня в мире не существует стандартной схемы химиотерапии при данном варианте РГЖ, а результаты лечения остаются неутешительными. Активно внедряемые в последние годы принципы максимальной индивидуализации терапии при РГЖ данного подтипа не являются успешными. В статье представлен обзор наиболее представительных клинических исследований последних лет, посвященный неоадъювантной и адъювантной химиотерапии ТНРГЖ.
 Рак грудной железы (РГЖ) в последние годы как в Украине, так и в большинстве стран Западной Европы и Северной Америки остается самым распространенным злокачественным заболеванием у женщин. Вместе с тем, анализируя показатели выживаемости пациенток с РГЖ за последнее десятилетие, можно сделать вывод о тенденции к улучшению результатов лечения при данной нозологической форме. Так, по данным SEER (Surveillance, Epidemiology and End Results) — статистической базы данных Национального института рака (США), 5-летняя выживаемость при локализованных формах РГЖ составляет 83,4–98,4%, а метастатической — 23,3% [9]. Столь высокие результаты связывают, прежде всего, с достижениями системной терапии РГЖ, в частности с использованием стратегии максимальной индивидуализации терапии РГЖ.
Рак грудной железы (РГЖ) в последние годы как в Украине, так и в большинстве стран Западной Европы и Северной Америки остается самым распространенным злокачественным заболеванием у женщин. Вместе с тем, анализируя показатели выживаемости пациенток с РГЖ за последнее десятилетие, можно сделать вывод о тенденции к улучшению результатов лечения при данной нозологической форме. Так, по данным SEER (Surveillance, Epidemiology and End Results) — статистической базы данных Национального института рака (США), 5-летняя выживаемость при локализованных формах РГЖ составляет 83,4–98,4%, а метастатической — 23,3% [9]. Столь высокие результаты связывают, прежде всего, с достижениями системной терапии РГЖ, в частности с использованием стратегии максимальной индивидуализации терапии РГЖ.
Известным фактом является то, что РГЖ представляет собой гетерогенную группу опухолей. Согласно молекулярно-генетической классификации [16] выделяют 4 основных подтипа РГЖ. Каждый из них имеет свои эпидемиологические особенности, клиническое течение, прогноз и, соответственно, подходы к лечению. Так, при люминальном А подтипе основной акцент в лечении делается на гормонотерапию, при HER-2/neu гиперэкспресии — анти-HER-2/neu терапию (трастузумаб, лапатиниб, пертузумаб и т.д). С эффективностью стратегии воздействия на привычные для РГЖ мишени (рецепторы эстрогенов и прогестерона, онкопротеин HER-2/neu), скорее всего, и связаны успехи терапии РГЖ, достигнутые в последние годы.
Однако все это не относится к базальноподобному РГЖ, лечение которого остается одной из самых больших проблем современной онкологии. Базальноподобный и трижды негативный РГЖ (ТНРГЖ) далеко не всегда являются синонимами, хотя их часто используют как взаимозаменяемые термины. Около 70–75% базальноподобных видов РГЖ имеют тройной негативный фенотип [1, 5, 6, 10]. Приблизительно в 25% случаях трижды негативный рак не является базальноподобным (в эту же группу также входят так называемые редкие гистологические подтипы РГЖ); 15–20% базальноподобных опухолей, в свою очередь, не являются трижды негативными [5, 10]. В научной литературе в последние годы превалирует использование иммуногистохимического термина «трижды негативный», более удобного для интерпретации результатов клинических исследований, так как иммуногистохимические исследования намного доступнее молекулярно-генетических и проводятся почти рутинно. Клинико-эпидемиологические характеристики ТНРГЖ являются достаточно изученными и широко известными. По данным разных авторов [1, 5, 6], частота его составляет от 10 до 20%, чаще встречается у пациенток молодого возраста, факторы риска противоположны люминальным подтипам [5, 6]. В большинстве случаев ТНРГЖ гистологически представлен низкодифференцированной протоковой карциномой. Отличительной особенностью данного вида опухолей являются высокая пролиферативная активность и большая скорость роста [1, 5, 6, 10]. ТНРГЖ отличается агрессивным течением, ранним появлением висцеральных метастазов и, как следствие, неблагоприятным прогнозом. Так, по данным R. Dent [6], медиана времени от выявления прогрессирования процесса до смерти составляет при ТНРГЖ 9 мес по сравнению с 22 мес при люминальных типах. По результатам ретроспективного исследования, проведенного H. Kennecke [10] (изучение архивных данных 3726 пациенток, лечившихся в период с 1986 по 1992 г.), медиана выживаемости при метастатическом ТНРГЖ составляла всего 6 мес, люминальном А подтипе — 2,2 года, люминальном В подтипе — 1,6 года.
Одним из парадоксов ТНРГЖ является сочетание худшей выживаемости с высокой чувствительностью данной опухоли к цитостатикам, особенно показательной при неоадъювантной химиотерапии. В этом плане одним из самых цитируемых исследований является работа K. Liedtke (2008) [14]. Это ретроспективное исследование с участием 1118 пациенток, лечившихся с 1985 по 2004 г. Из них 255 (23%) — с ТНРГЖ. У пациенток с ТНРГЖ отмечена самая высокая чувствительность к химиотерапии (частота полного морфологического ответа 22% в отличие от 11% у остальных типов (р=0,034)). При этом 3-летняя безрецидивная выживаемость составила 63% по сравнению с 76% при других опухолях, а 3-летняя общая выживаемость — 74% против 89%.
На рис. 1 представлены данные о выживаемости пациенток в зависимости от ответа опухоли на неоадъювантную полихимиотерапию (ПХТ). У пациенток с ТНРГЖ с полным морфологическим ответом опухоли 3-летняя общая выживаемость составляла 94%, в то время как у больных с резидуальной опухолью — только 68%. У пациенток с остальными подтипами РГЖ 3-летняя общая выживаемость при полной морфологической регрессии составила 98%. Результатом данного исследования стал важнейший вывод: только пациентки с полным морфологическим ответом имели 3-летнюю общую выживаемость, сопоставимую с таковой при других типах (94% против 98%; р=0,24). Из этого следует, что основной целью неоадъювантной ПХТ при ТНРГЖ является достижение полной морфологической регрессии, а никакой другой результат не может считаться приемлемым [14].
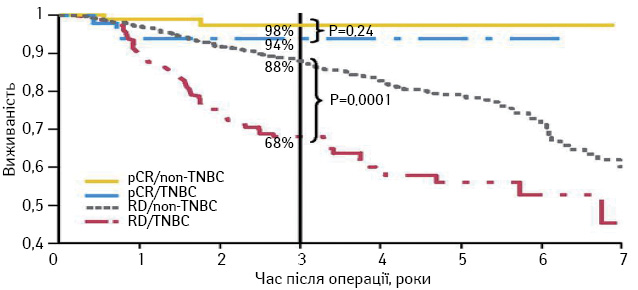
Вопрос оптимальной схемы неоадъювантной ПХТ при ТНРГЖ остается открытым, хотя в рутинной практике распространено использование комбинации антрациклинов и таксанов. Показательным является исследование GEPARTRIO, в котором авторы применяли комбинацию ТАС (доцетаксел, доксорубицин, циклофосфамид) [12]. В исследование было включено 2072 пациентки, из них 509 — с ТНРГЖ (рис. 2). У больных с данным подтипом частота полной морфологической регрессии составила 39% (это самый высокий результат для неоадъювантной ПХТ, полученный в проспективном рандомизированном исследовании с большим объемом выборки).
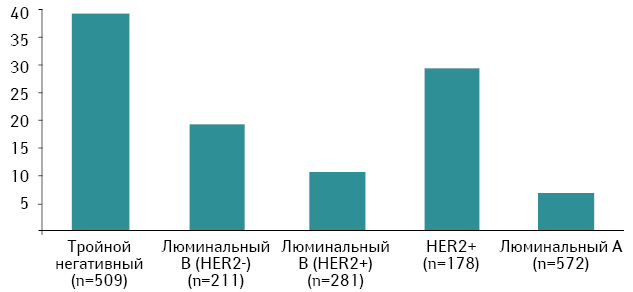
Отдельное внимание в последние годы привлекает использование в неоадъювантной ПХТ ТНРГЖ препаратов платины. Механизм действия препаратов платины заключается в нарушении синтеза ДНК путем образования межнитевых сшивок. В последние годы доказано, что платиночувствительность ТНРГЖ реализуется в большей степени у «наследственных» BRCA-ассоциированных видов рака. Хотя BRCA1/2-зависимые виды РГЖ в общей популяции составляют около 5%, подавляющее большинство их является базальноподобными [10, 15]. В ретроспективном исследовании T. Byrski (2009) проанализирован эффект неоадъювантной ПХТ у 102 пациенток с BRCA-ассоциированным РГЖ. При этом частота полного морфологического ответа составляла только 8% у пациенток, получавших ПХТ по схеме АТ (доцетаксел, доксорубицин), 22% — у больных, лечившихся по схеме FAC (флуороурацил, циклофосфамид, доксорубицин), и 83% женщин, получавших монотерапию цисплатином [3]. При этом, однако, следует отметить небольшое количество наблюдений (группа цисплатина — 12 пациенток) и ретроспективный характер данного исследования.
Обсуждая тему адъювантной химиотерапии РГЖ, невозможно не упомянуть о результатах 2 метаанализов, проведенных EBCTCG (научной группой по изучению раннего РГЖ). Первый из них, опубликованный в 2005 г., включал в себя 194 рандомизированных исследования, проведенных в 80–90-е годы ХХ ст. Основные результаты данного метаанализа представлены в табл. 1. Оценивая их, с уверенностью можно сказать о явном преимуществе назначения адъювантной ПХТ у пациенток в возрасте моложе 50 лет, то есть в пременопаузе: отмечено повышение 15-летней общей и безрецидивной выживаемости на 7–8% (учитывая огромный объем выборки различия имеют высочайшую степень статистической достоверности) [7].
Таблица 1. Влияние адъювантной химиотерапии на 15-летнюю безрецидивную и общую выживаемость. Метаанализ 194 рандомизированных исследований
| Возраст моложе 50 лет | Возраст старше 50 лет |
| Повышение безрецидивной выживаемости на 12,3% (2р<0,00001) |
Повышение безрецидивной выживаемости на 4,1% (2р<0,00001) |
| Повышение общей выживаемости на 10% (2р<0,00001) |
Повышение общей выживаемости на 3% (2р<0,00001) |
Особенностью второго метаанализа (табл. 2), опубликованного в 2008 г., является то, что в него включены только пациентки с эстрогеннегативными опухолями (46 рандомизированных исследований). У данной категории пациенток различия в 10-летней общей и безрецидивной выживаемости между возрастными группами гораздо менее заметны [8].
Таблица 2. Адъювантная химиотерапия у пациенток с эстрогеннегативными опухолями, влияние на 10-летнюю выживаемости. Метаанализ 46 рандомизированных исследований, проведенный EBCTCG
| Возраст моложе 50 лет | Возраст старше 50 лет |
| Повышение безрецидивной выживаемости на 12% (2р<0,00001) |
Повышение безрецидивной выживаемости на 10% (2р<0,00001) |
| Повышение общей выживаемости на 8% (2р<0,00001) |
Повышение общей выживаемости на 6% (2р<0,00001) |
В большом исследовании BCIRG 001 в адъювантном режиме схему ТАС сравнивали с FAC [11]. Из включенных в него 1491 пациентки у 192 был трижды негативный фенотип. Именно в группе ТНРГЖ отмечена самая большая разница в 3-летней безрецидивной выживаемости в пользу схемы ТАС — 14% (74% против 60%).
В исследовании CALGB 9344 пациенткам с наличием метастазов в лимфатических узлах назначали 4 курса по схеме АС (доксорубицин, циклофосфамид), после чего больные рандомизированы в группу с дальнейшим переходом на монотерапию паклитакселом (4 курса) или подвержены только наблюдению. Добавление паклитаксела статистически достоверно приводило к повышению безрецидивной выживаемости пациенток с трижды негативным и HER2-позитивным РГЖ [13].
С учетом высокого пролиферативного потенциала ТНРГЖ перспективным является применение «уплотненных» (dose-dense) режимов ПХТ с сокращением интервалов между курсами. В 2010 г. опубликован метаанализ 10 подобных ретроспективных исследований в адъювантном режиме. В целом, отмечено повышение общей и безрецидивной выживаемости при использовании dose-dense режимов. Однако авторы подчеркнули, что эти данные нуждаются в подтверждении в проспективных исследованиях [2].
В последние годы появились данные о возможной эффективности в терапии метастатического ТНРГЖ ингибиторов ангиогенеза, в частности бевацизумаба. В 2007 г. начато исследование BEATRICE, в котором пациентки с ТНРГЖ в адъювантном режиме в дополнение к антрациклин- и/или таксаносодержащей схеме ПХТ получали бевацизумаб в течение года или ограничивались наблюдением. Предварительные результаты, опубликованные в декабре 2012 г., не показали статистически достоверных различий в 3-летней безрецидивной выживаемости в обеих группах (83,7 и 82,7%) [4].
Таким образом, стратегия максимальной индивидуализации терапии РГЖ в отношении трижды негативного подтипа на сегодня не привела к утверждению каких-либо специфических рекомендаций. С практической точки зрения, единственным эффективным подходом является только цитостатическая терапия. Исследования последних лет посвящены поиску и изучению в ТНРГЖ новых «мишеней», таких как EGFR, c-kit, BRCA и других сигнальных путей; с применением соответствующих ингибиторов [1, 10, 13]. И хотя ни одна из этих стратегий пока не имела практических результатов, проводимые сейчас рандомизированные исследования позволяют надеяться на их появление в ближайшем будущем.
СПИСОК ИСПОЛЬЗОВАННОЙ ЛИТЕРАТУРЫ
1. Andre F., Zielinski C. (2013) Optimal strategies for metastatic triple negative breast cancer with currently approved agents. Ann. Oncol., 24(4): 46–51.
2. Bonilla L., Ben-Aharon I., Vidal L. et al. (2010) Dose-dense chemotherapy in nonmetastatic breast cancer: a systematic review and meta-analysis of randomized controlled trials. J. Natl. Cancer Inst., 102: 1845–1854.
3. Byrski T., Gronwald J., Huzarski T. et al. (2010) Pathologic complete response rate in young women with BRCA-positive breast cancer after neoadjuvant chemotherapy. J. Clin. Oncol., 28: 375–379.
4. Cameron D., Brown J., Dent R. et al. (2012) Primary results of BEATRICE study, evaluating adjuvant bevacizumab-containing therapy in triple negative breast cancer. Cancer research, 72(3).
5. Carey L. (2011) Directed therapy subtypes of triple negative breast cancer. The oncologist., 25(2): 141–151.
6. Dent R., Trudeau M., Pritchard K. (2007) Triple negative breast cancer: clinical features and patterns of recurrence. Clin. Cancer Res., 13(1): 4429–4434.
7. Early Breast Cancer Trialists’ Collaborative Group (EBCTCG) (2005) Effects of chemotherapy and hormonal therapy for early breast cancer on recurrence and 15-year survival: an overview of the randomised trials. Lancet, 365(9472): 1687–1717.
8. Early Breast Cancer Trialists’ Collaborative Group (EBCTCG) (2008) Adjuvant chemotherapy in oestrogen-receptor-poor breast cancer: patient-level meta-analysis of randomised trials trials. Lancet, 371: 29–40.
9. Howlader N., Noone F., Krapcho M. et al. (2013) SEER cancer statistics review, 1975-2010//SEER data submission, posted to the SEER web site.
10. Hudis C., Gianni L. (2011) Triple negative breast cancer: an unmet medical need. The oncologist, 28(2): 135–146.
11. Hugh J., Hanson J., Cheang M.C. et al. (2009) Breast cancer subtypes and response to docetaxel in node-positive breast cancer: use of an immunohistochemical definition in the BCIRG 001 trial. J. Clin. Oncol., 27: 1168–1171.
12. Huober J., Von Minckwitz G. (2010) Effect of neoadjuvant anthracycline-taxane based chemotherapy in different biological cancer phenotypes: overall results of the Gepar Trio study. Breast cancer Res. treat, 124: 133–140.
13. Joensuu H., Gligorov J. (2013) Adjuvant treatments for triple negative breast cancer. Ann. Oncol., 24: 40–45.
14. Liedtke C., Mazouni C., Hess K.R. et al. (2008) Response to neoadjuvant treatment and long-term survival in patients with triple negative breast cancer. J. Clin. Oncol., 2: 1275–1278.
15. Minckwitz G., Martin M. (2013) Neoadjuvant treatments for triple negative breast cancer. Ann. Oncol., 23(6): 35–39.
16. Perou C.M. (2000) Molecular portraits of human breast tumors. Nature, 406: 747–752.














Leave a comment